Kombination von Systemtherapie und Radiotherapie beim Mammakarzinom
Autor:
OA Dr. Erich Gerber
Zentrum für Radioonkologie und Strahlentherapie
Klinik Donaustadt, Wien
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Zahlreiche neue Substanzklassen zur adjuvanten und palliativen Systemtherapie des Mammakarzinoms haben im letzten Jahrzehnt Eingang in den klinischen Alltag gefunden. Diese rasche Entwicklung brachte große Fortschritte in Verträglichkeit und Wirksamkeit der Behandlung mit sich und führte bei manchen Subtypen des Mammakarzinoms zu einer deutlichen Verbesserung der Prognose. Dabei stellt sich auch die Frage, wie diese neuen Therapeutika mit der Radiotherapie kombiniert werden können und welche Folgen für Tolerabilität und Effizienz daraus resultieren.
Keypoints
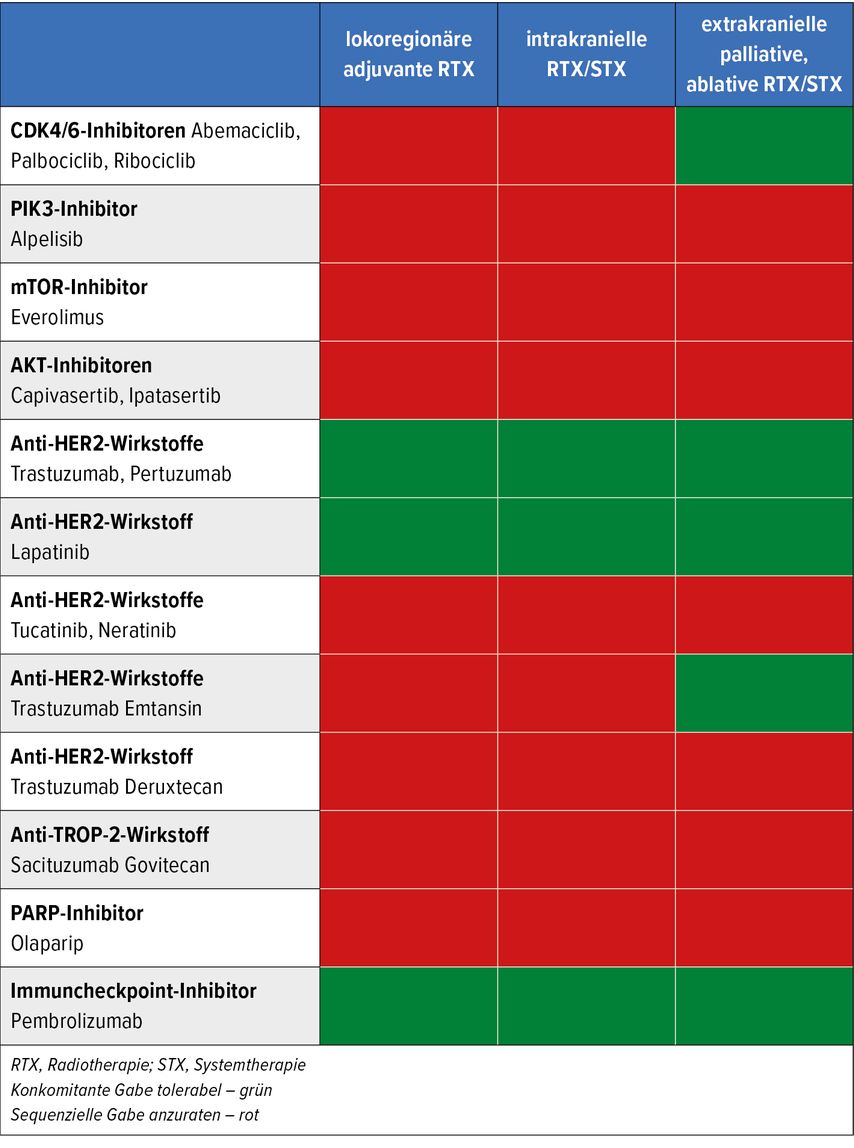
Für die meisten neuen Substanzen liegen keine ausreichenden Daten vor, um eine konkomitante Gabe mit einer Radiatio zu empfehlen (Tab. 1).
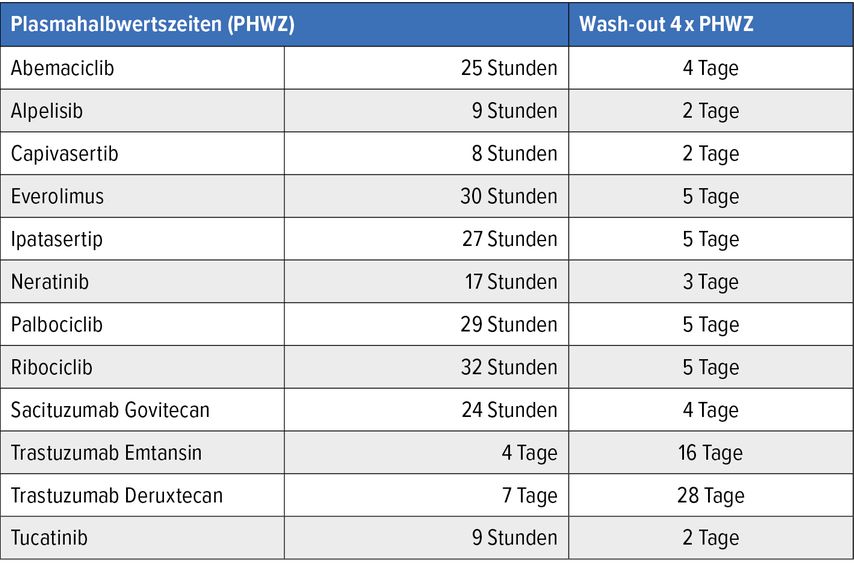
Bei sequenzieller Anwendung ist ein Wash-out mit vier bis fünf Halbwertszeiten als ausreichend anzusehen (Tab. 2).
Um eine gute Verträglichkeit zu gewährleisten, wurde in den bisherigen Phase-III-Studien zumeist darauf geachtet, Systemtherapie und Radiotherapie sequenziell einzusetzen. Damit fehlen für viele neue Substanzen belastbare Daten zur konkomitanten Anwendung. Dies gilt auch für andere Tumorentitäten, wenngleich das Mammakarzinom besonders stark davon betroffen ist, weil die Radiotherapie adjuvant und palliativ fast immer zum Einsatz kommt.
Dies war schließlich der Anlass für die ESTRO (European Society for Radiotherapy and Oncology), einen Konsensus für die Anwendung der Radiotherapie beim Mammakarzinom interdisziplinär erarbeiten zu lassen.1 Es waren Repräsentant:innen aus Epidemiologie, Statistik, medizinischer Onkologie, Radioonkologie und präklinischer Forschung vertreten. Aus der medizinischen Onkologie waren es unter anderem Nadia Harbeck, Javier Cortés, Giuseppe Curigliano und Hope Rugo.
Der zentrale Endpunkt war die Sicherheit einer konkomitanten Anwendung. Wenn die Datenlage nicht eindeutig war, konnte nur eine sequenzielle Anwendung empfohlen werden. Für diese Situation wurde eine Wash-out-Periode von zumindest vier bis fünf Halbwertszeiten festgelegt. Vom klinischen Einsatz her wurde unterschieden zwischen adjuvanter und metastasierter Situation, ablativer und palliativer Bestrahlung sowie intra- und extrakranieller Indikation. Die Datenlage wurde in vielen dieser Szenarien als gering oder sehr gering mit klinischer Evidenz unterlegbar eingeschätzt.
CDK4/6-Inhibitoren
In der adjuvanten Situation fehlen Daten zur konkomitanten Gabe von CDK4/6-Inhibitoren und lokoregionärer Bestrahlung. In der Studie monarchE war gefordert, dass die lokale Therapie, sei es Operation, sei es Radiotherapie, abgeschlossen und die therapeutischen Reaktionen abgeklungen sein mussten, ehe die Behandlung mit Abemaciclib begonnen werden konnte.
Was die Behandlung von Hirnmetastasen und eine konkomitante Gabe von CDK4/6-Inhibitoren betrifft, fehlen ebenfalls ausreichende Daten, um dies bei Ganzhirnbestrahlung oder intrakranielle Stereotaxie empfehlen zu können.
Die palliative Bestrahlung extrakranieller Metastasen kann unter Berücksichtigung von Lokalisation, Bestrahlungsvolumen und Dosis auch konkomitant angewendet werden.
Immuncheckpoint-Inhibitoren
Für die adjuvante Situation liegen die Ergebnisse der Studie KEYNOTE-522 mit Pembrolizumab beim tripelnegativen Mammakarzinom vor. Die Erfahrungen stützen sich auf 280 Patient:innen mit sequenzieller und 144 mit konkomitanter adjuvanter Radiotherapie im Arm mit Pembrolizumab und auf 159 Patient:innen mit sequenzieller und 91 mit konkomitanter Bestrahlung im Placeboarm.
Ohne adjuvante Radiatio waren 330 Patient:innen mit Pembrolizumab und 129 mit Placebo behandelt worden. Das mediane Follow-up betrug mit Pembrolizumab 41 Monate bei sequenzieller und 35 Monate bei konkomitanter Radiatio. Es zeigte sich durch die adjuvante Radiotherapie kein negativer Einfluss auf das ereignisfreie Überleben. Auch hatten weder sequenzielle noch konkomitante Bestrahlung eine erhöhte Toxizität zur Folge. Der Konsensus war, die Radiotherapie in der adjuvanten Situation auch in Kombination mit Pembrolizumab zu empfehlen. Für weitere Substanzen der Immuntherapeutika liegen in der adjuvanten Situation vorerst keine ausreichenden Daten vor.
Bei Oligometastasierung erscheint die Kombination mit stereotaktischer Bestrahlung sicher, allerdings gibt es keine Hinweise auf eine positive Wirkung durch die Radiatio.
Im polymetastatischen Setting war ebenfalls keine erhöhte Toxizität zu beobachten und die Erfahrungen bezüglich der Wirkung sind vielversprechend, bedürfen aber noch der Bestätigung durch die laufenden Phase-III-Studien.
PARP-Inhibitoren
Angesichts überschaubarer Patient:innenzahlen und der damit vorliegenden Erfahrungen konnte nur ein Konsens gefunden werden, von der konkomitanten Anwendung außerhalb von Studien abzusehen, sowohl palliativ als auch adjuvant.
PIK3-, AKT- und mTOR-Inhibitoren
Für Inhibitoren von PIK3 (Alpelisib) und AKT (Capivasertib, Ipatasertib) fehlen die Daten und bei m-TOR-Inhibitoren (Everolimus) zeigte sich ein klar erhöhtes Risiko für toxische Reaktionen bei konkomitanter Anwendung.
Anti-HER2-Wirkstoffe und Non-ADC
Trastuzumab und Pertuzumab stellen für die adjuvante Anwendung mit konkomitanter Radiotherapie kein Sicherheitsrisiko dar. Es wurde nach Einführung neuer radiotherapeutischer Techniken auch keine erhöhte Kardiotoxizität beobachtet.
Bei konkomitanter Behandlung von Hirnmetastasen mit Ganzhirnbestrahlung oder Stereotaxie gibt es für Trastuzumab und Pertuzumab keine Hinweise auf verstärkte toxische Reaktionen.
Lapatinib wurde ebenfalls als sicher bei konkomitanter adjuvanter und palliativer Radiotherapie eingeschätzt. Die Stereotaxie von Hirnmetastasen in Kombination mit Lapatinib ergab eine höhere Lokalkontrolle ohne erhöhtes Risiko für Radionekrosen.
Für die weiteren Tyrosinkinase-Inhibitoren Tucatinib, Pyrotinib und Neratinibkann aufgrund des Fehlens von Daten für die konkomitante nur die sequenzielle Applikation empfohlen werden.
ADC, Anti-HER2, Anti-TROP-2
Die vorerst größte klinische Bedeutung aller ADC in Kombination mit Radiotherapie hat Trastuzumab Emtansin aufgrund der Indikation in der adjuvanten Situation bei residualem Tumor nach neoadjuvanter Applikation von Chemotherapie in Kombination mit Trastuzumab und Pertuzumab. Die Datenlage unterstützt die konkomitante Anwendung von Radiotherapie und Trastuzumab Emtansin. Was das Fraktionierungsschema angeht, ist die Hypofraktionierung mit 15 Fraktionen über drei Wochen verträglicher als die ehemalige Standardfraktionierung mit einer 2-Gray-Einzeldosis über fünf Wochen.
In der ATEMPT-Studie zeigten sich keine Unterschiede in der mit der Radiotherapie assoziierten Toxizität zwischen Trastuzumab und Trastuzumab Emtansin hinsichtlich einer Pneumonitis und Reduktion der linksventrikulären Auswurffraktion, aber verstärkte Hautreaktionen, vor allem beim Langzeitschema der Bestrahlung.2
Bei der Behandlung von Hirnmetastasen ist der Konsensus ebenfalls eindeutig und die Empfehlung lautet, von einer konkomitanten Bestrahlung Abstand zu nehmen. Bei konkomitanter Gabe von Trastuzumab Emtansin und stereotaktischer Bestrahlung war ein zum Teil massiv erhöhtes Risiko für Radionekrosen zu beobachten. Für die Ganzhirnbestrahlung ist die berichtete klinische Erfahrung unzureichend und angesichts der potenziellen Risiken ist auch davon im klinischen Alltag abzuraten.
Für TrastuzumabDeruxtecan und SacituzumabGovitecan liegen keine Daten für konkomitante Anwendungen vor.
Fazit
Zusammenfassend ist leider festzustellen, dass für viele neue Substanzen keine ausreichenden Daten zur konkomitanten Anwendung mit Strahlentherapie vorliegen und mit großer Wahrscheinlichkeit auch gut tolerable und effizienzsteigernde kombinierte Anwendungen als solche nicht erfasst werden können. Es ist zu hoffen, dass zukünftige Studien die Dokumentation der Radiotherapie inkludieren und auch entsprechende Analysen erlauben werden.
Literatur:
1 Meattini I et al.: International multidisciplinary consensus on the integration of radiotherapy with new systemic treatments for breast cancer: European Society for Radiotherapy and Oncology(ESTRO)-endorsed recommendations. Lancet Oncol 2024; 25(2): e73-83 2 Bellon JR et al.: Local therapy outcomes and toxicity from the ATEMPT trial (TBCRC 033): a phase II randomized trial of adjuvant trastuzumab emtansine versus paclitaxel in combination with trastuzumab in women with stage I HER2-positive breast cancer. Int J Radiat Oncol Biol Phys 2022; 113(1): 117-24
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...