
Immuntherapie als Standard beim fortgeschrittenen nicht kleinzelligen Lungenkarzinom?
Quelle: European Lung Cancer Conference (ELCC), 5.–8. Mai 2017, Genf
Die Immuntherapie hat beim fortgeschrittenen nicht kleinzelligen Lungenkarzinom innerhalb kurzer Zeit einen hohen Stellenwert erreicht. Doch kann diese Option bereits als Therapiestandard angesehen werden und die bisherige Behandlung sowohl in der ersten als auch der zweiten Linie ersetzen? Dr. Giannis Mountzios gab den Kongressbesuchern seine Antwort auf diese Frage, untermauert durch entsprechende Daten.
Im Zusammenhang mit der Behandlung fortgeschrittener nicht kleinzelliger Lungenkarzinome (NSCLC) ist der Begriff „Immuntherapie“ mittlerweile in aller Munde. Auf der European Lung Cancer Conference (ELCC) in Genf befasste sich eine der vielen Veranstaltungen mit der Frage, ob diese Art der Therapie beim NSCLC bald als Standard anzusehen ist. Dr. Giannis Mountzios (Athen/GR) erklärte zu Beginn seines Vortrags: „Die Immuntherapie bei Tumoren ist eigentlich gar nicht so neu, wie wir vielleicht denken würden. Bereits 1972 wurden elektronenmikroskopische Aufnahmen publiziert, die T-Lymphozyten zeigten dabei, wie sie Tumorzellen attackieren.“ Einzig das Wissen über die molekularen Mechanismen, die der Interaktion zwischen den Zellen des Immunsystems und den Tumorzellen zugrunde liegen würden, sei seither entscheidend gewachsen. „Dadurch wurden wir in die Lage versetzt, hier gezielt eingreifen zu können.“
Zweite Linien: Immuntherapie oder Chemotherapie?
Im ersten Teil seines Vortrags ging Dr. Mountzios auf den Stellenwert der Immuntherapie in der Zweitlinientherapie des NSCLC ein. „Schauen wir uns dazu einmal die Datenlage an“, meinte er. Die beiden Phase-III-Studien CheckMate 017 (plattenepitheliale Tumoren) und CheckMate 057 (nicht plattenepitheliale Tumoren) untersuchten die Zweitlinientherapie mit dem Anti-PD-1-Antikörper Nivolumab im Vergleich zu Docetaxel.1, 2 Dabei zeigte sich ein klarer Überlebensvorteil für die mit Nivolumab behandelten Patienten. Das 2-Jahres-Update ergab für Patienten mit plattenepithelialen Tumoren ein medianes Gesamtüberleben (OS) von 9,2 Monaten unter Nivolumab vs. 6,0 Monate unter Docetaxel.3 „Wir alle wissen, dass eine Verlängerung des Überlebens von rund 3 Monaten in der Zweitlinientherapie plattenepithelialer Lungenkarzinome nicht nur statistisch, sondern auch klinisch von Bedeutung ist“, erläuterte der Redner dazu. Bei den Patienten mit nicht plattenepithelialen Tumoren ergab CheckMate 057 nach 2 Jahren ein medianes OS von 12,2 Monaten unter Nivolumab im Vergleich zu 9,5 Monaten unter Chemotherapie. „Bei den plattenepithelialen Tumoren profitierten alle Patienten von Nivolumab, unabhängig von der PD-L1-Expression. Bei den nicht plattenepithelialen Tumoren profitierten ebenfalls alle Patienten, jedoch stieg der Nutzen mit zunehmender PD-L1-Expression an“, präzisierte Dr. Mountzios.
Ähnliche Resultate liegen aus der Studie KEYNOTE-010 vor.4 Hier erhielten vorbehandelte Patienten mit einem PD-L1-exprimierenden NSCLC (Tumor-Proportion-Score [TPS] ≥1 % ) entweder Pembrolizumab oder Docetaxel. Nach einem medianen Follow-up von 19,2 Monaten betrug das mediane OS unter Pembrolizumab 2mg/kg für Patienten mit einem TPS ≥1 % 10,5 Monate vs. 8,6 Monate unter Docetaxel (HR: 0,72; p=0,0003).5 Patienten mit einem TPS ≥50 % profitierten noch deutlicher von der Immuntherapie. Hier lag das mediane OS bei 15,8 Monaten unter Nivolumab vs. 8,2 Monate unter Docetaxel.
Der erste Anti-PD-L1-Antikörper in der Zweitlinientherapie, Atezolizumab, schließlich erreichte in der OAK-Studie nach einem minimalen Follow-up von 19 Monaten ein medianes OS von 13,8 Monaten (vs. 9,6 Monate unter Docetaxel, HR: 0,73; p=0,0003).6 „Das ist das erste Mal, dass wir uns bei einer gemischten Patientenpopulation – mit plattenepithelialen und nicht plattenepithelialen Tumoren – einem Überleben von 14 Monaten annähern“, kommentierte Dr. Mountzios dies. „Ich denke, wir können also die Frage, ob die Immuntherapie eine Chemotherapie in der zweiten Therapielinie des fortgeschrittenen NSCLC ersetzen kann, klar mit Ja beantworten.“
Stellenwert der Immuntherapie in der ersten Linie
Im zweiten Teil seines Referates widmete sich Dr. Mountzios der Rolle der Immuntherapie in der ersten Therapielinie. „Hier sieht die Situation insgesamt etwas komplizierter aus“, erklärte er einleitend und gab im Anschluss wiederum einen Überblick über die Datenlage.
Die Erstlinientherapie mit Pembrolizumab wurde in der Studie KEYNOTE-024 untersucht.7 Patienten mit einem TPS von mindestens 50 % erhielten entweder eine fixe Pembrolizumab-Dosis oder eine Platin-basierte Chemotherapie-Doublette. „Ein wichtiger Aspekt dieser Studie ist, dass fast 2000 Patienten gescreent werden mussten, um schliesslich 500 Patienten mit der gewünschten hohen PD-L1-Expression selektionieren zu können“, so der Redner. „Aufgrund weiterer Kriterien wie z.B. des Performance-Status, des Vorliegens instabiler Hirnmetastasen etc., konnten von ihnen schließlich nur 305 in die Studie eingeschlossen werden. Es handelt sich hier also um eine stark selektionierte Patientenpopulation.“
KEYNOTE-024 zeigte schließlich für Pembrolizumab ein medianes progressionsfreies Überleben (PFS) von 10,3 Monaten vs. 6,0 Monate unter Chemotherapie (HR für Progression oder Tod: 0,50; 95 % CI: 0,37–0,68; p<0,001). Die geschätzte OS-Rate nach 6 Monaten betrug 80,2 % in der Pembrolizumab-Gruppe vs. 72,4 % in der Vergleichsgruppe (p=0,005). „Dies war das erste Mal, dass mit einer Checkpoint-Inhibitor-Monotherapie in der ersten Linie bei einer selektionierten Patientensubpopulation mit einem fortgeschrittenen NSCLC ein signifikanter Überlebensvorteil gegenüber einer Chemotherapie erzielt werden konnte“, kommentierte Dr. Mountzios die Resultate. Die Studie zeigte des Weiteren auch eine signifikant höhere Rate des objektiven Ansprechens (ORR) unter Pembrolizumab im Vergleich zur Chemotherapie (44,8 % vs. 27,8). „Dies ist für die Erstlinientherapie eines fortgeschrittenen NSCLC eine sehr gute Ansprechrate“, so der Redner.
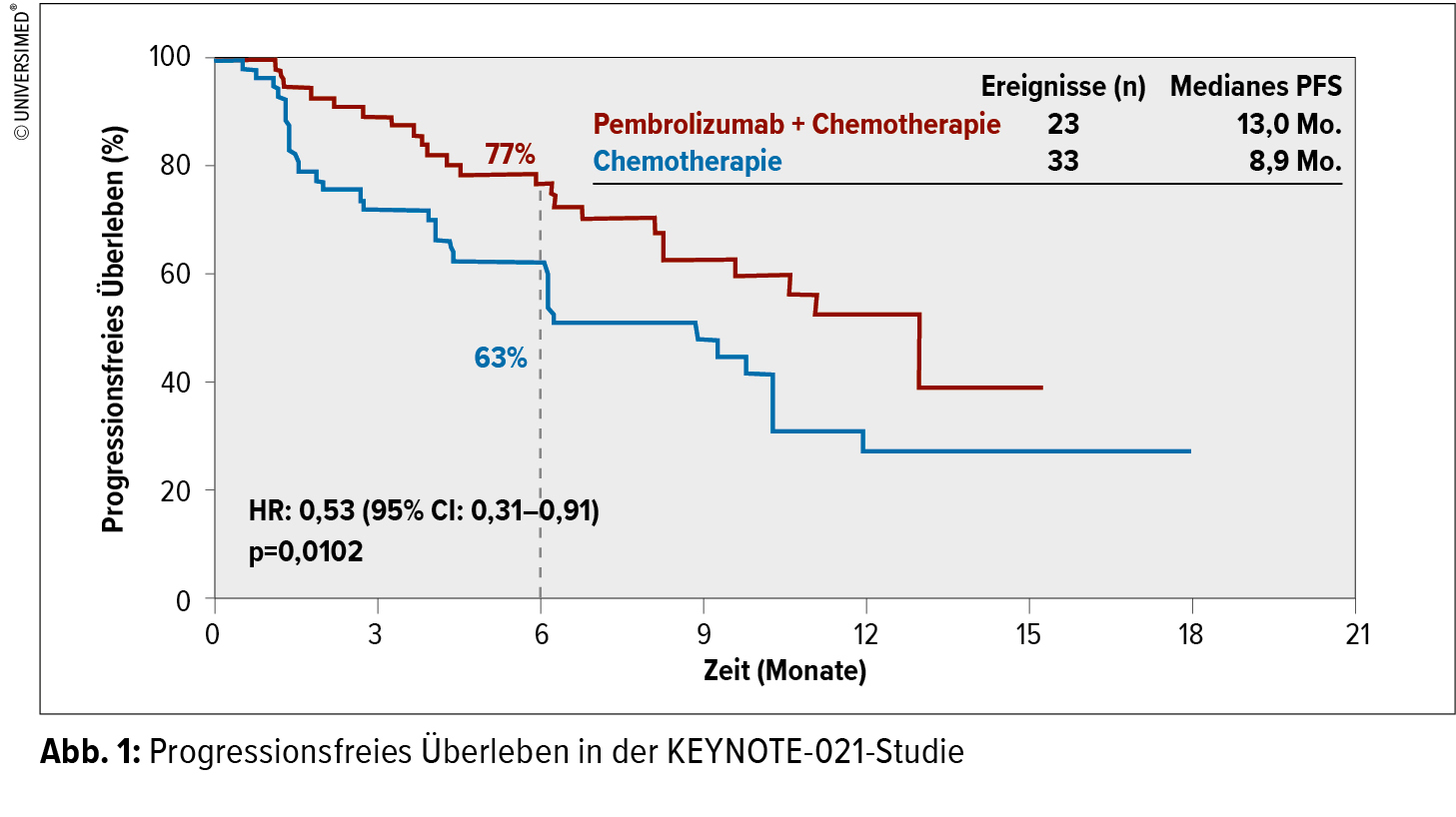
In einer Kohorte der Studie KEYNOTE-021 (Cohort G) wurde Pembrolizumab zusätzlich zu einer Chemotherapie mit Pemetrexed und Carboplatin bzw. die Chemotherapie alleine als Erstlinientherapie bei Patienten mit nicht plattenepithelialen NSCLC untersucht.8 Der primäre Endpunkt dieser Phase-II-Studie war die ORR. Nach einem medianen Follow-up von 10,6 Monaten lag diese im Studienarm bei 55 % gegenüber 29 % im Kontrollarm (HR: 0,53; p=0,0102). „Dies ist eine eindrückliche Ansprechrate“, meinte Dr. Mountzios. „Zudem wurde das progressionsfreie Überleben im Studienarm gegenüber dem Kontrollarm mit 13,0 Monaten vs. 8,9 verlängert.“ (Abb. 1) Obwohl die eingeschlossenen Patienten nicht anhand der PD-L1-Expression selektioniert worden waren, konnte in einer entsprechenden Analyse bei den Patienten mit einer PD-L1-Expression von mindestens 50 % eine höhere Ansprechrate unter Pembrolizumab plus Chemotherapie (etwa 80 % ) festgestellt werden.
Die Studie CheckMate 026 schließlich untersuchte eine Erstlinientherapie mit Nivolumab im Vergleich zu einer Platin-basierten Chemotherapie-Doublette.9 „Eingeschlossen wurden Patienten mit einer PD-L1-Expression von mindestens einem Prozent. Der primäre Endpunkt war jedoch das progressionsfreie Überleben bei Patienten mit einer Expression von mindestens fünf Prozent“, erläuterte der Redner. Diese Studie war klar negativ, kam es doch zu keiner Verlängerung des progressionsfreien und des Gesamtüberlebens. „Eine Post-hoc-Analyse zeigte zudem, dass die Kombination selbst bei Patienten mit einer PD-L1-Expression von 50 Prozent oder mehr kein besseres Resultat als die Chemotherapie allein erreichte“, ergänzte Dr. Mountzios. „Damit stellt die Immuntherapie in der ersten Linie für mich nicht generell einen Ersatz für die Chemotherapie dar, sondern nur bei anhand der PD-L1-Expression selektionierten Patienten“, schloss er seine Ausführungen.
1 Brahmer J et al: Nivolumab versus docetaxel in advanced squamous-cell non-small-cell lung cancer. N Engl J Med 2015; 373: 123-35 2 Borghaei H et al: Nivolumab versus docetaxel in advanced non-squamous non-small-cell lung cancer. N Engl J Med 2015; 373: 1627-39 3 Barlesi F et al: Long-term outcomes with nivolumab vs docetaxel in patients with advanced NSCLC: CheckMate 017 and CheckMate 057 2-y Update. ESMO 2016; Abstract 1215PD 4 Herbst RS et al: Pembrolizumab versus docetaxel for previously treated, PD-L1-positive, advanced non-small-cell lung cancer (KEYNOTE-010): a randomised controlled trial. Lancet 2016; 387: 1540-50 5 Herbst RS et al: Pembrolizumab versus docetaxel for previously treated, PD-L1–expressing NSCLC: updated outcomes of KEYNOTE-010. ESMO 2016; Abstract LBA48 6 Barlesi F et al: Primary analysis from OAK, a randomized phase III study comparing atezolizumab with docetaxel in 2L/3L NSCLC. ESMO 2016; Abstract LBA44_PR 7 Reck M et al: Pembrolizumab versus chemotherapy for PD-L1–positive non–small-cell lung cancer. N Engl J Med 2016; 375: 1823-33 8 Langer C et al: Randomized, phase 2 study of carboplatin and pemetrexed with or without pembrolizumab as first-line therapy for advanced NSCLC: KEYNOTE-021 cohort G. ESMO 2016; Abstract LBA46_PR 9 Socinski M et al: CheckMate 026: A phase 3 trial of nivolumab vs investigator's choice of platinum-based doublet chemotherapy as first-line therapy for stage IV/recurrent programmed death ligand 1-positive NSCLC. ESMO 2016; Abstract LBA7_PR
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...


