Hormonersatzbehandlung nach Krebstherapie
Autorin:
Priv.-Doz. Dr. Gunda Pristauz-Telsnigg
Leiterin Schwerpunkt Brusterkrankungen
Abteilung für Gynäkologie
Univ.-Frauenklinik Graz
E-Mail: gunda.pristauz@klinikum-graz.at
Gerade bei der Therapie von gynäkologischen Krebserkrankungen kommt es durch Chemo- oder Radiotherapien häufig zu einer iatrogen induzierten Menopause. Die daraus resultierenden klimakterischen Symptome können akut einsetzen und schwerer verlaufen als die natürliche Menopause. Die effektivste Therapie zur Bekämpfung klimakterischer Beschwerden ist die Hormonersatztherapie (HRT), doch ist diese nach einer Krebstherapie überhaupt möglich?
Grundsätzlich stand man bisher dem Einsatz von Hormonersatzpräparaten nach einer gynäkologischen Krebstherapie eher ablehnend gegenüber. Die wissenschaftlichen Daten hierfür sind auch spärlich, und wenn vorhanden, dann nur von mangelnder Qualität. Studien wurden mit geringen Fallzahlen durchgeführt und ergaben teils kontroversielle Ergebnisse. Zieht man eine Hormonersatztherapie (HRT) für Patientinnen nach einer gynäkologischen Krebserkrankung in Betracht, sollte die Patientin über die schlechte Datenlage hierzu informiert werden.
Im Folgenden sei nun auf die unterschiedlichen Krebserkrankungen im Fachbereich der Gynäkologie eingegangen.
Endometriumkarzinom
Das mediane Erkrankungsalter beim Endometriumkarzion ist 69 Jahre, aber 25% der Patientinnen befinden sich in der Prämenopause und 2,5–14% der Frauen sind bei der Diagnose sogar jünger als 40 Jahre.1 2018 versuchte ein systematischer Review der Cochrane Data Base die Frage zu beantworten, ob eine HRT bei Patientinnen nach Endometriumkarzinom möglich ist. Insgesamt 8 Studien wurden analysiert. Daten von 2190 Patientinnen wurden untersucht.2 Patientinnen, die eine Östrogensubstitution erhalten hatten, zeigten eine Rezidivrate von 2,3% versus 1,9% der Patientinnen in den Placebogruppen (relatives Risiko [RR]: 1,17; Konfidenzintervall [CI]: 0,54–2,50). Nach einer Nachbeobachtungszeit von 36 Monaten waren 94,3% der Patientinnen in der HRT-Gruppe am Leben versus 96,9% in der Placebogruppe. Die Autoren schlossen daraus, dass die Daten nicht ausreichen, um eine HRT nach Endometriumkarzinom empfehlen zu können.
Andere Autoren plädieren für eine individuelle Betreuung von Patientinnen mit Endometriumkarzinom und sind der Meinung, dass eventuell nach genauer Aufklärung das frühe endometrioide niedriggradige Karzinome eine Ausnahme in Bezug auf eine HRT darstellen könnte, v.a. wenn die Krebstherapie schon mehr als zwei Jahre zurückliegt.3
Eine lokale Östrogentherapie gerade bei nicht zufriedenstellender Behandlung mit Gleitgels oder Cremen ist allerdings jederzeit möglich.4
Ovarialkarzinom
Obwohl das mediane Erkrankungsalter beim Ovarialkarzinom 69 Jahre ist, erkranken doch 35% der Patientinnen vor der Menopause.5 Ein 2015 erschienener Review und eine Metaanalyse von Li et al.6 haben sechs Studien zur HRT nach einem epithelialen Ovarialkarzinom zusammengefasst. 419 Patientinnen mit epithelialen Ovarialkarzinomen, die unter HRT standen, wurden mit 1029 Patientinnen mit epithelialen Ovarialkarzinomen ohne HRT verglichen und hinsichtlich der Rezidivrate untersucht. Es konnte keine Erhöhung des Risikos für ein Rezidiv unter HRT festgestellt werden, mit einem relativen Risiko von 0,83 (95% CI: 0,64–1,07).
Auch in der aktuellen AWMF-S3-Leitlinie „Ovarialkarzinom“ ist eine konsensbasierte Empfehlung in Bezug auf die Möglichkeit einer HRT nach Ovarialkarzinom festgehalten.7
Eine Ausnahme scheint allerdings bei den Granulosazelltumoren des Ovars gegeben zu sein. Hier sollte auf eine HRT verzichtet werden.3
Zervixkarzinom
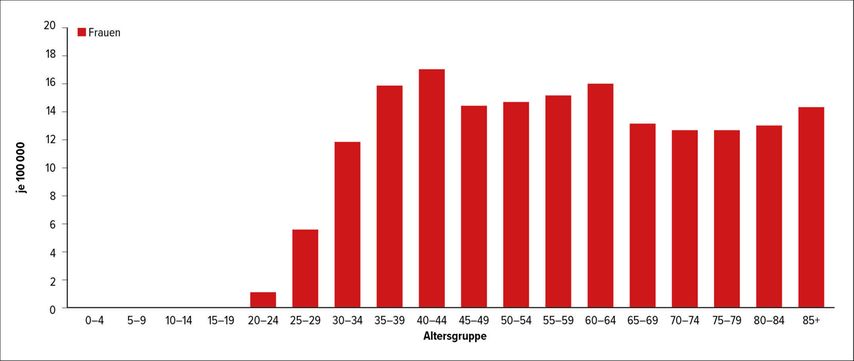
Das Zervixkarzinom ist sicherlich das gynäkologische Malignom der jungen Frau. In Abbildung 1 kann man die Altersverteilung der Patientinnen zum Zeitpunkt der Diagnose Zervixkarzinom in Deutschland sehen. Ein Großteil der Patientinnen hat das 54. Lebensjahr noch nicht vollendet. Bei der Behandlung des Zervixkarzinoms werden zwar grundsätzlich die Ovarien ausgespart, sei es durch eine Wertheim-Operation oder Radiochemotherapie. Trotzdem kommt es sehr häufig zu einer verfrühten Menopause.
Abb. 1: Altersspezifische Erkrankungsraten mit bösartigen Neubildungen der Cervix uteri (ICD-10 C53) bei Frauen in Deutschland 2015–2016. Modifiziert nach: Zentrum für Krebsregisterdaten11
Die Datenlage zur HRT beim Zervixkarzinom ist extrem schlecht, weshalb sich ein Blick auf Daten zur hormonellen Kontrazeption und zur Entwicklung eines Zervixkarzinoms lohnt. Appleby et al.8 konnten in einer Studie zeigen, dass die Kombinationspille bei HPV(humane Papillomaviren)-positiven Patientinnen das Zervixkarzinomrisiko erhöht (RR von 3,8 auf 4,5/1000 Frauen). Dies könnte eventuell durch eine modulatorische Wirkung des Östrogens, welche die Empfindlichkeit der Zellen gegenüber HPV erhöht, verursacht werden, denn eine rein gestagenhältige Pille zeigte keine Inzidenzerhöhung beim Zervixkarzinom.
Vorsicht geboten ist allerdings bei den Adenokarzinomen der Zervix, die ca. 15% aller Zervixkarzinome ausmachen. Ein Drittel der Adenokarzinome weist Östrogenrezeptoren auf, bei denen eine hormonelle Interaktion vermutet wird. So konnte in einer Studie bei Patientinnen mit einem Adenokarzinom der Zervix und unter einer Östrogen-Monotherapie ein deutlich erhöhtes Rezidivrisiko festgestellt werden (Odds Ratio [OR]=2,07; 95% CI: 1,1–6,8).3 Deswegen sollte bei Patientinnen mit einem Adenokarzinom der Zervix auf eine HRT verzichtet werden.
Mammakarzinom
Bezüglich des Mammakarzinoms und einer Hormonersatztherapie liegen die meisten wissenschaftlichen Daten zu gynäkologischen Malignomen vor. Nicht außer Acht gelassen werden darf allerdings die Tatsache, dass ca. 80% der Mammakarzinome hormonrezeptorpositiv sind und Hormone somit proliferativ wirken. Auf die zwei bekanntesten Studien zur HRT nach Mammakarzinom wird im Folgenden eingegangen.
In der HABITS-Studie wurden 434 Mammakarzinompatientinnen randomisiert in eine Gruppe unter HRT und eine ohne HRT. Bereits nach einer sehr kurzen Follow-up-Zeit von median nur einem Jahr zeigten sich in der HRT-Gruppe 26 Rezidive verglichen mit nur 7 Rezidiven in der Gruppe ohne HRT. Die Studie wurde daraufhin aufgrund des deutlich erhöhten Rezidivrisikos abgebrochen (RR: 3,41; 95% CI: 1,59–7,33)9
In der LIBERATE-Studie wurden 3148 Frauen mit einem durchschnittlichen Alter von 52,7 Jahren zwei Jahre nach ihrer Brustkrebserkrankung randomisiert in eine Gruppe, welche Tibolon erhielt, und eine, welche nur Placebo erhielt. Die mediane Nachbeobachtungszeit war 3,1 Jahre. In der Tibolon-Gruppe kam es zu einem statistisch signifikanten Anstieg von Rezidiven mit 15,2% versus 10,7% in der Placebogruppe (HR: 1,40; 95% CI: 1,14–1,70).10
Somit kann eine systemische HRT sowie auch die Tibolon-Gabe bei Patientinnen nach Brustkrebs generell nicht empfohlen werden. Ebenso ist von einer hormonellen Kontrazeption Abstand zu nehmen. Eine eventuell mögliche Ausnahme könnte bei den tripelnegativen Brustkrebspatientinnen mit großem Leidensdruck nach genauester Aufklärung bestehen. Eine lokale intravaginale Östrogentherapie scheint allerdings möglich zu sein.
Vaginalkarzinom/Vulvakarzinom
Hier sind die wissenschaftlichen Daten besonders spärlich, in einer epidemiologischen Arbeit konnte kein Zusammenhang zwischen dem Auftreten von Vaginal- oder Vulvakarzinomen und der Einnahme von Hormonen gezeigt werden. So scheint die Hormongabe zumindest nicht kontraindiziert zu sein. Vorsicht ist allerdings bei den seltenen Adenokarzinomen der Vagina und Vulva geboten.
Zusammenfassung
Vor der Einleitung einer HRT bei Patientinnen mit gynäkologischen Malignomen und abgeschlossener Krebstherapie sollten die Patientinnen über die Vor- und Nachteile v.a. hinsichtlich des Rezidivrisikos ausführlich aufgeklärt werden.
Literatur:
1 Aoki D: J Obstet Gynecol Res 2014; 40(2): 338-48 2 Edey K et al.: Cochrane Database Syst Rev 2018; 2018(5): CD008830 3 Angioli et al.: Crit Rev Oncol Hematol 2018; 124: 51-60 4 Leitlinienprogramm Onkologie (Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF): 2018. AWMF Registernummer: 032/034-OL 5 Moorman PG et al.: Am J Epidemiol 2008: 167(9): 1059-69 6 Li D et al.: Gynecol Oncol 2015; 139(2): 355-62 7 Leitlinienprogramm Onkologie (Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF): 2020. AWMF-Registernummer: 032/035OL 8 International Collaboration of Epidemiological Studies of Cervical Cancer: Lancet 2007; 370(9599): 1609-21 9 Holmberg L et al.: Lancet 2004; 363(9407): 453-5 10 Kenemans P et al.: Lancet Oncol 2009; 10(2): 135-46 11 Zentrum für Krebsregisterdaten, Gesellschaft der Epidemiologischen Krebsregister in Deutschland e.V.: Robert Koch Institut 2019, Berlin
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...