Hodentumoren im Stadium I: Active Surveillance oder adjuvante Therapie?
Autorin:
OÄ Dr. med. Stefanie Fischer
Fachärztin für Medizinische Onkologie
Oberärztin Klinik für Medizinische Onkologie und Hämatologie, St. Gallen
E-Mail: stefanie.fischer@kssg.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Mehrheit der Keimzelltumoren präsentiert sich im Stadium I. Nach der operativen Behandlung mittels Orchiektomie stellt sich die Frage des weiteren Vorgehens: Active Surveillance oder adjuvante Therapie? Mit einem optimalen Management ist die Prognose dieser Patienten exzellent. Das Ziel der Behandlung sollte ein bestmögliches onkologisches Resultat bei zugleich möglichst geringer Toxizität sein.
Keypoints
-
60–80% der Keimzelltumoren präsentieren sich im StadiumI.
-
Das Stadium I ist eine auf den Hoden limitierte Erkrankung. Die Orchiektomie ist die primäre Therapie.
-
Active Surveillance ist für die meisten Patienten mit einem Seminom im Stadium I die präferierte Option.
-
Bei Nicht-Seminomen empfiehlt sich ein risikoadaptiertes Vorgehen basierend auf der lymphovaskulären Invasion (LVI): Active Surveillance für LVI-negative Patienten und ein Zyklus adjuvante Chemotherapie mit BEP als Option für LVI-positive Patienten.
Keimzelltumoren des Hodens stellen die häufigste maligne Erkrankung bei jungen Männern zwischen 20 und 40 Jahren dar. Die Inzidenz liegt bei 3–10/100000, wobei insbesondere in der kaukasischen Bevölkerung eine Zunahme zu verzeichnen ist.1
Für seminomatöse Keimzelltumoren liegt die höchste Inzidenz in der vierten Lebensdekade. Nicht-Seminome treten oftmals in noch jüngerem Alter auf, mit einer Peak-Inzidenz in der dritten Dekade des Lebens.
60–80% der Keimzelltumoren präsentieren sich bei Diagnosestellung im Stadium I. Dieses ist definiert als eine auf den Hoden limitierte Erkrankung ohne Hinweis auf Metastasen und mit normalen postoperativen Tumormarkern.
Die Prognose im Stadium I ist mit einer Rate des krebsspezifischen 10-Jahres-Überlebens von über 99% exzellent, setzt jedoch ein optimales Management im Falle eines Rezidivs voraus. Für Seminome und Nicht-Seminome im Stadium I gibt es verschiedene Optionen des postoperativen Managements, welche im Folgenden näher aufgeführt und diskutiert werden.
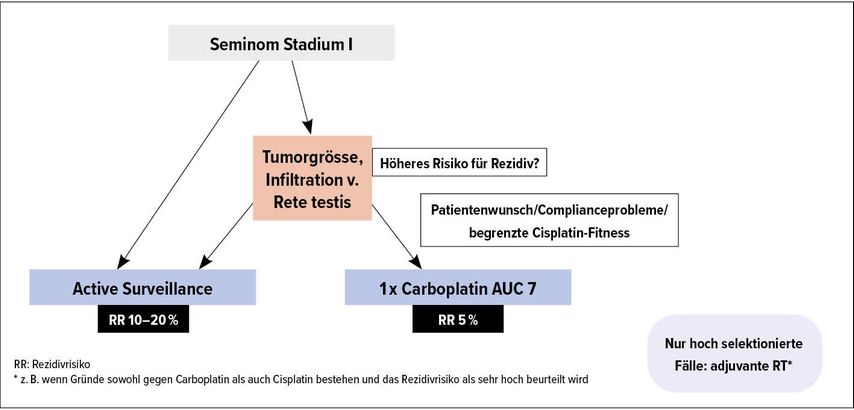
Seminome im Stadium I
Für Patienten mit einem Seminom im Stadium I besteht ohne adjuvante Therapie ein Rezidivrisiko von geschätzt 10–20%. Die Tumorgrösse und der histologische Nachweis einer Infiltration des Rete testis wurden als mögliche Faktoren identifiziert, welche das Risiko für ein systemisches Rezidiv erhöhen.2–4 Die zugrunde liegende Datenqualität der Studien wird jedoch als unzureichend kritisiert.5 Der Stellenwert dieser beiden Faktoren im Hinblick auf die Entscheidungsfindung bzgl. einer möglichen adjuvanten Therapie ist daher unklar.
Mit Active Surveillance, welche regelmässige Kontrollen der Tumormarker und radiologische Untersuchungen zur Detektion eines Rezidivs/einer Metastasierung beinhaltet, lässt sich eine Rate des krankheitsspezifischen 5-Jahres-Überlebens von 99% erzielen. Eine der grössten Surveillance-Studien mit über 1300 eingeschlossenen Patienten dokumentierte eine Rezidivrate von 13% mit einer medianen Zeit bis zum Rezidiv von 14 Monaten.6 Über 60% dieser Patienten benötigten im Rezidiv dann jedoch eine Cisplatin-basierte Chemotherapie mit mindestens drei Zyklen und der damit verbundenen Toxizität. Eine weitere Voraussetzung für ein optimales onkologisches Ergebnis mit Active Surveillance ist eine gute Adhärenz bzgl. der Kontrolluntersuchungen.
Seminome sind äusserst radiosensitive Tumoren. Eine adjuvante paraaortale Radiotherapie mit 20–30Gy galt lange als Standard nach der Orchiektomie und reduziert das Rezidivrisiko auf unter 5%.7,8 Es besteht bei diesem Vorgehen jedoch das Risiko für Spättoxizität, insbesondere für die Entstehung von Sekundärmalignomen. Retrospektive Daten zeigen eine erhöhte Inzidenz von Tumoren im Strahlenfeld, wie Karzinomen von Harnblase, Pankreas, Magen, Nierenbecken und Ureteren.9 Aufgrund des exzellenten Ergebnisses mit Active Surveillance und der Tatsache, dass rund 80% der Patienten mit alleiniger Orchiektomie geheilt sind, sollte gemäss Nutzen-Risiko-Abwägung eine adjuvante Radiotherapie heute standardmässig nicht mehr zur Anwendung kommen.
Eine adjuvante Chemotherapie mit einem Zyklus Carboplatin AUC 7 ist bezüglich der Rezidivrate der adjuvanten Radiotherapie nicht unterlegen. Hierdurch kann das Rezidivrisiko auch auf etwa 5% gesenkt werden, bei zugleich günstigerem Toxizitätsprofil.10 Eine möglichst exakte Bestimmung der Nierenfunktion, idealerweise nuklearmedizinisch mit 99mTc-DTPA oder 51Cr-EDTA, ist zur korrekten Dosierung wichtig und ein Dosiscapping (beispielsweise eine auf maximal 2m2 Körperoberfläche berechnete Dosis) sollte generell vermieden werden.
Es bleibt jedoch festzuhalten, dass mit jeder Form der adjuvanten Therapie die Mehrheit der Patienten mit einem Seminom im Stadium I überbehandelt ist. Eine korrekt durchgeführte Active Surveillance kann also für die Mehrheit der Patienten als Option der Wahl angesehen werden. Dennoch ist eine adjuvante Therapie mit Carboplatin eine mögliche Alternative, die insbesondere in Betracht gezogen werden kann bei Patienten mit histologischen Risikofaktoren und wenn zusätzlich Bedenken bestehen bezüglich der Cisplatin-Fitness des Patienten im Falle eines möglichen Rezidivs (z.B. bei höherem Alter, kardiovaskulärer oder renaler Komorbidität) oder wenn eine gute Compliance mit dem Surveillance-Plan nicht gewährleistet werden kann.
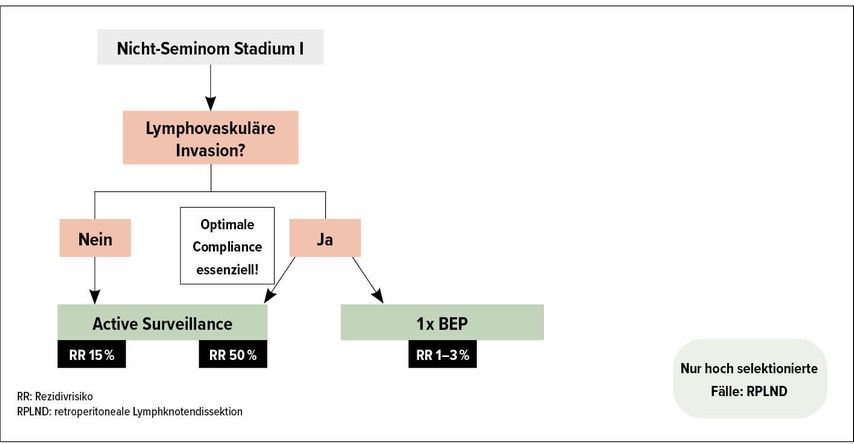
Nicht-Seminome im Stadium I
Das Rezidivrisiko für Nicht-Seminome im Stadium I ist von der lymphovaskulären Invasion (LVI) des Tumors abhängig.11,12 Bei LVI-negativen Tumoren liegt das Risiko für ein systemisches Rezidiv bei etwa 15%, mit Vorliegen einer lymphovaskulären Invasion erhöht sich dieses jedoch deutlich. In dieser Situation erleiden dann knapp 50% der Patienten ein systemisches Rezidiv.
Die bereits erwähnte grosse Surveillance-Studie6 zeigte für über 1000 Patienten mit einem Nicht-Seminom im Stadium I eine mediane Zeit von sechs Monaten bis zum Rezidiv. Für dieses mussten dann etwa 90% der Patienten mit einer Cisplatin-basierten Chemotherapie behandelt werden. Zudem beinhaltet der Surveillance-Plan für LVI-positive Patienten aufgrund des hohen Rezidivrisikos engmaschige Kontrollen mit empfohlenen Visiten alle ein bis zwei Monate im ersten Jahr. Optimale Adhärenz ist dementsprechend von äusserster Wichtigkeit.
Seit den 1990er-Jahren wurde eine adjuvante Chemotherapie mit BEP (Bleomycin, Etoposid, Cisplatin) für Patienten mit Nicht-Seminomen im Stadium I untersucht.13,14 Initial wurden zwei Zyklen verabreicht, welche das Rezidivrisiko auf etwa zwei Prozent reduzieren. Eine Studie der deutschen Testicular Cancer Study Group von 200815 mit knapp 400 Patienten randomisierte Patienten zu nur einem Zyklus adjuvant BEP im Vergleich zur retroperitonealen Lymphknotendissektion (RPLND). Die adjuvante Chemotherapie zeigte sich hier der Operation überlegen mit einer um 7,6% besseren Rate des rezidivfreien Überlebens nach 2 Jahren (99,5% für Chemotherapie und 91,9% für die RPLND).
Eine Studie der schwedisch-norwegischen Gruppe SWENOTECA hat ein risikoadaptiertes Vorgehen untersucht.16 Patienten mit lymphovaskulärer Invasion wurde eine adjuvante Chemotherapie mit ein oder zwei Zyklen BEP empfohlen, LVI-negativen Patienten wurde adjuvante Chemotherapie oder Active Surveillance als Optionen angeboten. Systemische Rezidive wurden bei LVI-negativen Patienten in 13,2% und bei LVI-positiven Patienten in 41,7% der Fälle dokumentiert. Mit einem Zyklus adjuvanter Chemotherapie wurde die Rezidivrate um 90% gesenkt, auf 1,3% bei LVI-negativen und 3,2% bei LVI-positiven Patienten. Die Minderheit der Patienten in dieser Studie erhielt einen zweiten Zyklus BEP, welcher auch keine wesentliche zusätzliche Verbesserung des bereits sehr guten Outcomes erzielte, sodass mittlerweile ein Zyklus BEP als Standard angesehen wird, wenn eine adjuvante Chemotherapie im Stadium I bei Nicht-Seminomen durchgeführt wird. Die akute Toxizität von einem Zyklus BEP ist gering, negative Einflüsse auf Fertilität und Sexualität wurden nicht dokumentiert.17,18 Daten zur Langzeittoxizität >20 Jahre nach adjuvanter Chemotherapie und möglichen kardiovaskulären Folgen liegen jedoch bislang nicht vor.
Ob nun eine adjuvante Chemotherapie beim Nicht-Seminom im Stadium I zur Anwendung kommen soll oder nicht, ist schon länger international sehr kontrovers diskutiert. Während Befürworter einer Active-Surveillance-Strategie für alle Patienten ungeachtet von Risikofaktoren insbesondere vor einer unnötigen Übertherapie warnen, betonen Unterstützer einer adjuvanten Chemotherapie, dass diese kumulativ die eingesetzte Zykluszahl Chemotherapie über alle Patienten reduziert und somit Toxizität einspart, da im Rezidivfall ja für die meisten Patienten mindestens drei Zyklen Cisplatin-basierte Therapie nötig sind.19,20
Zusammenfassend scheint beim Nicht-Seminom im Stadium I ein risikoadaptiertes Vorgehen basierend auf der lymphovaskulären Invasion sinnvoll. Für LVI-negative Patienten ist Active Surveillance eine gute Option. LVI-positive Patienten sollten über ihr hohes Rezidivrisiko aufgeklärt und die adjuvante Chemotherapie mit einem Zyklus BEP als Option thematisiert werden, um Patienten im Sinne eines «shared-decision-making» in die Entscheidungsfindung einzubeziehen. Die adjuvante retroperitoneale Lymphknotendissektion ist kein Standard und sollte routinemässig nicht zur Anwendung kommen.
Literatur:
1 Park JS et al.: Recent global trends in testicular cancer incidence and mortality. Medicine (Baltimore) 2018; 97(37): 12390 2 Chung P et al.: Evaluation of a prognostic model for risk of relapse in stage I seminoma surveillance. Cancer Med 2015; 4(1): 155-60 3 Mortensen MS et al.: A nationwide cohort study of stage I seminoma patients followed on a surveillance program. Eur Urol 2014; 66(6): 1172-8 4 Aparicio J et al.: Prognostic factors for relapse in stage I seminoma: a new nomogram derived from three consecutive, risk-adapted studies from the Spanish Germ Cell Cancer Group (SGCCG). Ann Oncol 2014; 25(11): 2173-8 5 Boormans JL et al.: Testicular tumour size and rete testis invasion as prognostic factors for the risk of relapse of clinical stage I seminoma testis patients under surveillance: a systematic review by the testicular cancer guidelines panel. Eur Urol 2018; 73(3): 394-405 6 Kollmannsberger C et al.: Patterns of relapse in patients with clinical stage I testicular cancer managed with active surveillance. J Clin Oncol 2015; 33(1): 51-7 7 Jones WG et al.: Randomized trial of 30 versus 20 Gy in the adjuvant treatment of stage I Testicular Seminoma: a report on medical research council trial TE18, european organisation for the research and treatment of cancer trial 30942 (ISRCTN18525328). J Clin Oncol 2005; 23(6): 1200-8 8 Fossa SD et al.: Optimal planning target volume for stage I testicular seminoma: a medical research council randomized trial. J Clin Oncol 1999; 17(4): 1146 9 Horwich A et al.: Second cancer risk and mortality in men treated with radiotherapy for stage I seminoma. Br J Cancer 2014; 110(1): 256-63 10 Oliver RT et al.: Radiotherapy versus single-dose carboplatin in adjuvant treatment of stage I seminoma: a randomised trial. Lancet 2005; 366(9482): 293-300 11 Blok JM et al.: Lymphovascular invasion and presence of embryonal carcinoma as risk factors for occult metastatic disease in clinical stage I nonseminomatous germ cell tumour: a systematic review and meta-analysis. BJU Int 2020; 125(3): 355-68 12 Albers P et al.: Risk factors for relapse in clinical stage I nonseminomatous testicular germ cell tumors: results of the german testicular cancer study group trial. J Clin Oncol 2003; 21(8): 1505-12 13 Cullen MH et al.: Short-course adjuvant chemotherapy in high-risk stage I nonseminomatous germ cell tumors of the testis: a medical research council report. J Clin Oncol 1996; 14(4): 1106-13 14 Chevreau C et al.: Long-term efficacy of two cycles of BEP regimen in high-risk stage I nonseminomatous testicular germ cell tumors with embryonal carcinoma and/or vascular invasion. Eur Urol 2004; 46(2): 209-15 15 Albers P et al.: Randomized phase III trial comparing retroperitoneal lymph node dissection with one course of bleomycin and etoposide plus cisplatin chemotherapy in the adjuvant treatment of clinical stage I nonseminomatous testicular germ cell tumors: AUO trial AH 01/94 by the german testicular cancer study group. J Clin Oncol 2008; 26(18): 2966-72 16 Tandstad T et al.: Risk-adapted treatment in clinical stage I nonseminomatous germ cell testicular cancer: the SWENOTECA management program. J Clin Oncol 2009; 27(13): 2122-8 17 Flechtner, HH et al.: Quality-of-life analysis of the german prospective multicentre trial of single-cycle adjuvant BEP versus retroperitoneal lymph node dissection in clinical stage I nonseminomatous germ cell tumours. Eur Urol 2016; 69(3): 518-25 18 Westermann DH et al.: Long-term followup results of 1 cycle of adjuvant bleomycin, etoposide and cisplatin chemotherapy for high risk clinical stage I nonseminomatous germ cell tumors of the testis. J Urol 2008; 179(1): 163-6 19 Kollmannsberger C et al.: Non-risk-adapted surveillance for patients with stage I nonseminomatous testicular germ-cell tumors: diminishing treatment-related morbidity while maintaining efficacy. Ann Oncol 2010; 21(6): 1296-301 20 Oldenburg J et al.: Personalizing, not patronizing: the case for patient autonomy by unbiased presentation of management options in stage I testicular cancer. Ann Oncol 2015; 26(5): 833-8
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...