Highlights zum Urothelkarzinom vom ASCO-Meeting 2021
Autorin:
OÄ Dr. Dora Niedersüß-Beke, MBA
Zentrum für Onkologie, Hämatologie und
Palliativmedizin
Wilhelminenspital, Wien
E-Mail: dora.niedersuess-beke@wienkav.at
Beim diesjährigen ASCO-Kongress wurden keine aktuell praxisrelevanten Daten, jedoch mehrere hochinteressante Studien zu blasenerhaltenden Konzepten, mit und ohne Lokaltherapie, präsentiert.
Blasenerhaltende Konzepte beim muskelinvasiven Blasenkrebs
In drei Phase-II-Studien wurden eine lokale Strahlentherapie der Blase in Kombination mit einer doppelten Immuntherapie, einer Immuntherapie in Kombination mit Chemotherapie bzw. eine Immun-Chemotherapie-Kombination, ohne Lokaltherapie, untersucht. Patienten mit einem klinischen Tumorstadium von cT2-T4 N0M0 wurden eingeschlossen.1
Pembrolizumab + Chemoradiatio
Diese Studie testete die Kombination von Pembrolizumab (4x) mit einer Chemoradiatio der Blase nach maximaler TURB. Die Chemoradiatio bestand aus zweiwöchentlich verabreichtem Gemcitabin 27mg/m2 mit einer hypofraktionierten Radiatio der Blase mit insgesamt 52Gy. Der primäre Endpunkt war das krankheitsfreieÜberleben bei intakter Blase (BIDFS). Von insgesamt 54 Patienten erhielten 48 die geplante Therapie vollständig. In der 12. Woche, nach Abschluss der Radiatio, hatten 80% eine komplette Remission erreicht. Bei einem medianen Follow-up von 15,5 Monaten lag das geschätzte 1-Jahres-BIDFS in der Gesamtkohorte bei 89%. Ungefähr ein Drittel der Patienten hatte eine Toxizität Grad≥3. Die immunassoziierte Toxizität war gering und konsistent mit den bisherigen IO-Daten.
Durvalumab + Tremelimumab + Radiatio
In der IMMUNOPRESERVE-SOGUG-Studie wurde die doppelte Immuntherapie mit konkomitanter Radiatio der Blase nach maximaler TURB untersucht.2 Die systemische Therapie bestand aus 3x 4-wöchentlicher Durvalumab- und Tremelimumab-Gabe, parallel zur Radiatio mit insgesamt 64–66Gy sowie zusätzlich 46Gy im Bereich des kleinen Beckens. Insgesamtwurden32 Patienten behandelt, von denen alle zumindest 2 Zyklen der geplanten Immuntherapie erhielten. Der primäre Endpunkt, die komplette Remissionsrate, betrug 81% (T0: 78%; T1, Tis, Ta: 3%). DieRate des krankheitsfreien1-Jahres-Überlebens wurde mit 76%, die 1-Jahres-Gesamtüberlebensrate mit 87% geschätzt. Bei einem medianen Follow-up von 12,7 Monaten lag das BIDFS bei 73%. Toxizitäten Grad ≥3 ereigneten sich bei 31%, wobei die häufigste Toxizitäten gastrointestinale Nebenwirkungen (12,5%) bzw. akutes Nierenversagen (6%) waren. Diese Studie ist insofern interessant, als ein blasenerhaltendes Konzept ganz ohne Chemotherapie untersucht wurde.
Nivolumab + Cisplatin/Gemcitabin ohne Lokaltherapie
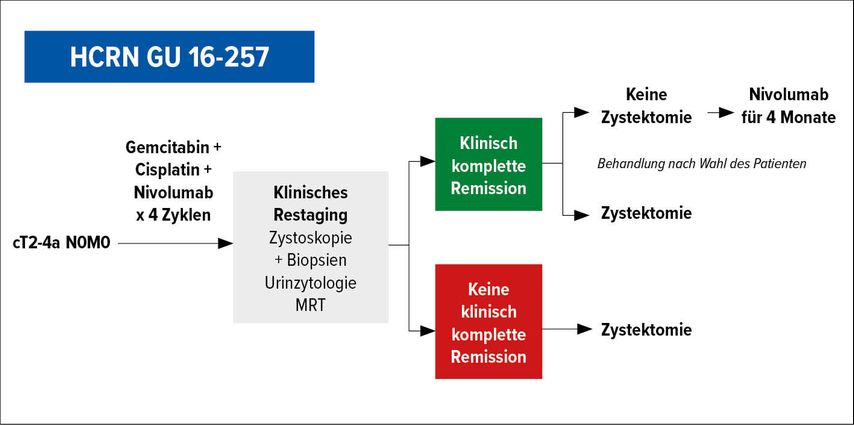
Die amerikanische HCRN GU 16-257Studieuntersuchte die Kombination von 4x Nivolumab mit Cisplatin/Gemcitabin ohne einer Lokaltherapie nach maximaler TURB (Abb.1).3 Wenn in den Re-Staging-Untersuchungen nach der multimodalen Behandlung eine klinische komplette Remission (cCR, koprimärer Endpunkt) erreicht wurde (cCR definiert als negative Blasenbiopsie pT0/pTa, unauffällige Bildgebung [MRT] sowie negative Harnzytologie), erhielten die Patientin weitere 8 Zyklen Nivolumab. Patienten ohne CR wurden zystektomiert. Von 76 Patienten wurden 64 (84%) den Staging-Untersuchungen unterzogen. 48% hatten eine komplette Remission und erhielten im Anschluss Nivolumab-Monotherapie. Die restlichen 33 Patienten erhielten eine radikale Zystektomie. Im Rahmen der Nachsorge (median 13,7 Monatebei CR-Patienten) hatten 8/31 ein Rezidiv und wurden zystektomiert. Die Studie untersuchte im weiteren Verlauf, ob Patienten mit einer DDR(„DNA damage response“)-Alteration ein besseres Outcome auf eine platinhaltige Chemotherapie zeigen. Eine signifikant höhere cCR- bzw. pT0-Rate war bei Patienten mit hohem Mutationslast (≥ 10mut/Mb) sowie bei ERCC2-Mutation evident.
Zusammenfassend zeigen diese drei Studien, dass blasenerhaltende Konzepte mit oder ohne Lokaltherapie hohe Remissionsraten erreichen können und bei gut selektierten Patienten eine radikale Zystektomie vermieden werden kann. Ob durch diese Konzepte eine Langzeitremission erreichbar ist und wie eine klinische komplette Remission verlässlich nachgewiesen werden soll bzw. welche Patienten mit welchem molekularem Profil am ehesten von diesen Konzepten profitieren, muss in größeren Phase-III-Studien mit längerem Follow-up beurteilt werden. Davor sollten diese blasenerhaltenden Konzepte nicht routinemäßig in den klinischen Alltag implementiert werden.
Metastasiertes Urothelkarzinom
Seit 2017 ist Pembrolizumab aufgrund der Phase-II-Daten der KEYNOTE-052-Studie, für „platinunfitte“ Patienten mit hoher PD-L1-Expression in Verwendung. Beim diesjährigen ASCO-Kongress wurden die Ansprech- sowie Gesamtüberlebensdaten nach bis zu 5Jahren Follow-up präsentiert.4
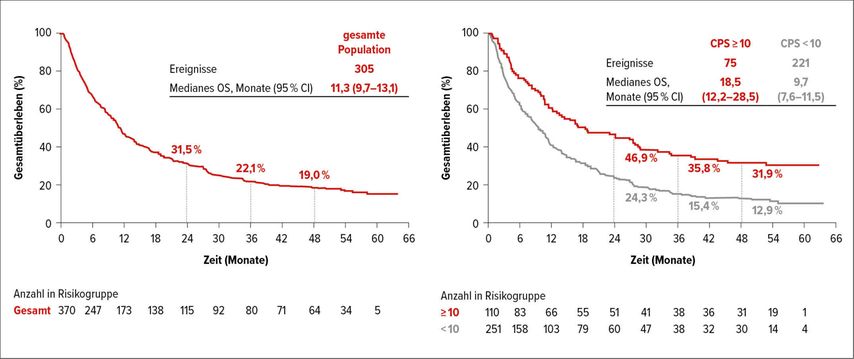
Dabei wurde die Ansprechrate mit 28,9%in der Gesamtpopulation, davon 9,5% mit kompletter Remission, bestätigt. Bei weiteren 18,1% konnte eine Krankheitsstabilisierung erreicht werden. Das Gesamtüberleben in der Gesamtpopulation lag bei 11,3 Monaten (Abb. 2A). Die mediane Dauer des Ansprechens lag bei 33,4 Monaten. 57,7% der Patienten zeigten nach über 36 Monaten ein anhaltendes Ansprechen auf Pembrolizumab.
In den prädefinierten Subgruppenanalysen zeigten Patienten mit einer hohen PD-L1-Expression (CPS ≥10) eine deutlich höhere Ansprechrate (47,3%) mit einer CR von 20,9% sowie einem deutlich verlängerten Gesamtüberleben (18,5 vs. 9,7 Monate) (Abb. 2B).
Abb. 2: Gesamtüberleben (OS) in der KEYNOTE-052-Studie: (A) Gesamtüberleben in der Gesamtpopulation, (B) Gesamtüberleben nach PD-L1-Status (CPS ≥10 versus CPS <10) (nach O’Donnel PH et al.)4
Die Daten bestätigen den Einsatz von Pembrolizumab bei hoher PD-L1 Expression in der Erstlinientherapie, sofern die Patienten für eine platinhaltige Therapie nicht fit sind. Für platinfitte Patienten ist nach wie vor eine platinhaltige Kombination, bei Ansprechen gefolgt von Avelumab der Standard.
Literatur:
1 Pembrolizumab (pembro) in combination with gemcitabine (gem) and concurrent hypofractionated radiation therapy as bladder sparing treatment for muscle-invasive urothelial cancer (MIBC) of the bladder. ASCO 2021, Abstr. #4505 2 Del Muro GY et al.: Phase II trial of durvalumab plus tremelimumab with concurrent radiotherapy in patients with localized muscle invasive bladder cancer treated with a selective bladder preservation approach. ASCO 2021, Abstr. #4505 3 Galsky MD et al.: Phase 2 trial of gemcitabine, cisplatin, plus nivolumab with selective bladder sparing in patients with muscle invasive bladder cancer. ASCO 2021, Abstr. #4503 4 O’Donnel PH et al.: First-line pembrolizumab (pembro) in cisplatin-ineligible patients with advanced urothelial cancer (UC): Response and survival results up to five years from the KEYNOTE-052 phase 2 study. ASCO 2021, Abstr. #4508
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...