Highlights vom ASCO 2021 zu den gynäkologischen Tumoren
Autoren:
PD Dr. med. Marcus Vetter1,3
Prof. Dr. med. Viola Heinzelmann-Schwarz2,3
1 Abteilung für Onkologie, Hämatologie, Immuntherapie
Medizinische Universitätsklinik
Kantonsspital Baselland
2 Klinik für Gynäkologie und Geburtshilfe
Universitätsspital Basel
3 Gynäkologisches Tumorzentrum
Universitätsspital Basel
Korrespondierender Autor:
PD Dr. med. Marcus Vetter1,3
E-Mail: marcus.vetter@ksbl.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Der virtuelle ASCO-Kongress 2021 war wieder von vielen Neuerungen auf dem Gebiet der gynäkologischen Tumoren gekennzeichnet. Es wurden über 100 Abstracts aus dem Bereich der gynäkologischen Onkologie präsentiert. Es gab wieder einige Highlights auf dem Gebiet des Ovarialkarzinoms. Hier ist sicher die ENGOT-OV15-Studie zu nennen, die eine verlängerte Bevacizumab-Gabe untersuchte. Aus dem Bereich des frühen Endometriumkarzinoms ist eine Studie zu nennen, welche das optimale Follow-up untersuchte (TOTEM-Trial). Auf dem Gebiet des Zervixkarzinoms lag der Schwerpunkt im Bereich der Immuntherapie und kombinierten Immuntherapie. Der Review-Artikel gibt Ihnen die wichtigsten Neuerungen vom Kongress mit dem Fokus auf die Systemtherapie wieder.
Keypoints
-
Beim fortgeschrittenen Ovarialkarzinom mit der Indikation für eine Bevacizumab-Therapie bleibt eine 15-monatige Therapie mit Bevacizumab der Standard.
-
In der NeoPembrOV-Studie konnte kein klarer Vorteil (OS/PFS) einer neoadjuvanten Pembrolizumab-Therapie beim fortgeschrittenen Ovarialkarzinom gezeigt werden.
-
Im VITAL-Trial wurde das Verfahren einer autologen Vakzinierung beim fortgeschrittenen Ovarialkarzinom angewendet. Ein Benefit wurde vor allem in der HRP (Homologous Recombination Proficiency) gezeigt.
-
Das ADC Mirvetuximab-Soravtansine (MIRV) in Kombination mit Bevacizumab zeigte eine hohe Ansprechrate von 60% beim vorbehandelten Ovarialkarzinom.
-
Adavosertib, ein WEE-1-Inhibitor, zeigt beim vorbehandelten Ovarialkarzinom in Kombination mit Olaparib eine hohe Krankheitskontrollrate von 89% (Phase II).
-
Beim Endometriumkarzinom konnte der TOTEM-Trial zeigen, dass ein intensiviertes Follow-up nicht mit einer besseren Prognose einhergeht.
-
Die Kombination von Vistusertib plus Anastrozol zeigte beim metastasierten Endometriumkarzinom ein hohes 8-Wochen-PFS von 67,3%. Aus verschiedenen Gründen wird die Substanz jedoch nicht weiterentwickelt.
-
Die TAPUR-Studie verdeutlicht erneut, wie wichtig eine Selektion der Biomarker wie ERBB2/3-Amplifikation/Mutation und -Überexpression zu werten ist.
-
Beim metastasierten Zervixkarzinom gab es mehrere Studien, welche neuartige Kombinationstherapien mit Immunstimulanzien z.B. durch Vakzinierung und Checkpoint-Inhibitoren untersuchten.
Neuerungen beim Ovarialkarzinom
ENGOT-OV15-Studie
Trotz deutlich verbesserter Behandlungsoptionen auf dem Gebiet der Operation und Systemtherapie hat das Ovarialkarzinom weiterhin eine schlechte Prognose mit einem 5-Jahres-Gesamtüberleben von rund 40%. Im Bereich der Systemtherapie sind die PARP-Inhibitoren und Bevacizumab mittlerweile Standard in der Erstlinie und im Rezidiv. Die genaue Sequenz ist noch nicht vollumfänglich definiert. Patientinnen mit einer HRD (Homologous Repair Deficiency) und BRCA-Mutationen haben einen deutlichen Benefit mit der Kombination von Bevacizumab und Olaparib. Die Dauer der Bevacizumab-Gabe war Gegenstand der ENGOT-OV15-Studie, welche 15 Monate (bisheriger Standard; BEV15) gegen 30 Monate untersuchte (Studienarm BEV30).1 Der primäre Endpunkt (progressionsfreies Überleben, PFS) wie auch der sekundäre Endpunkt (Gesamtüberleben, OS) waren nicht signifikant unterschiedlich (PFS BEV15 vs. BEV30 = 24,2 vs. 26,0 Monate; p=0,90, und OS BEV15 vs. BEV30 = 54,3 vs. 60 Monate; p=0,68). Damit bleibt die Dauer der Behandlung mit Bevacizumab bei 15 Monaten als Standard.
NeoPembrOV-Studie
Eine weitere Studie (NeoPembrOV-Trial) auf dem Gebiet der Systemtherapie untersuchte die neoadjuvante Therapie mit Pembrolizumab und Standard-Chemotherapie mit Carboplatin/Paclitaxel.2 Die Daten zur Immuntherapie beim Ovarialkarzinom waren bisher ernüchternd und ohne grösseren Benefit (z.B. JAVELIN-Studien, ImaGYN050, NINJA-Trial und andere). In diese Phase-II-Studie wurden 91 Patientinnen eingeschlossen und randomisiert in den Arm Chemotherapie mit Carboplatin/Paclitaxel allein oder Chemotherapie und Pembrolizumab. Nach 4 Zyklen wurde das Intervall-Debulking durchgeführt. Der primäre Endpunkt war die komplette Resektionsrate (CRR). Der primäre Endpunkt der Studie wurde erreicht mit einer CRR von 74% vs. 70%. Das PFS bei kurzem Follow-up war vergleichbar. Translationale Daten und Gesamtüberlebensdaten wurden noch nicht präsentiert und werden im Verlauf mit Spannung erwartet. Grad-3-Nebenwirkungen traten bei 75% der Patientinnen im Studienarm auf gegenüber 67% im Standardarm. Die wichtigsten Nebenwirkungen umfassten Knochenmarktoxizität und gastrointestinale Toxizität. Ob eine Immuntherapie in Zukunft als neoadjuvante Therapie gegeben wird, ist Gegenstand weiterer Untersuchungen. Das Thema Immuntherapie beim Ovarialkarzinom ist noch nicht vollumfänglich untersucht und weitere Studien und translationale Untersuchungen sind erforderlich, um eine zugeschnittene Therapie zu etablieren.
VITAL-Studie
Eine weitere interessante frühe Studie aus dem weiten Bereich der Immuntherapie war die Phase-IIB-Studie VITAL mit Gemogenovatucel-T (GEM).3 In dieser Studie wurden die Patientinnen nach Standardtherapie mit einer neuen autologen Tumorvakzine behandelt. Die Patientinnen erhielten in der Studie 1:1-randomisiert GEM vs. Placebo. Insgesamt konnten bis zu 12 Injektionen alle 4 Wochen verabreicht werden. Einschlusskriterium war ein Stadium IIIB–IV. Zudem mussten die Patientinnen nach Standardtherapie in einer kompletten Remission sein. Die Verträglichkeit war exzellent bis auf leichte Beschwerden an der Injektionsstelle. In der Gesamtkohorte konnte die Vakzinierung keinen Benefit zeigen, jedoch in der Kohorte der Patientinnen mit einer Homologous Repair Proficiency (HRP), hier konnten gegenüber Placebo ein 2-Jahres-OS von 92% vs. 55% und ein 3-Jahres-OS von 70% vs. 40% gezeigt werden. Weitere Untersuchungen inkl. Phase-III-Studien sind erforderlich. Die Gruppe der HRP bleibt hierbei die Zielkohorte. Diese Gruppe von Patientinnen hat in der Regel einen schlechten Verlauf mit kurzer Maintenance-Phase.
Mirvetuximab-Soravtansine + Bevacizumab
Eine weitere Systemtherapiestudie untersuchte die Behandlung mit einem Antikörper-Wirkstoff-Konjugat (ADC), Mirvetuximab-Soravtansine (MIRV), in Kombination mit Bevacizumab bei Patientinnen mit Rezidiv eines Ovarialkarzinoms mit bis zu drei Vorbehandlungen.4 Das ADC bindet am Folatrezeptor-alpha (FR-a), welcher bei rund 90% der Ovarialkarzinome exprimiert ist. Am ASCO 2021 wurden das Follow-up und die finalen Daten der Phase-II-Studie gezeigt.
Der primäre Endpunkt der Studie war die Ansprechrate. Insgesamt wurden 60 Patientinnen eingeschlossen. Die Ansprechrate lag in der Gesamtpopulation bei 60%. Bei Tumoren mit hoher FR-a-Expression lag die Ansprechrate bei 64%. Auch Patientinnen mit einer Platin-Resistenz und einer hohen FR-alpha-Expression hatten eine Ansprechrate von 59%. Die wichtigsten Nebenwirkungen umfassten gastrointestinale Toxizität, Augentoxizität und Fatigue. Die Autoren der Studie empfehlen eine weitere Untersuchung von MIRV und Bevacizumab in Phase-III-Studien.
Wee-1-Inhibitor Adavosertib
Eine weitere Studie aus dem Bereich der Systemtherapie untersuchte den Wee-1-Inhibitor Adavosertib bei PARP-Inhibitor-resistenter Erkrankung.5 Wee-1 ist ein kleines regulierendes Molekül, das den G2/M-Checkpoint im Zellzyklus kontrolliert. Zellen mit einer p53-Mutation oder -Verlust verlieren den G1/S-Checkpoint. Dadurch kommt es zu einem erhöhten Zellstress und einer vermehrten Abhängigkeit des Zellzyklus vom G2/M-Checkpoint. Der Wee-1-Inhibitor Adavosertib blockiert den G2/M-Checkpoint, der Zellzyklus bleibt stehen. In präklinischen Modellen konnte ein synergistischer Effekt von Olaparib und Adavosertib gezeigt werden. In der Phase-II-Studie wurde die Behandlung mit Adavosertib oder Adavosertib und Olaparib nicht komparativ untersucht. Primärer Endpunkt war die Ansprechrate. Eingeschlossen werden konnten Patientinnen mit unlimitierter Vorbehandlung, die eine Progression auf einen PARP-Inhibitor hatten. Insgesamt wurden 80 Patientinnen behandelt. Das mittlere Alter lag bei rund 60 Jahren. Nach PARP-Inhibitor-Versagen war die mittlere Anzahl an Linien 1 in beiden Gruppen (Range 0–5). In der Adavosertib-Monogruppe war das Ansprechen bei 23% und die klinische Benefitrate bei 63%. In der Kombinationsgruppe (Adavosertib und Olaparib) lag das Ansprechen bei 29% und die klinische Benefitrate bei 89%. Das mittlere PFS lag bei 5,5 Monaten Monotherapie bzw. 6,4 Monaten für die Kombination. Die wichtigsten Nebenwirkungen waren gastrointestinale Toxizität und Knochenmarktoxizität, welche für die Kombination häufiger zu verzeichnen war. Zusammenfassend konnte eine effektive Therapie unabhängig vom BRCA-Status gezeigt werden, mit managebarer Toxizität. Weitere Forschung und klinische Studien sind jedoch sicher erforderlich.
Neuerungen beim Endometriumkarzinom
TOTEM-Studie
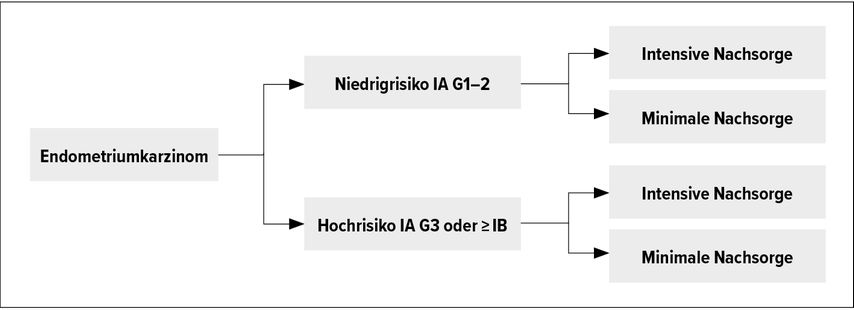
Das Endometriumkarzinom ist die häufigste gynäkologische Tumorerkrankung in der westlichen Welt. Eine interessante italienische Studie untersuchte das Follow-up (TOTEM-Trial) beim kurativ behandelten Endometriumkarzinom. Dabei wurde eine intensive mit einer minimalistischen Nachsorge verglichen.6 Das Follow-up ist weltweit nicht klar standardisiert und ein grosser Aufwand an klinischen Ressourcen wird betrieben bei recht wenig verfügbarer Evidenz. In der Studie wurde zwischen intensivierter Nachsorge und minimalistischer Nachsorge randomisiert und zwar in einer Low-Risk-Gruppe (LRG) und einer High-Risk-Gruppe (HRG) (Abb. 1). In der LRG wurde im minimalistischen Follow-up ausschliesslich klinisch nachgesorgt und in der intensivierten Nachsorge mit regelmässigen CT und PAP-Abstrich.
Abb. 1: Studiendesign des TOTEM-Trials: Es wird zwischen einer Niedrigrisikogruppe und einer Hochrisikogruppe unterschieden. In beiden Gruppen wurde randomisiert in eine intensive vs. minimalistische Nachsorge
In der HRG wurde ein rein klinisches Follow-up mit zwei CT nach 12 und 24 Monaten durchgeführt. Beim intensivierten Follow-up wurden CT bis zum 5. Jahr durchgeführt sowie Tumormarker erhoben und PAP-Abstriche und Abdomen-Ultraschall durchgeführt. Der primäre Endpunkt der Studie war das Gesamtüberleben. Insgesamt wurden 1847 Patientinnen in die Studie und Analyse eingeschlossen. Der primäre Endpunkt Gesamtüberleben war in beiden Gruppen ohne signifikanten Unterschied (HR: 1,12; p=0,424). Auch für Patientinnen mit Hochrisikotumoren gab es keinen signifikanten Unterschied für das Gesamtüberleben. Schlussfolgerung der Arbeit war, dass ein intensives Follow-up keinen Überlebensvorteil bringt. Ob neuere Techniken wie molekulares Follow-up oder moderne Schnittbildverfahren wie PET-CT oder Ganzkörper-MRI einen Vorteil bringen, bleibt zu bezweifeln, aber offen.
VICTORIA-Studie
Auf dem Gebiet der Systemtherapie des metastasierten Endometriumkarzinoms gab es zwei interessante Studien aus dem Bereich der zielgerichteten Therapie. Eine grosse Anzahl an Tumoren ist abhängig von den endokrinen Pathways und des PIK3CA/AKT/mTOR-Pathways. Die VICTORIA-Studie untersuchte die Therapie mit Vistusertib, einem mTOR1- und mTOR2-Inhibitor, in Kombination mit Anastrozol.7 In die Phase-I/II-Studie konnten Patientinnen mit maximal 1 Linie Chemotherapie und 2 Linien endokriner Therapie eingeschlossen werden. Gesamthaft wurden 73 Patientinnen in der Studie behandelt (Vistusertib plus Anastrozol n=49 und Anastrozol n=29). Das 8-Wochen-PFS lag in der Kombinationsgruppe bei 67,3% und in der Anastrozol-Gruppe bei 39,1% (Central Review). Die Gesamtansprechrate und die Dauer des Ansprechens lagen bei 24,5% und 29,6 Monate für die Kombinationsgruppe und 17,4% und 7,5 Monate für die Anastrozol-Gruppe. Die häufigsten Nebenwirkungen der Kombination waren Diarrhö, Nausea, Fatigue, Hyperglykämie, Anämie und Lymphopenie. Obgleich diese Daten sehr vielversprechend sind, wurde die weitere Entwicklung vom Hersteller aus verschiedenen Gründen gestoppt. Weitere Studien in diesem Bereich mit Kombinationen z.B. mit AKT-Inhibitoren oder CDK4/6-Inhibitoren sind in der klinischen Entwicklung.
TAPUR-Studie
Eine weitere zielgerichtete Studie beim Endometriumkarzinom wurde präsentiert. In die Studie konnten Patientinnen mit metastasiertem Endometriumkarzinom und ERBB2- oder ERBB3-Amplifikationen, -Überexpression oder -Mutation eingeschlossen werden. Die Studie lief als Registry-«TAPUR»-Studie.8 Eine HER2-Überexpression findet sich beim Endometriumkarzinom in etwas 20–30% der Fälle. Amplifikationen und Mutationen sind noch häufiger, ob sich dabei ein Ansprechen ableitet, wird kontrovers diskutiert. Im ERBB2-positiven Endometriumkarzinom hat Trastuzumab-Monotherapie eine geringe Ansprechwahrscheinlichkeit. Die «TAPUR»-Studie ist eine nicht randomisierte Basketstudie mit mehr als 18 Behandlungen und mehr als 85 genomischen «Targets». Der Therapieentscheid wird an einem virtuellen molekularen Tumorboard gefällt. Der primäre Endpunkt war die Rate der Erkrankungskontrolle (DCR). Weitere Endpunkte waren PFS, OS und Nebenwirkungen. Die Endometriumkarzinomkohorte umfasste 28 Patientinnen. Davon hatten 57% bereits mindestens 3 Vorbehandlungen. Folgende genetische Alterationen wurden gefunden:
-
ERBB2-Amplifikation: 21 (75%)
-
ERBB2-Überexpresion: 1 (4%)
-
ERBB2-Mutationen: 4 (14%)
-
ERBB3-Amplifikationen: 1 (4%)
-
ERBB2-Amplifikation und -Mutation: 1 (4%)
Die meisten Patientinnen waren in einem guten Zustand (PS 0–1: 89%; PS 2: 11%). Die Krankheitskontrollrate lag bei 37%, die Ansprechrate bei 7%. Nach 16 Wochen waren noch 10 Patientinnen mit einer stabilen oder ansprechenden Tumorerkrankung zu verzeichnen (36%).
Das mediane PFS lag bei 28,1 Wochen und das mediane OS bei 60,9 Wochen. Die Therapie war sehr gut verträglich. Als einzige Grad-3-Toxizität wurde eine Muskelschwäche bei einer Patientin festgestellt. Die Autoren konnten eine gewisse Tumoraktivität in dieser Patientinnen-Kohorte mit ERBB2/3-Alterationen aufzeigen. Weitere Studien sind jedoch notwendig, um dies zu bestätigen. Die bisherigen Daten (GOG181B- und NCT01367002-Studien) zeigten nur eine sehr geringe Aktivität mit der Trastuzumab-Monotherapie, aber eine gewisse Aktivität und einen PFS-Benefit für die Kombination von Chemotherapie plus Trastuzumab.
Neuerungen beim Zervixkarzinom
Beim Zervixkarzinom gab es beim virtuellen ASCO 2021 auch wieder einige Neuerungen.
Immuntherapie
Eine Studie befasste sich mit der Verbesserung der Immuntherapie beim metastasierten Zervixkarzinom. Durch den Einsatz von Immuncheckpoint-Inhibitoren konnte eine Ansprechrate von 10–15% erreicht werden. Mehrere Studien versuchen nun, mit Kombinationstherapien höhere und lang dauernde Remissionen zu erreichen.
Bintrafusp-alpha
Eine Phase-I/II-Studie untersuchte Bintrafusp-alpha, ein bifunktionales Fusionsprotein, welches TGF-beta und PD-L1 zielgerichtet blockiert (ein TGFb-«trap» fusioniert mit einem «human» IgG1-mAb gegen PD-L1).9 Die Patientinnen erhielten Bintrafusp alfa 0,3–30mg/kg oder 1200mg alle 2 Wochen bei metastasiertem nicht Checkpoint-Inhibitor-vorbehandeltem Zervixkarzinom. Dabei hatten 41% der 39 eingeschlossenen Patientinnen mindestens 3 Vorbehandlungen erhalten. Die Gesamtansprechrate nach RECIST 1,1 lag bei 28,2%. Die mediane Ansprechdauer lag bei 11,7 Monaten (Range: 1,4–41,2 Monate). Insgesamt hatten 5 Patientinnen eine anhaltende Remission (Dauer 1,5–41,2 Monate). Die Gesamtrate an Nebenwirkungen lag bei 84%, für Grad-3-Toxizitäten lag sie bei 20,5%: Anämie, Kolitis, Gastroparese, obere gastrointestinale Blutung, Keratoakanthom, nicht infektiöse Zystitis, Hämaturie, Pneumonitis und Rash. Die Substanz ist interessant und sollte in weiteren Studien untersucht werden, der klinische Benefit ist deutlich höher als mit einer PD-L1-Checkpoint-Inhibitor-Blockade alleine.
Simlukafusp alfa
Eine weitere Systemtherapiestudie beim Zervixkarzinom geht in eine ähnliche Richtung wie die oben genannte. Auch hier wurde eine «Immunstimulanz» kreiert, um ein besseres Ansprechen zu erreichen.10 Simlukafusp alfa ist eine genetisch hergestellte Variante des Interleukins 2, welche zielgerichtet das Fibroblasten-Protein A angreift. In der Phase-II-Basketstudie (NCT03386721) wurden 47 Patientinnen mit vorbehandeltem metastasiertem Zervixkarzinom eingeschlossen und eine Kombination aus Simlukafusp alfa und Atezolizumab wurde untersucht. Alle Patientinnen waren Checkpoint-Inhibitor-naiv. Die Ansprechrate lag bei 27% und die Krankheitskontrollrate bei 71%. Die Tumoren mit Ansprechen hatten eine längere Kontrolle über 13,3 Monate. Die häufigsten Nebenwirkungen umfassten Pyrexie, Anämie, Asthenie, AST/ALT-Erhöhung, Nausea, Vomitus und Diarrhö. Die Autoren schlossen aus der Arbeit, dass die Kombination vielversprechend ist und von den Nebenwirkungen managebar.
Therapeutische DNA-Vakzine
Eine weitere Arbeit untersuchte ebenfalls beim metastasierten Zervixkarzinom die Rolle einer DNA-Vakzinierung mit GX188E.11 Das ist eine therapeutische DNA-Vakzine, welche mit Pembrolizumab kombiniert wurde. In dieser Phase-II-Studie wurden 52 Patientinnen mit metastasiertem Zervixkarzinom eingeschlossen. Die Gesamtansprechrate lag bei 31,3%. Bei Patientinnen mit einem PD-L1-positiven Tumor war die Gesamtansprechrate bei 48%. Das mediane PFS lag bei 4,1 Monaten und das mediane OS bei 16,7 Monaten. Insgesamt sah man eine Nebenwirkungsrate von 32,7%, Grad-3–4-Nebenwirkungen waren selten – bei 3,8%. Die Kombinationstherapie könnte eine neue Behandlungsoption sein, sollte aber sicher in weiteren Studie geprüft werden.
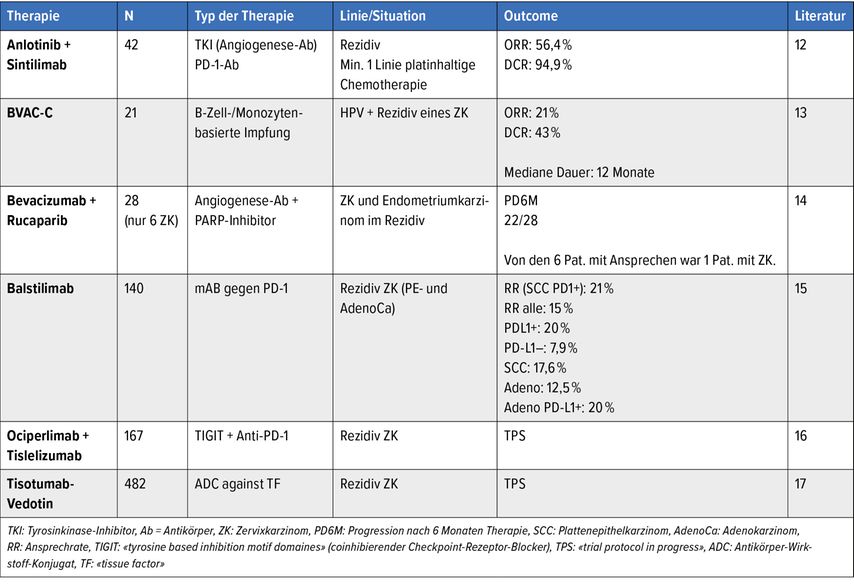
Tabelle 1 gibt einen Überblick über weitere neue frühe therapeutische Optionen beim Zervixkarzinom.
Literatur:
1 Pfisterer J et al.: Optimal treatment duration of bevacizumab (BEV) combined with carboplatin and paclitaxel in patients (pts) with primary epithelial ovarian (EOC), fallopian tube (FTC) or peritoneal cancer (PPC): a multicenter open-label randomized 2-arm phase 3 ENGOT/GCIG trial of the AGO Study Group, GINECO, and NSGO (AGO-OVAR 17/BOOST, GINECO OV118, ENGOT Ov-15, NCT01462890). J Clin Oncol 2021; 39(Suppl 15): Abstr. #5501 2 Ray-Coquard IL et al.: Efficacy and safety results from neopembrov study, a randomized phase II trial of neoadjuvant chemotherapy (CT) with or without pembrolizumab (P) followed by interval debulking surgery and standard systemic therapy ± P for advanced high-grade serous carcinoma (HGSC): a GINECO study. J Clin Oncol 2021; 39(Suppl 15): Abstr. #5500 3 Rocconi RP et al.: Maintenance vigil immunotherapy in newly diagnosed advanced ovarian cancer: efficacy assessment of homologous recombination proficient (HRP) patients in the phase IIb VITAL trial. J Clin Oncol 2021; 39(Suppl 15): Abstr. #5502 4 OʼMalley DM et al.: Mirvetuximab soravtansine, a folate receptor alpha (FRα)-targeting antibody-drug conjugate (ADC), in combination with bevacizumab in patients (pts) with platinum-agnostic ovarian cancer: final analysis. JClin Oncol 2021; 39(Suppl 15): Abstr. #5504 5 Westin SN et. al EFFORT: EFFicacy Of adavosertib in parp ResisTance: A randomized two-arm non-comparative phase II study of adavosertib with or without olaparib in women with PARP-resistant ovarian cancer. J Clin Oncol 2021; 39(Suppl 15): Abstr. #5505 6 Zola P et al.: Intensive versus minimalist follow-up in patients treated for endometrial cancer: a multicentric randomized controlled trial (the TOTEM study—NCT00916708). J Clin Oncol 2021; 39(Suppl 15): Abstr. #5506 7 Heudel PE et al.: Victoria: a multicentric, randomized, open-label, phase I/II of mTOR inhibitor (VISTUSERTIB) combined with anastrozole in patients with hormone receptor-positive advanced/metastatic endometrial cancer – a CLIPP program INCA in collaboration with GINECO group. J Clin Oncol 2021; 39(Suppl 15): 5507 8 Ali-Ahmad HM et al.: Pertuzumab plus trastuzumab (P+T) in patients (Pts) with uterine cancer (UC) with ERBB2 or ERBB3 amplification, overexpression or mutation: results from the Targeted Agent and Profiling Utilization Registry (TAPUR) study. J Clin Oncol 2021; 39(Suppl 15): 5508 9 Strauss J et al.: Evaluation of bintrafusp alfa, a bifunctional fusion protein targeting TGF-b and PD-L1, in cervical cancer: data from phase 1 and phase 2 studies. JClin Oncol 2021; 39(15_Suppl): 5509 10 Italiano A et al.: Clinical activity and safety of simlukafusp alfa, an engineered interleukin-2 variant targeted to fibroblast activation protein-a, combined with atezolizumab in patients with recurrent or metastatic cervical cancer. J Clin Oncol 2021; 39(Suppl 15): 5510 11 Park JS et al.: Efficacy and safety results of GX-188E, a therapeutic DNA vaccine, combined with pembrolizumab administration in patients with HPV 16- and/or 18- positive advanced cervical cancer: phase II interim analysis results (KEYNOTE-567). JClin Oncol 2021; 39(Suppl 15): 5511 12 Xu Q et al.: Anlotinib plus sintilimab in patients with recurrent advanced cervical cancer: a prospective, multicenter, single-arm, phase II clinical trial. J Clin Oncol 2021; 39(Suppl 15): 5524 13 Choi CH et al.: Phase IIa study of BVAC-C in HPV type 16 or 18 positive recurrent cervical carcinoma. J Clin Oncol 2021: 39(Suppl 15): 5512 14 Jackson CC et al.: A phase II trial of bevacizumab and rucaparib in recurrent carcinoma of the cervix or endometrium. JClin Oncol 2021; 39(Suppl 15): 5527 15 Joyce CE et al.: Differentiated activity profile for the PD-1 inhibitor balstilimab. J Clin Oncol 2021; 39(Suppl 15): 5529 16 Wu L et al.: AdvanTIG-202: a phase 2-study investigating anti-TIGIT monoclonal antibody ociperlimab plus anti-PD-1 monoclonal antibody tislelizumab in patients with previously treated recurrent or metastatic cervical cancer. J Clin Oncol 2021; 39(Suppl 15): TPS5595 17 Vergote I et al.: Tisotumab vedotin versus investigator’s choice chemotherapy in second- or third-line recurrent or metastatic cervical cancer (innovaTV 301/ENGOT-cx12/GOG 3057, trial in progress). JClin Oncol 2021; 39(Suppl 15): TPS 5596
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...