Fortschritte in der systemischen Therapie
Bericht:
Dr. Corina Ringsell
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Tumoren im Hals-Nasen-Ohren-Bereich stellen besondere Herausforderungen an die behandelnden Ärzt:innen. Die Therapie soll nicht nur den Krebs bekämpfen, sondern auch die Organfunktion erhalten und die Ästhetik wahren. Welche Möglichkeiten es gibt, zeigten Referent:innen verschiedener Fachbereiche der MedUni Wien/AKH Wien. Durch die Veranstaltung führten Dr. Tina Bartosik, Universitätsklinik für Hals-, Nasen- und Ohrenerkrankungen, DDr. Simone Holawe, Universitätsklinik für Mund-, Kiefer und Gesichtschirurgie, und Dr. Harald Herrmann, Universitätsklinik für Radioonkologie.
Für die kurative Behandlung stehen die Operation und die Strahlentherapie (allein oder in Kombination mit systemischer Therapie) zur Verfügung. Die Therapiewahl hängt ab von funktionellen Aspekten sowie tumor- und patient:innenspezifischen Faktoren wie kardiovaskulären, pulmonalen oder hepatischen Komorbiditäten. Daher sollten Empfehlungen immer multidisziplinär diskutiert und entschieden werden.1
Revolution in der Systemtherapie
„Zum ersten Mal seit langer Zeit können wir wirklich ein Update zur Systemtherapie geben“, leitete DDr. Ariane Steindl, Universitätsklinik für Innere Medizin I, Klinische Abteilung für Onkologie, MedUni Wien/AKH Wien, ihren Vortrag ein. Dank neuer Therapien könne man von einer Revolution der Behandlung von Kopf-Hals-Tumoren sprechen, erklärte sie. Die systemische Therapie ist indiziert bei lokal fortgeschrittenen oder metastasierten Tumoren sowie bei Rezidiven.
Lokal fortgeschrittene HNO-Tumoren
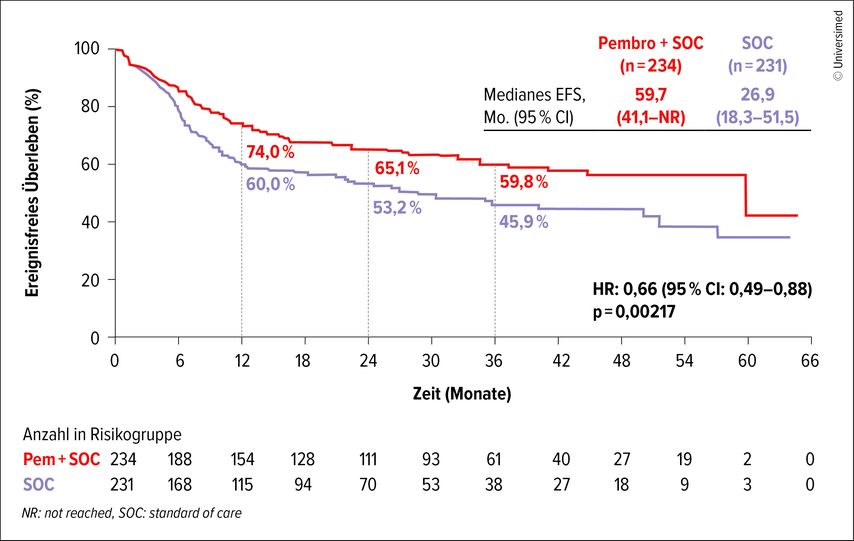
Therapieziele bei lokal fortgeschrittenen HNO-Tumoren sind vor allem Organ- und Funktionserhalt sowie möglichst langes Gesamtüberleben – und das bei möglichst geringen Nebenwirkungen. Hier wurde durch die Zugabe der Immuntherapie zur Strahlen(chemo)therapie eine deutliche Verbesserung erzielt, wie die Phase-III-Studie KEYNOTE-689 zeigt. Randomisiert wurden mehr als 700 Patient:innen mit resezierbaren HNO-Plattenepithelkarzinomen (HNSCC). Der überwiegende Teil (>90%) war HPV-negativ. Im Immuntherapiearm wurde neoadjuvant Pembrolizumab (Pembro) verabreicht, dann erfolgte die OP, gefolgt von Strahlentherapie ± Cisplatin plus insgesamt 15 Zyklen Pembro. Der Kontrollarm erhielt die Standardtherapie (OP plus adjuvante Bestrahlung ± Cisplatin). Primärer Endpunkt war das ereignisfreie Überleben (EFS) bei PD-L1-positiven Patient:innen mit einem CPS („combined positive score“) >10 (höchste PD-L1-Expression) bzw. CPS >1.2
Bei einem medianen Follow-up von 38 Monaten betrug die EFS-Rate zu Monat 36 in der CPS-10-Gruppe im Immuntherapiearm 59,8%, im Kontrollarm 45,9% (p=0,004). Das EFS war im Pembro-Arm mit knapp 60 Monaten (vs. 27 Monate) um fast drei Jahre länger als unter der Standardtherapie (Abb.1). Die CPS-1-Gruppe erreichte EFS-Raten von 58,2% bzw. 44,9% (p=0,003).2 Die Daten zum Gesamtüberleben (OS) waren noch nicht final, aber es zeigte sich ein Trend zugunsten der Immuntherapie.
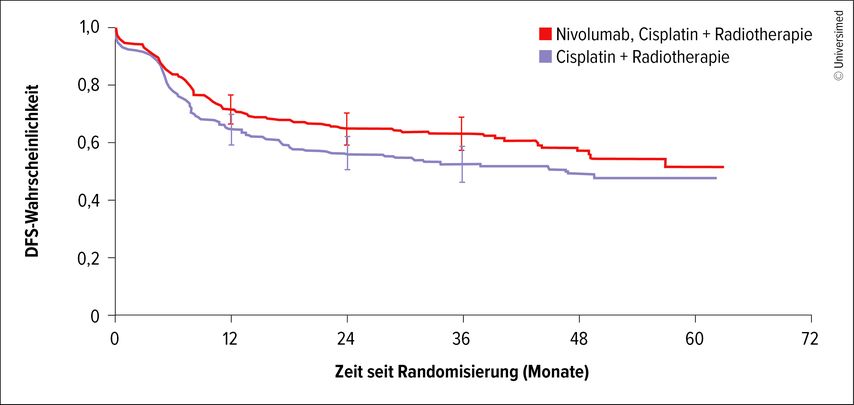
Eine weitere aktuelle Phase-III-Studie, NIVOPOST-OP, schloss 680 Hochrisikopatient:innen (u.a. R1-Resektion, Lymphknotenbefall, Kapseldurchbruch) nach Resektion eines lokal fortgeschrittenen HNSCC ein. Sie erhielten entweder die Standardtherapie mit Cisplatin plus Bestrahlung oder zunächst Nivolumab (Nivo), gefolgt von Cisplatin plus Bestrahlung und Nivo und einer Nivo-Erhaltungstherapie. Primärer Endpunkt war das krankheitsfreie Überleben (DFS). Diese Patient:innen profitierten ebenfalls von der Immuntherapie: Die 3-Jahres-DFS-Rate betrug 63,1% im Nivo-Arm versus 52,5% im Standardarm (Abb. 2). Auch hier werden die OS-Daten noch erwartet.3
Sinnvoller Einsatz der Immuntherapie im lokal fortgeschrittenen Setting
Die Frage bei allen resektablen Tumoren sei, ob eine Immuntherapie besser neoadjuvant oder adjuvant erfolgen sollte, sagte Steindl. Frage man die Patient:innen, dann würden sie sich eher für die sofortige Operation entscheiden, doch eine Immuntherapie wirke umso besser, je mehr nicht vorbehandeltes Tumorgewebe vorhanden sei, erklärte sie. Sofern eine Immuntherapie möglich ist, sollte sie daher vor der Operation eingesetzt werden.4
Ein wichtiger Aspekt ist die Auswahl der geeigneten Patient:innen, da ein Teil unter der Immuntherapie progredient ist. Deshalb wird bei einem hohen Progressrisiko zuerst operiert und die Immuntherapie im Anschluss adjuvant gegeben. „Man möchte natürlich keinem Patienten, der primär operabel ist, eine kurative Intervention vorenthalten“, sagte Steindl.
Metastasierte und rezidivierte HNO-Tumoren
In diesen Fällen stehe neben dem Gesamtüberleben vor allem die Lebensqualität der Patient:innen im Vordergrund, so Steindl. Viele Betroffene hätten eine eingeschränkte Fitness und Komorbiditäten, die die Therapieentscheidung beeinflussen, erklärte sie. Die etablierte Erstlinientherapie ist Pembro-basiert. Es wird in der Regel mit einer Chemotherapie kombiniert.6 Bei Patient:innen mit eingeschränkter Fitness, geringerer Symptomlast oder guten Markern für eine Immuntherapie kann auch eine Immunmonotherapie erwogen werden.
Tritt ein Rezidiv nach neoadjuvanter Immuntherapie auf, spielen in der Praxis klinische Faktoren und Vorbehandlungen eine Rolle für die Therapiewahl. Dazu zählen unter anderem die Fitness der Patient:innen sowie wie sie auf die erste Immuntherapie angesprochen und sie vertragen haben. Die Referentin stellte drei mögliche Verfahren einer Re-Challenge nach Ende der Immuntherapie vor: Beim „retreatment“ wird nochmals ein Medikament derselben Wirkstoffklasse gegeben. Bei der „Resensibilisierung“ wird vor der erneuten Immuntherapie eine andere Behandlung verabreicht, zum Beispiel eine Chemotherapie. Ziel ist, den Tumor wieder empfindlich zu machen. Und schließlich ist auch eine Eskalation möglich, also Immuntherapie plus eine andere Wirkstoffklasse.7
Wenn ein Rezidiv innerhalb von sechs Monaten nach Ende einer Immuntherapie auftritt, sei dies ein Zeichen, dass diese nicht wie gewünscht angesprochen habe, so Steindl: „Dann würde ich eine Immuntherapie nicht als initiale Therapielinie im Rezidiv empfehlen.“ Bei längeren rezidivfreien Intervallen könne man es dagegen noch einmal versuchen, sagte sie.
Blick in die Zukunft
Eine Wirkstoffklasse, die bereits bei anderen Entitäten eingesetzt wird, sind bispezifische Antikörper. Auch für HNO-Tumoren gibt es dazu Studien, beispielsweise eine Phase-I-Studie mit Ficerafusp alfa, einem gegen EGFR und TGF-β gerichteten Antikörper, in Kombination mit Pembro bei HPV-negativem rezidiviertem/metastasiertem HNSCC.8 Die Kombination erzielte eine objektive Ansprechrate (ORR) von 54%, wobei 21,4% der Patient:innen ein komplettes Ansprechen (CR) aufwiesen. Das mediane PFS betrug 9,9 Monate. Hauptnebenwirkungen Grad ≥3 waren Dermatitis und Anämie. In Österreich läuft derzeit an zwei Standorten (Wien, Salzburg) die Phase-II-Studie FORTIFI-HN01 mit dieser Kombination. Die Rekrutierung ist noch nicht abgeschlossen, es können noch Patient:innen aufgenommen werden.
PD-L1 – Marker für die (erfolgreiche) Immuntherapie
Wichtig für eine Entscheidung für oder gegen die Immuntherapie ist der Nachweis der PD-L1-Expression auf Tumor- und Immunzellen. Einen Einblick, wie der Nachweis erfolgt und was die angegebenen Werte aussagen, gab Dr. Bettina Trimmel, Klinisches Institut für Pathologie, MedUni Wien/AKH Wien. Für die immunhistochemische Färbung wird am Klinischen Institut für Pathologie der Antikörper BSR90 verwendet und für die Auswertung der CPS. Hier gilt ein Grenzwert von ≥1, wobei Trimmel darauf hinwies, dass Werte ≥20 eine bessere Aussagekraft haben.
Sie betonte, dass das passende Ausgangsmaterial essenziell für die Untersuchung ist. So werden mindestens 100 vitale invasive Tumorzellen für die Auswertung benötigt. Eine Herausforderung sei die Heterogenität des Materials. Einerseits sei die PD-L1-Expression innerhalb eines Tumors nicht homogen, was besonders bei sehr kleinen Biopsieproben problematisch werden könne. Hier schließe ein negativer CPS die PD-L1-Positivität nicht aus, sagte Trimmel. Andererseits unterscheide sich die PD-L1-Expression auch zwischen dem Primärtumor und einer zeitgleich auftretenden Lymphknotenmetastase.
Darüber hinaus spielen vorangegangene Therapien eine Rolle, weshalb es nicht ausreiche, PD-L1 nur bei der Erstdiagnose zu bestimmen, sondern PD-L1 auch im weiteren Verlauf bestimmt werden muss, erklärte Trimmel.
Weitere interessante Vorträge
Trotz der Fortschritte in der medikamentösen Therapie sind Operation und Bestrahlung unverzichtbar für die Behandlung von HNO-Tumoren. Beeindruckend war daher der mit vielen Bildern illustrierte Vortrag „Rekonstruktion nach Tumorresektion – Möglichkeiten und Herausforderungen“ von DDr. Simone Holawe, Universitätsklinik für Mund-, Kiefer und Gesichtschirurgie.
In vielen Fällen genügt aber auch ein minimalivasiver Eingriff. Wie OP-Roboter dabei eingesetzt werden können, zeigte Dr. Tina Bartosik, Universitätsklinik für Hals-, Nasen- und Ohrenerkrankungen, in ihrem Vortrag „Transorale robotische Chirurgie – Entwicklungen und Limitationen“.
Dr. Harald Herrmann, Universitätsklinik für Radioonkologie, erläuterte in „Schlucken im Fokus – pharynxsparende Strahlentherapie im Kopf-Hals-Bereich“, wie moderne computergestützte Systeme eine effektive und die Funktion erhaltende Bestrahlung ermöglichen.
Ein besonderes Thema hatte DDr. Dino Tur, MClinDent (Periodontology), Universitätszahnklinik Wien, Fachbereich Parodontologie, gewählt: „Parodontitis – ein Risikofaktor für Krebs?“ Zwar konnte eine Assoziation der Parodontitis mit verschiedenen Krebsentitäten, vor allem im Kopf-Hals-Bereich, beschrieben werden. Allerdings gibt es bislang keine ausreichende Evidenz für einen kausalen Zusammenhang.
Literatur:
1 S3-Leitlinie Diagnostik, Therapie, Prävention und Nachsorge des Oro- und Hypopharynxkarzinoms. März 2024. www.leitlinienprogramm-onkologie.de/leitlinien/oro-und-hypopharynxkarzinom ; zuletzt aufgerufen am 31.3.2026 2 Uppaluri R et al.: N Engl J Med 2025; 393(1): 37-50 3 Bourhis J et al.: Lancet 2026; 407 (10526): 363-74 4 Awada G et al.: Nat Cancer 2025; 6(6): 967-87 5 Li J et al.: Int Immunopharmacol 2024; 134: 112200 6 Tahara M et al.: ESMO-Kongress 2022, Abstr. #659MO 7 Tang LB et al.: Nat Rev Clin Oncol 2025; 22(8): 546-65 8 Chung CH et al.: J Clin Oncol 2025; 43(16_suppl): 6017
Informationen zur FORTIFI-Studie unter: https://clinicaltrials.gov/study/NCT06788990
Studienleiter an der MedUni Wien ist Assoc. Prof. Dr. Thorsten Füreder, der auch selbst Patient:innen rekrutiert: thorsten.fuereder@meduniwien.ac.at
Studienleiter am Universitätsklinikum Salzburg ist Univ.-Prof. Dr. Thomas Melchardt: t.melchardt@salk.at
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...