Forschung identifiziert potenzielle neue therapeutische Ansatzpunkte beim SCLC
Bericht:
Dr. Therese Schwender
Die aktuelle Standard-Erstlinientherapie beim kleinzelligen Lungenkarzinom setzt sich aus Carboplatin/Etoposid und einem Anti-PD-1-/PD-L1-Antikörper zusammen. Optionen für die zweite Linie sind allerdings weiterhin begrenzt und liefern unbefriedigende Resultate. Forschungsarbeiten zu neuen therapeutischen Ansatzpunkten konzentrieren sich nun unter anderem auf den Zelloberflächenmarker Delta-like Ligand 3 (DLL-3).
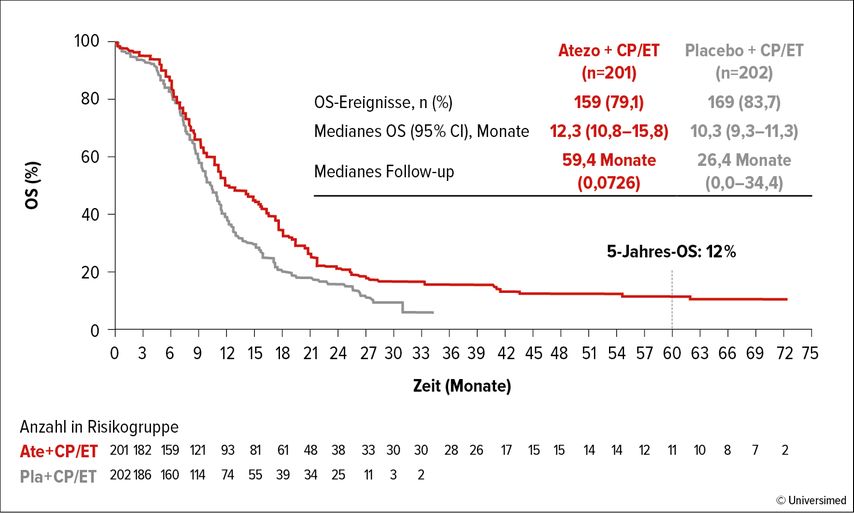
Kaushal Parikh, MD, Mayo Clinic, Rochester (USA), sprach im ersten Teil seines Vortrags am International Lung Cancer Summit über die Datenlage zur Erstlinientherapie des kleinzelligen Lungenkarzinoms (SCLC) und startete mit der 2018 publizierten Studie IMpower133, die Carboplatin/Etoposid plus Atezolizumab untersucht hatte.1,2«Nach mehr als 30 Jahren war dies die erste Landmark-Studie, die für Patient:innen mit einem kleinzelligen Lungenkarzinom einen Überlebensvorteil gezeigt hat», betonte er. Seither erwiesen sich verschiedene Chemo-Immuntherapiekombinationen als erfolgreich. Die neusten Daten zu IMpower133 und ihrer Verlängerungsstudie IMbrella A ergaben eine 5-Jahres-Gesamtüberlebensrate von 12% (Abb. 1).3«Das mag sich nach wenig anhören, jedoch liegt der historische Wert für Platin/Etoposid bei 2 bis 4%», gab er zu bedenken. Beeindruckend sei zudem, dass das Kurvenende flach auszulaufen scheint. «Die Frage ist nun, was diejenigen Patient:innen, die langfristig von der Chemoimmuntherapie profitieren, charakterisiert und wie wir sie identifizieren können.»
Abb. 1: Carboplatin/Etoposid plus Atezolizumab erreichte in der Erstlinientherapie des kleinzelligen Lungenkarzinoms eine 5-Jahres-Gesamtüberlebensrate von 12% und damit eine deutliche Verbesserung im Vergleich zu bisher vorliegenden Resultaten. Modifiziert nach Liu SV et al.3
Zweite Therapielinie: viel Raum für Verbesserungen
Die verfügbaren Möglichkeiten zur Zweitlinientherapie des SCLC sind nach wie vor begrenzt. «Hat das chemotherapiefreie Intervall bis zu einem Rezidiv mindestens 3 Monate betragen, ist ein ‹Re-Challenge› mit der Erstlinientherapie eine Option. In den anderen Fälle wird Topotecan eingesetzt», so Parikh. Von verschiedenen weiteren Optionen, darunter z.B. Paclitaxel, Irinotecan und Temozolomid, habe bisher keine einen Überlebensvorteil gegenüber Topotecan zeigen können. Da in den USA Lurbinectedin die einzige Option darstellt, die seit vielen Jahren zur Zweitlinientherapie des SCLC zugelassen wurde (in der Schweiz befristet zugelassen), ging Parikh anschliessend kurz auf diese Substanz ein. Lurbinectedin ist ein Analogon von Trabectedin, dem halbsynthetischen Wirkstoff, der ursprünglich aus dem marinen Manteltier Ecteinascidia turbinata isoliert wurde.4 Die Substanz führte in einer einarmigen Phase-II-Studie zu einer Gesamtansprechrate von 35,2% (platinsensitiv 45%, platinresistent 22,2%) und einem progressionsfreien Überleben von 3,5 Monaten (chemotherapiefreies Intervall [CTFI] <90 Tage: 2,6 Monate; CTFI>90 Tage: 4,6 Monate).5 Das Gesamtüberleben lag bei 9,3 Monaten (CTFI <90 Tage: 5,0Monate; CTFI>90 Tage: 11,9 Monate). «Zu den Vorteilen von Lurbinectedin gehört, dass es nur alle 3 Wochen gegeben werden muss und dass seine Verträglichkeit gut ist», erläuterte der Referent. Eine Phase-III-Studie zur Kombination von Lurbinectedin mit Doxorubicin zeigte im Vergleich zu einer Kontrollgruppe, die eine vom Arzt/von einer Ärztin frei wählbare Zweitlinientherapie erhielt, allerdings keinen Überlebensvorteil.6
DLL-3 als neuer Ansatzpunkt
«Der aktuell vielversprechendste neue therapeutische Ansatzpunkt stellt der Zelloberflächenmarker DLL3 – Delta-like Ligand 3 – dar, der in bis zu 80% der SCLC überexprimiert wird», führte Dr. Parikh weiter aus. In gesundem Gewebe wird DLL3 nicht exprimiert. Zwei Studien (TAHOE und MERU), in denen ein gegen DLL3 gerichtetes Antikörper-Wirkstoff-Konjugat (Rovalpituzumab-Tesirine, Rova-T) eingesetzt worden war, waren allerdings negativ.7,8 TAHOE schloss 442 Patient:innen mit einem DLL3-hoch-positiven metastasierten SCLC ein und verglich die Zweitlinientherapie mit Rova-T mit Topotecan. Das mediane Überleben betrug 6,3 Monate im Rova-T-Arm und 8,6 Monate im Topotecan-Arm. Die HR betrug 1,46. Daraufhin wurde die Studie vorzeitig beendet. In MERU wurden 748 Patient:innen nach Abschluss einer Chemotherapie und fehlender Progression auf eine Rova-T-Erhaltungstherapie oder Placebo randomisiert. Mit einer HR von 1,07 (medianes Gesamtüberleben: 8,5 Monate vs. 9,8 Monate) wurde auch hier der primäre Endpunkt nicht erreicht. Die Substanz war zudem mit einer höheren Rate an therapiebedingten Nebenwirkungen wie Pleuraergüssen, peripheren Ödemen und Photosensitivitätsreaktionen verbunden.
Mit AMG-757 (Tarlatamab) befindet sich auch ein bispezifischer Antikörper (BiTE) in klinischer Prüfung, der zum einen an DLL-3 auf der Oberfläche der Tumorzellen und zum anderen an CD3 auf zytotoxischen T-Zellen bindet. In der Phase-II-Studie DeLLphi-301 wurden die Antitumor-Aktivität und die Sicherheit von Tarlatamab in zwei verschiedenen Dosierungen (10mg bzw. 100mg alle 2 Wochen i.v.) bei Patient:innen mit vorbehandeltem SCLC im fortgeschrittenen Stadium untersucht.9 Der primäre Endpunkt war das objektive Ansprechen. Insgesamt wurden 220 Personen mit SCLC behandelt, die zuvor im Median zwei Therapielinien erhalten hatten. Bei einer medianen Nachbeobachtungszeit von 10,6 Monaten in der 10-mg-Gruppe und 10,3 Monaten in der 100-mg-Gruppe konnte ein objektives Ansprechen bei 40% (97,5% CI: 29–52) der Teilnehmenden in der 10-mg-Gruppe und bei 32% (97,5% CI: 21–44) der Teilnehmenden in der 100-mg-Gruppe beobachtet werden. «Wichtig zu betonen ist hier, dass die mediane Ansprechdauer bei 59% der Patient:innen mit objektivem Ansprechen bei mindestens sechs Monaten lag», so der Redner. Zu den häufigsten Nebenwirkungen einer Behandlung mit Tarlatamab gehörten das Zytokinfreisetzungssyndrom (CRS), Appetitlosigkeit und Pyrexie. Ein CRS trat dabei hauptsächlich im ersten Behandlungszyklus auf und wies meist den Schweregrad 1 oder 2 auf. «Insgesamt sind die Resultate dieser Studie als sehr ermutigend zu beurteilen», fand Parikh abschliessend.
Quelle:
5th International Lung Cancer Summit, 10. November 2023, Lausanne und online
Literatur:
1 Horn L et al.: N Engl J Med 2018; 379: 2220-9 2 Liu SV et al.: J Clin Oncol. 2021; 39: 619-30 3 Liu SV et al.: WCLC 2023; Abstr. #OA01.04 4 Romano M et al.: Int J Cancer 2013; 133: 2024-33 5 Trigo J et al.: Lancet Oncol 2020; 21: 645-54 6 Aix SP et al.: Lancet Respir Med 2023; 11: 74-86 7 Blackhall F et al.: J Thorac Oncol 2021; 16: 1547-58 8 Johnson ML et al.: J Thorac Oncol 2021; 16: 1570-81 9 Ahn MJ et al.: N Engl J Med. 2023; online ahead of print
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...