Differenzierter Substanzeinsatz in einzelnen Gruppen
Bericht:
Dr. med. Judith Moser
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Behandlung von fortgeschrittenen Primärtumoren im Bereich der Leber und des Pankreas ist noch immer herausfordernd. In einem Vortrag fasste PD Dr. med. Sara De Dosso, Bellinzona, aktuelle Studienergebnisse zur Immuntherapie des hepatozellulären Karzinoms sowie zur Identifikation optimaler Behandlungsschemata in bestimmten Subgruppen mit Pankreaskarzinom zusammen, die am ASCO-Kongress 2024 präsentiert wurden.
Beim inoperablen hepatozellulären Karzinom (HCC) bestehe ein Bedarf an neuen Therapien mit lang anhaltender Wirkung, wie De Dosso erklärte. Die globale, randomisierte Phase-III-Studie CheckMate 9DW prüfte daher Nivolumab plus Ipilimumab bis zu vier Zyklen gefolgt von Nivolumab alle vier Wochen bei Patient:innen, die mindestens eine messbare Läsion ohne Pfortaderinvasion aufwiesen. Der Vergleich erfolgte mit Lenvatinib oder Sorafenib je nach Entscheidung der Prüfärzt:innen.
Erste Ergebnisse der CheckMate-9DW-Studie
Das als primärer Endpunkt definierte Gesamtüberleben (OS) fiel unter der Checkpoint-Inhibitor-Kombination tatsächlich signifikant länger aus als mit den zielgerichteten Substanzen (23,7 vs. 20,6 Monate; HR: 0,79; p=0,018).1
Im ersten Behandlungsjahr schnitt der Kontrollarm jedoch besser ab als der experimentelle Arm. Nach etwa zwölf Monaten kreuzten sich die Kurven schliesslich und zeigten danach eine zunehmende Auftrennung zugunsten der Immuntherapie. Die Gesamtansprechrate war unter Nivolumab/Ipilimumab vergleichsweise höher (36% vs. 13%; p<0,0001), während sich für das progressionsfreie Überleben (PFS) kein Unterschied ergab (9,1 vs. 9,2 Monate; HR: 0,87).
Das anfänglich schlechtere Abschneiden im experimentellen Arm könnte laut De Dosso auf die gesteigerte Toxizität der Therapie zurückzuführen sein. Behandlungsbedingte Nebenwirkungen (TRAE) aller Grade, die zum Therapieabbruch führten, traten im Prüfarm häufiger auf (18% vs. 10%), ebenso wie behandlungsbedingte Todesfälle (4% vs. <1%). Die Onkologin betonte, dass dieser Aspekt daher Berücksichtigung finden sollte, wenn Nivolumab/Ipilimumab als alternative Option in Betracht gezogen werde. 28% der mit der Kombination behandelten Patient:innen entwickelten immunmediierte AE der Grade 3/4 und 29% erhielten hochdosierte Steroide. Im Vergleich dazu war in der HIMALAYA-Studie, die Durvalumab plus Tremelimumab testete, der Prozentsatz an toxischen Todesfällen niedriger, was auch auf TRAE der Grade 3/4 und mit hohen Steroiddosen behandelte Patient:innen zutraf.2
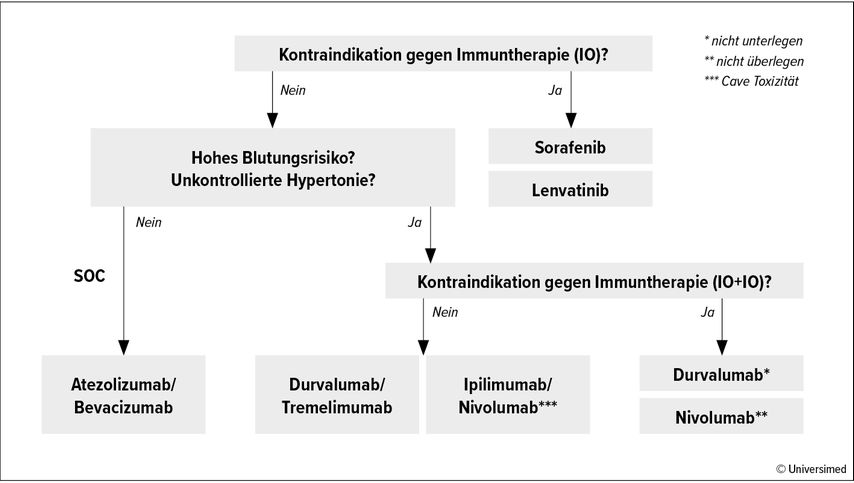
De Dosso betonte, dass auf der Grundlage der verfügbaren Studiendaten in der Erstlinienbehandlung des fortgeschrittenen HCC neben der zielgerichteten Therapie verschiedene Checkpoint-Inhibitor-Schemata einschliesslich Nivolumab/Ipilimumab verordnet werden können (Abb. 1).1–4 Die wichtigsten Entscheidungskriterien umfassen das Vorliegen von Kontraindikationen, hohes Blutungsrisiko und unkontrollierte Hypertonie.
Abb. 1: Wesentliche Entscheidungskriterien in der Erstlinientherapie des fortgeschrittenen hepatozellulären Karzinoms1–4
Ältere Patient:innen mit Pankreaskarzinom
Im Setting des metastasierten Pankreaskarzinoms zeichnet sich die GIANT-Studie durch den Einschluss einer älteren Population (≥70 Jahre) aus. Diese Gruppe ist in Studien normalerweise unterrepräsentiert, während sie in der klinischen Praxis den Grossteil der Patient:innen ausmacht.
Vor der Rekrutierung erfolgte ein Screening anhand eines geriatrischen Assessments; nur die vulnerable Gruppe ging in die Studie ein, während die fitten und gebrechlichen Personen ausgeschlossen wurden. Nach einem vollständigen geriatrischen Assessment inklusive Einschätzung der Lebensqualität wurden die Studienteilnehmer:innen randomisiert und erhielten entweder dosisreduziertes 5-FU plus liposomales Irinotecan oder modifiziertes Gemcitabin plus Nab-Paclitaxel.
In Bezug auf das OS resultierte kein wesentlicher Unterschied zwischen den beiden Schemata (4,4 vs. 4,7 Monate; HR: 1,12; p=0,72), wenngleich die Ergebnisse die schlechte Prognose dieser Patient:innengruppe unterstreichen.5 Der Grund für das kurze Überleben von <5 Monaten könnte laut De Dosso das frühe Absetzen der Therapie in vielen Fällen sein. Patient:innen, die ≥4 Wochen behandelt wurden, erreichten ein medianes OS von acht Monaten, was den Ergebnissen entspricht, die sich mit der Erstlinientherapie bei jüngeren Personen erzielen lassen.
Sowohl der Performance-Status (PS) als auch das körperliche/funktionelle Wohlbefinden erwiesen sich als starke Prädiktoren für das OS. So zeigten Patient:innen mit einem ECOG PS von 0 ein medianes OS von 6,9 Monaten, während dies bei einem PS von 2 nur 1,4 Monate betrug (p<0,001).
Eine wichtige Botschaft der GIANT-Studie bestehe darin, so De Dosso, dass die rechtzeitige Identifikation der Bedürfnisse der Patient:innen sowie die Verabreichung einer aggressiven supportiven Therapie einschliesslich Rehabilitation noch vor dem Start der Krebsbehandlung wichtiger sein könnten als der frühe Beginn der Chemotherapie.
PASS-01: multiomisches Profiling «upfront»
Die randomisierte Phase-II-Studie PASS-01 wurde initiiert, um einerseits Biomarker für das Ansprechen des unbehandelten metastasierten Pankreaskarzinoms auf Erstlinien-Standardchemotherapien zu evaluieren. Andererseits sollten Grundlagen für verbesserte Entscheidungen in Bezug auf die Wahl der Präzisionstherapie in späteren Linien geliefert werden. PASS-01 untersuchte diese Fragestellung als erste Studie prospektiv. Patient:innen ohne BRCA/PALB2-Mutationen erhielten randomisiert entweder modifiziertes FOLFIRINOX (n=75) oder Gemcitabin plus Nab-Paclitaxel (n=75). Zu Studienbeginn erfolgten Tumorbiopsien zwecks Whole-Genome- und Transkriptionssequenzierung, Pharmakotypisierung und weiteren Untersuchungen.
Hinsichtlich des PFS fand sich ein Trend zugunsten von Gemcitabin/Nab-Paclitaxel (5,5 vs. 4,0 Monate; p=0,0836), während das OS signifikant verbessert wurde (9,7 vs. 8,4 Monate; p=0,0138).6 Ein Viertel der Population war zum Zeitpunkt des ersten CT-Scans bereits progredient. Dies unterstreiche die aggressive Biologie der Erkrankung, sagte die Onkologin. Insgesamt handelte es sich um eine Patient:innengruppe mit schlechter Prognose; dies sei auf den Ausschluss BRCA-mutierter Personen, das Fehlen einer vorangegangenen Resektion des Primums und andere Faktoren zurückzuführen, erläuterte sie.
Wie vorläufige Einblicke in die korrelativen Analysen nahelegten, könnten die molekularen Subtypen gemäss der Moffitt-Klassifikation als prognostische und prädiktive Biomarker dienen, so De Dosso. Das mediane PFS war beim klassischen transkriptionellen Subtyp länger als beim «basal-like» transkriptionellen Subtyp (5,7 vs. 2,7 Monate; p=0,0316).
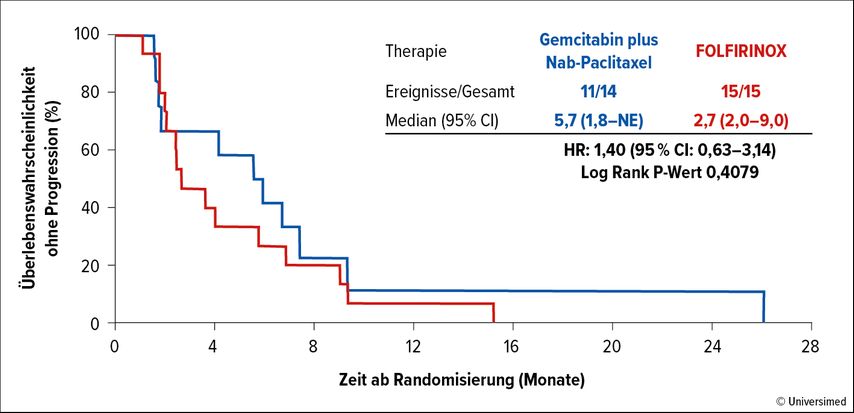
Auch implizierten die Ergebnisse laut De Dosso ein unterschiedliches Ansprechen auf die Chemotherapie: Gemcitabin/Nab-Paclitaxel schnitt in der «basal-like» Subgruppe besser ab als FOLFIRINOX (5,7 vs. 2,7 Monate; Abb. 2), während beim klassischen Subtyp kein Unterschied auffiel. Demzufolge müsse man bestimmten Patient:innen keine aggressive Chemotherapie anbieten, da sie vermutlich besser auf eine Gemcitabin-basierte Behandlung ansprechen.
Abb. 2: Ansprechen auf Gemcitabin/Nab-Paclitaxel und FOLFIRINOX beim Pankreaskarzinom vom «basal like» transkriptionellen Subtyp (modifiziert nach Knox JJ et al.)6
Allerdings sei die Patient:innenzahl in dieser Studie klein, und weitere Untersuchungen sollten folgen. Dennoch beobachte man auch beim Pankreaskarzinom faszinierende Fortschritte im Hinblick auf molekulare Subtypen und prädiktive Faktoren, erklärte De Dosso. Sie gehe davon aus, dass in den kommenden Jahren klinische Studien gestartet werden, die unterschiedliche molekulare Subgruppen einschliessen.
Literatur:
1 Galle PR et al.: Nivolumab plus ipilimumab vs lenvatinib or sorafenib as first-line treatment for unresectable hepatocellular carcinoma: first results from CheckMate 9DW. JClin Oncol 2024; 42(Suppl. 17): Abstr. #LBA4008 2 Abou-Alfa GK et al.: Tremelimumab plus durvalumab in unresectable hepatocellular carcinoma. N Engl J Med Evid 2022; 1(8): EVIDoa2100070 3 Finn RS et al.: Atezolizumab plus bevacizumab in unresectable hepatocellular carcinoma. NEngl J Med 2020; 382(20): 1894-905 4 Yau T et al.: Nivolumab versus sorafenib in advanced hepatocellular carcinoma (CheckMate 459): a randomised, multicentre, open-label, phase 3 trial. Lancet Oncol 2022; 23(1): 77-90 5 Dotan E et al.: A randomized phase II study of gemcitabine and nab-paclitaxel compared with 5-fluorouracil, leucovorin, and liposomal irinotecan in older patients with treatment-naïve metastatic pancreatic cancer (GIANT) ECOG-ACRIN EA2186. J Clin Oncol 2024; 42(Suppl. 16): Abstr. #4003 6 Knox JJ et al.: Early results of the PASS-01 trial: pancreatic adenocarcinoma signature stratification for treatment-01. J Clin Oncol 2024; 42(Suppl. 17): Abstr. #LBA4004
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...