ASCO-Highlights zum Nierenzellkarzinom
Autorin:
Univ.-Prof. Dr. Manuela Schmidinger
Universitätsklinik für Urologie
Medizinische Universität Wien
Seit Einführung der Immuncheckpoint-Inhibitoren (ICI) zur Therapie des metastasierten Nierenzellkarzinoms (mRCC) hat sich die Behandlungsstrategie erheblich verändert und vor allem dramatisch verbessert. Am Jahreskongress der American Society of Clinical Oncology (ASCO) 2021 wurden zahlreiche weitere Analysen zu diesen modernen Therapien vorgestellt; auch der Aspekt der zytoreduktiven Nephrektomie im Zeitalter der ICI-Therapie wurde neu beleuchtet. Das größte Highlight war aber sicher die Vorstellung der Ergebnisse der ersten adjuvanten ICI-Studie beim RCC. Schließlich könnten neue Daten zur Gabe eines Probiotikums bei Patienten unter Immuntherapie unseren klinischen Alltag erheblich beeinflussen.
Keypoints
-
Pembrolizumab ist die erste adjuvante Immuntherapie, die eine Verbesserung der DFS-Rate aufzeigen konnte.
-
Die Zulassung von Pembrolizumab wird aufgrund der guten Ergebnisse und des günstigen Toxizitätsprofils erwartet.
-
Die Debatte zur zytoreduktiven Nephrektomie geht weiter: In der Ära der kombinierten Immun-TKI-Therapie scheint ein Überlebensvorteil zugunsten nephrektomierter Patienten erkennbar.
-
Die Effektivität der neuesten ICI-TKI-Kombinationen wird auch nach längerem Follow- up und in einzelnen Subgruppen bestätigt.
-
Nivolumab + Cabozantinib scheint bei nicht klarzelligem RCC aktiv zu sein: Ausnahme ist das chromophobe RCC.
-
Cabozantinib zeigt Wirkung bei Ductus-Bellini-Karzinomen.
-
Probiotika verbessern Ansprechen bei Patienten unter Nivolumab + Ipilimumab.
Adjuvante Therapie des Nierenzellkarzinoms
Beim lokalisierten Nierenzellkarzinom (RCC) ist die chirurgische Entfernung des Tumors der einzige kurative Therapieansatz. Die Prognose ist zu diesem Zeitpunkt von makroskopischen und mikroskopischen Eigenschaften des Tumors abhängig. Patienten mit höherem T-Stadium, schlechter Tumordifferenzierung, positiven regionalen Lymphknoten, sarkomatoiden oder nekrotischen Tumoren haben eine sehr hohe Wahrscheinlichkeit, zu metastasieren.1 Adjuvante Studien mit Tyrosinkinase-Inhibitoren (TKI; z.B. Sunitinib, Pazopanib, Sorafenib und Axitinib) oder dem mTOR-Inhibitor Everolimus waren eher entäuschend. Lediglich eine adjuvante Sunitinib-Studie (STRAC) zeigte für Patienten im Sunitinib-Arm eine Verbesserung der Rate des krankheitsfreien Überlebens (DFS) nach 3 und nach 5 Jahren im Vergleich zu Placebo (3-Jahres-DFS-Rate 64,9% versus 59,5%; 5-Jahres-DFS-Rate 59,3% versus 51,3%, p=0,030; HR: 0,761; 95% CI: 0,594–0,975). Eine Verbesserung der Rate des Gesamtüberlebens (OS) konnte jedoch nicht gezeigt werden und die Toxizitäten Grad 3–4 waren mit 60,45% sehr hoch.2 Eine gepoolte Analyse aus drei adjuvanten TKI-Studien (mit Sunitinib, Sorafenib und Pazopanib) kam zu dem Schluss, dass eine adjuvante TKI-Therapie keinen Benefit in Bezug auf das DFS oder Gesamtüberleben bringt, die Therapie jedoch mit substanzieller Toxizität assoziiert ist.3
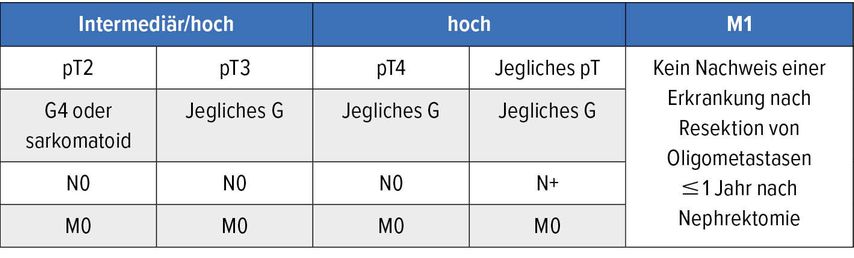
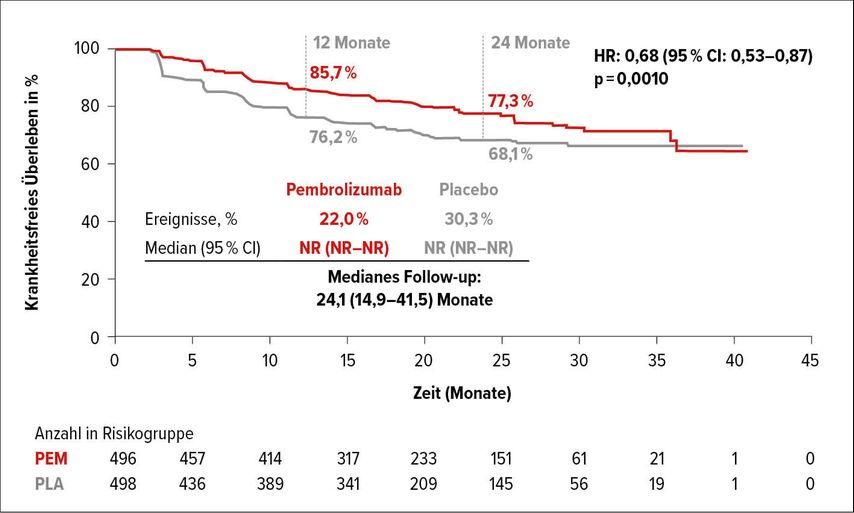
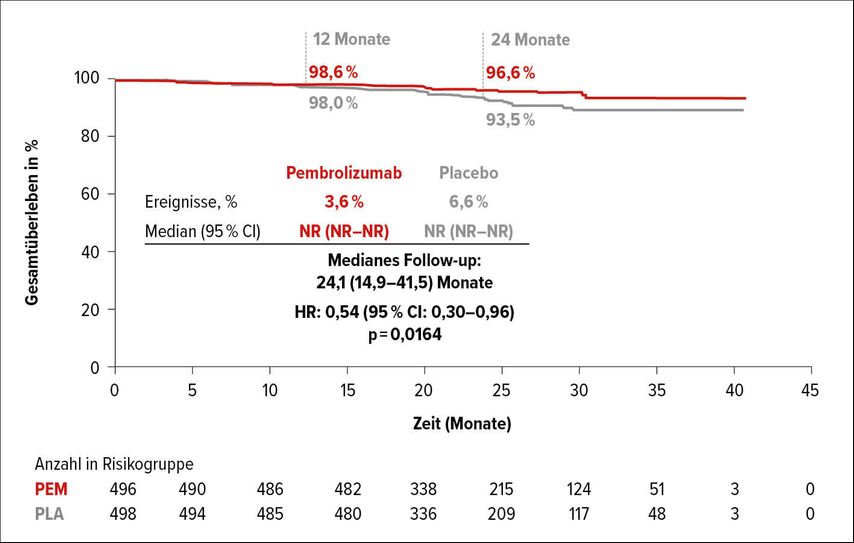
Nach dem durchschlagenden Erfolg von ICI im metastasierten Stadium wurden zahlreiche randomisierte Studien initiiert, um den möglichen Benefit einer ICI-Therapie im adjuvanten Setting zu überprüfen. Die Ergebnisse der ersten adjuvanten ICI-Studie wurden am ASCO-Kongress 2021 vorgestellt. Die Keynote-564-Studie war eine randomisierte, placebokontrollierte, doppelblinde Phase-III-Studie mit dem PD-1-Inhibitor Pembrolizumab.4 Tabelle 1 stellt die Risikogruppen dar, die in diese Studie eingeschlossen wurden. Wie daraus zu erkennen ist, wurden auch Patienten mit resezierten Oligometastasen eingeschlossen (5,8% in beiden Armen); die meisten Patienten hatten einen positiven PD-L1-Status, definiert als „combined positive score“ (CPS) >1 (73,6% im Pembrolizumab-Arm und 76,9% im Placeboarm). Pembrolizumab (200mg alle 3 Wochen) bzw. Placebo wurden innerhalb von 12 Wochen nach Nephrektomie eingeleitet und für die Dauer von etwa einem Jahr gegeben. Der primäre Endpunkt der Studie war das DFS (erfasst durch den Untersucher). OS und Sicherheit waren sekundäre Endpunkte. Nach einer medianen Nachbeobachtungszeit von 24,1 Monaten (14,9–41,5) war die DFS-Rate statistisch signifikant besser im Pembrolizumab-Arm (Abb.1) (HR: 0,68; 95% CI: 0,53–0,87, p=0,0010). Der Benefit war erwartungsgemäß am stärksten in der M1-Risikogruppe gegeben (HR: 0,29; 95% CI: 0,12–0,69), aber prinzipiell auch in den anderen Risikogruppen vorhanden. Das mediane OS ist zum jetzigen Zeitpunkt noch nicht erreicht, auffallend ist aber bereits jetzt eine Trennung der OS-Kurven nach 24 Monaten zugunsten von Pembrolizumab (Abb. 2). Die Toxizitäten waren, vor allem im Vergleich zu den adjuvanten TKI-Studien, mit einer Grad-3–4- Inzidenz von 18,9% gering und es gab keine Therapie-assoziierten Todesfälle. Somit stellt Keynote-564 die erste positive adjuvante ICI-Studie beim lokalisierten RCC dar. Die Zulassung wird auf Basis des günstigen Nutzen-Risiko-Profils erwartet.
Abb. 1: Krankheitsfreies Überleben in der Intention-to-treat-Population in der KEYNOTE-564-Studie (nach Choueiri et al.)4
Abb. 2: Interimsanalyse zum Gesamtüberleben in der Intention-to-treat-Population in der KEYNOTE-564-Studie (nach Choueiri et al.)4
Zytoreduktive Nephrektomie
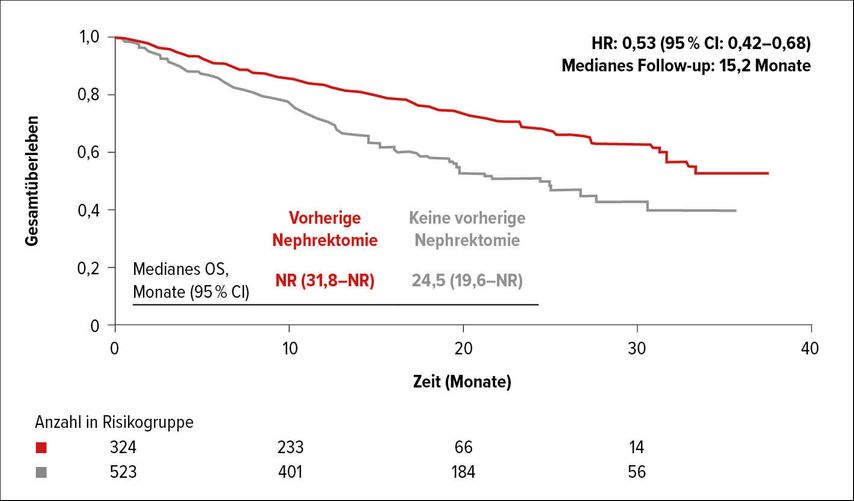
Seit Vorstellung der Ergebnisse der CARMENA-Studie5 wurde der Benefit einer zytoreduktiven Nephrektomie (CN) bei Patienten mit mittlerem und ungünstigem Risiko infrage gestellt. In dieser Studie war Sunitinib allein in Bezug auf Überleben einer Strategie „CN gefolgt von Sunitinib“ nicht unterlegen. Dennoch blieben über die Jahre erhebliche Zweifel an der Aussagekraft dieser Studie, denn einerseits stellt Sunitinib heute nicht mehr die Standardtherapie dar und andererseits hatten in manchen Subgruppen Patienten doch einen Vorteil durch CN. Zudem wurden zahlreiche Patienten im CN+Sunitinib-Arm nicht nephrektomiert oder erhielten kein Sutent und im Sunitinib-Arm gab es Patienten, die dennoch nephrektomiert wurden. Im Lichte dieser bestehenden Zweifel war die Analyse von Fallah und Kollegen6 besonders wertvoll. Hierbei handelt es sich um eine FDA-gepoolte Analyse zum Überlebensbenefit durch CN aus 5 randomisierten, auf ICI-Kombination basierenden, Erstlinienstudien (Phase II und III). Nach einer medianen Nachbeobachtungszeit von 15,2 Monaten zeigte sich für Patienten, die nephrektomiert waren, ein statistisch signifikanter OS-Vorteil (NR [nicht erreicht] [31,8–NR] versus 24,5 Monate [19,6–NR] für Patienten ohne Nephrektomie; HR: 0,53; 95% CI: 0,42–0,69 und HR korrigiert für Alter und Prognosegruppe: 0,59; 95% CI: 0,46–0,75) (Abb. 3).
Abb. 3: Medianes Gesamtüberleben mit oder ohne Nephrektomie bei Patienten mit einer Erstlinien-ICI-Kombinationstherapie (nach Fallah et al.)6
Highlights aus der First Line
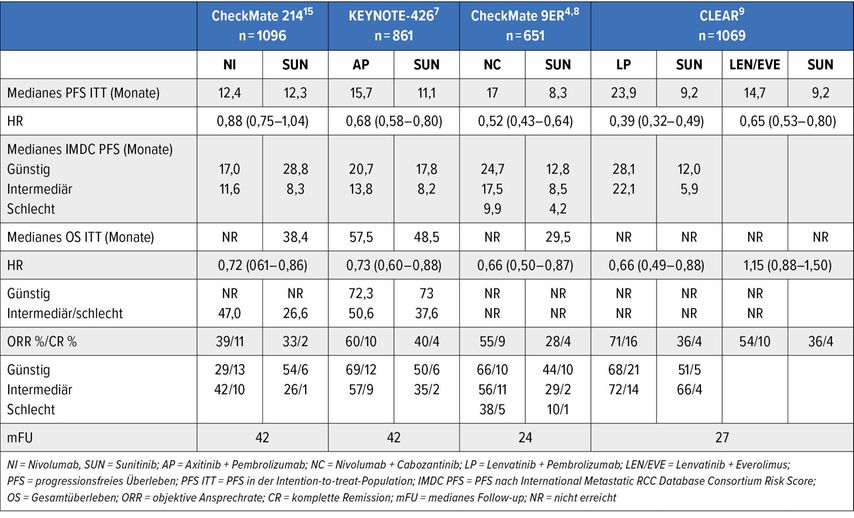
Auf Basis der Ergebnisse der ICI-Kombinationsstudien der letzten 4 Jahre werden für Patienten aller IMDC-Gruppen entweder Axitinib + Pembrolizumab oder Cabozantinib + Nivolumab oder Lenvatinib + Pembrolizumab empfohlen (alle IA-Empfehlung) sowie zusätzlich für Patienten mit intermediärem/hohem Risiko Nivolumab + Ipilimumab.
Ergebnisse zum längeren Follow-up wurden für Axitinib+Pembrolizumab7 und Nivolumab+Cabozantinib8 präsentiert, für die Nivolumab+Cabozantinib-Studie und die Lenvatinib+Pembrolizumab-Studie gab es zudem Lebensqualitätsanalysen. Subgruppenanalysen mit längerer Nachbeobachtungszeit sind in Tabelle 2, der Vollständigkeit halber für alle Erstlinientherapien mit OS-Benefit dargestellt. Betreffend die Lenvatinib+Pembrolizumab-Studie wurden auch Ergebnisse zur Beziehung der Tiefe des Ansprechens zum Überleben präsentiert.9
CheckMate 9ER
Eine Post-hoc-Analyse der CheckMate- 9ER-Studie, die die Kombinationstherapie aus Nivolumab + Cabozantinib untersucht hatte, führte eine Auswertung in Bezug auf Q-TWIST („quality-adjusted time without symptoms or toxicity“) durch. Diese Analyse ergab einen Gewinn an Q-TWIST von 4,0 Monaten (95% CI: 2,4–5,7), was einem relativen Gewinn von 16,9% entspricht. Zum Großteil war dieser Gewinn durch zusätzliche Zeit (+4,7 Monate) in gutem Gesundheitszustand bedingt.10
Lebensqualität unter Lenvatinib + Pembrolizumab
Zusammenfassend zeigt sich in der Studie von Motzer und Kollegen für Lenvatinib + Pembrolizumab im Vergleich zu Sunitinib die gleiche oder in manchen Bereichen (Fatigue, Dyspnoe, Obstipation) eine verbesserte Lebensqualität (HRQoL); im Gegensatz dazu war die HRQoL mit Lenvatinib + Everolimus gleich oder schlechter als im Sunitinib-Arm.11
Ansprechtiefe und Überleben
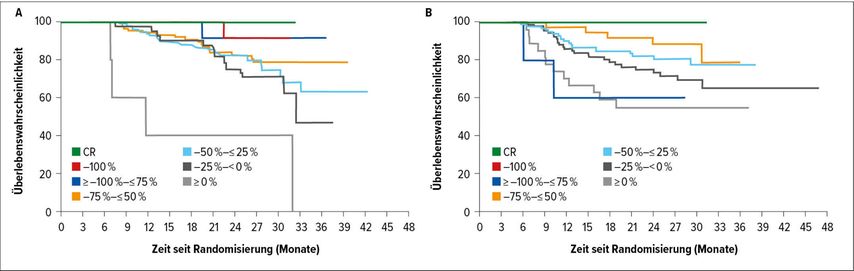
Die Beziehung Ansprechtiefe zu Überleben unter Lenvatinib + Pembrolizumab ist in Abbildung 4 dargestellt.9 In der Intention-to-treat-Population konnte bei 79,3% der Patienten, die eine Komplettremission (CR) erreicht hatten, diese auch nach 2 Jahren noch bestätigt werden und bei 74,3% auch nach 3 Jahren. Die 2-Jahres-Überlebensrate war zudem bei Patienten mit CR oder Remission von >75% des Tumorausmaßes ident. In Bezug auf Benefit in einzelnen Subgruppen ist die erfreulich hohe Rate an Komplettremissionen mit Pembrolizumab + Lenvatinib im Vergleich zu Sunitinib zu erwähnen (14% versus 3,9% bei intermediärem/hohem Risiko) und 20,9% versus 4,8% bei günstigem Risiko. Auch die Dauer des Ansprechens ist für die ICI-Kombination im Vergleich zu Sunitinib überzeugend (median 25,8 versus 12,9 Monate bei intermediärem/hohem Risiko und median 26,3 versus 14,7 Monate bei günstigem Risiko).
Abb. 4: 6-Monats-Analyse des Gesamtüberlebens nach Ansprechtiefe ermittelt nach RECIST 1.1. A: Lenvatinib + Pembrolizumab. B: Sunitinib (nach Grünwald et al.)9
Highlights beim nicht klarzelligen mRCC
Die Kombination Nivolumab + Cabozantinib (mit 0–1 vorangehenden Therapien) wurde in einer Single-Center-Phase-II-Studie von Lee und Kollegen untersucht.12 Hierbei wurden zwei Kohorten untersucht. Kohorte 1 waren Patienten mit papillären, unklassifizierten oder Translokationskarzinomen; Kohorte 2 Patienten mit chromophobem Karzinom. Während in Kohorte 1 eine objektive Ansprechrate (ORR) von 47,5% (31,5–63,9) und ein medianes PFS von 12,5 (6,3–15,9) erreicht wurde, konnte die Kombinationstherapie in Kohorte 2 nicht überzeugen (ORR 0%).
Aktins und Kollegen präsentierten die Kohorte B (nicht klarzelliges RCC) der HCRN-GU16-260-Studie, bei der die Therapie mit Nivolumab-Monotherapie initiiert wurde und nur bei Progression oder Stabilisierung als bestes Ansprechen mit Ipilimumab ergänzt wurde.13 Unter Nivolumab-Monotherapie kam es bei 22,9% der Patienten zu einem Ansprechen nach Immun-RECIST-Kriterien; ein Boost mit Ipilimumab konnte nur bei 6% der Patienten eine Remission herbeiführen.
Ductus-Bellini-Karzinom
Die BONSAI-Studie14 untersuchte diese besonders aggressive und seltene Form eines RCC, die üblicherweise in der Erstlinie mit Cisplatin und Gemcitabin behandelt wird. Insgesamt gibt es sonst kaum Evidenz für eine sinnvolle Therapie und keine ist bislang mit einer durchschlagenden Wirkung assoziiert. In einer kleinen Studie mit 25 Patienten konnten Procoppio und Kollegen mit Cabozantinib-Monotherapie (60mg) ein Ansprechen bei 35% der Patienten erreichen, ein Patient erreichte sogar eine Komplettremission. Das mediane Gesamtüberleben blieb jedoch bei 6 Monaten zurück.
Probiotika beim mRCC
In einer randomisierten Phase-Ib-Studie wurde der Benefit einer Gabe von Butyrat-produzierendem Clostridium butyricum bei Patienten unter Nivolumab + Ipilimumab untersucht. Stuhlsequenzierungen ergaben bei Patienten mit Substitution eine achtfache Steigerung von Bacterium bifidum und Bacterium adolescentis. Clostridium butyricum wurde nur bei Patienten mit Substitution nachgewiesen, dafür waren pathogene Darmkeime viel häufiger bei Patienten ohne Substitution zu beobachten. Bemerkenswert ist auch, wie sich die Substitution auf das Therapieansprechen auswirkte: Die Ansprechraten betrugen 59% versus 11% und das mediane PFS war nicht erreicht versus 11 Wochen für Patienten mit versus ohne Probiotikum.
Literatur:
1 Leibovich BC et al.: Prediction of progression after radical nephrectomy for patients with clear cell renal cell carcinoma: a stratification tool for prospective clinical trials. Cancer 2003; 97(7): 1663-71 2 Ravaud A et al.: Adjuvant sunitinib in high-risk renal-cell carcinoma after nephrectomy. N Engl J Med 2016; 375(23): 2246-54 3 Sun M et al.: Adjuvant vascular endothelial growth factor-targeted therapy in renal cell carcinoma: a systematic review and pooled analysis. Eur Urol 2018; 74(5): 611-20 4 Choueiri TK et al.: Pembrolizumab versus placebo as post-nephrectomy adjuvant therapy for patients with renal cell carcinoma: Randomized, double-blind, phase III KEYNOTE-564 study. ASCO 2021, Abstr. #LBA5 5 Méjean A et al.: Sunitinib alone or after nephrectomy in metastatic renal-cell carcinoma. N Engl J Med 2018; 379(5): 417-27 6 Fallah J et al.: Survival benefit of nephrectomy prior to immunotherapy-based combinations in patients with metastatic renal cell carcinoma: an FDA pooled analysis. ASCO 2021, Abstr. #4516 7 Rini BI et al.: Pembrolizumab (pembro) plus axitinib (axi) versus sunitinib as first-line therapy for advanced clear cell renal cell carcinoma (ccRCC): results from 42-month follow-up of KEYNOTE-426. ASCO 2021, Abstr. #4500 8 Apolo A et al.: Nivolumab plus cabozantinib (N+C) versus sunitinib (S) for advanced renal cell carcinoma (aRCC): outcomes by baseline disease characteristics in the phase 3 CheckMate 9ER trial. ASCO 2021, Abstr. #4553 9 Grünwald V et al.: Analysis of the CLEAR study in patients (pts) with advanced renal cell carcinoma (RCC): depth of response and efficacy for selected subgroups in the lenvatinib (LEN) + pembrolizumab (PEMBRO) and sunitinib (SUN) treatment arms. ASCO 2021, Abstr. #4560 10 Cella D et al.: Quality-adjusted time without symptoms of disease progression or toxicity (Q-TWiST) of nivolumab plus cabozantinib (N+C) versus sunitinib (SUN) in treatment-naïve, advanced/metastatic renal cell carcinoma (aRCC): a post-hoc analysis of CheckMate 9ER (CM 9ER) data. ASCO 2021, Abstr. #6567 11 Motzer R et al.: Health-related quality-of-life (HRQoL) analysis from the phase 3 CLEAR trial of lenvatinib (LEN) plus pembrolizumab (PEMBRO) or everolimus (EVE) versus sunitinib (SUN) for patients (pts) with advanced renal cell carcinoma (aRCC). ASCO 2021, Abstr. #4502 12 Lee CH et al.: Nivolumab plus cabozantinib in patients with non-clear cell renal cell carcinoma: results of a phase 2 trial. ASCO 2021, Abstr. #4509 13 Atkins et al.: Phase II study of nivolumab and salvage nivolumab + ipilimumab in treatment-naïve patients (pts) with advanced non-clear cell renal cell carcinoma (nccRCC) (HCRN GU16-260-Cohort B). ASCO 2021, Abstr. #4510 14 Procopio G et al.: A phase 2 prospective trial of cabozantinib as first-line treatment for metastatic collecting ducts renal cell carcinoma: the BONSAI trial (Meeturo 2) clinical trial information—NCT03354884. ASCO 2021, Abstr. #4571 15 Albiges L et al.: ESMO Open 2020
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...