Das Aderhautmelanom – vom Mauerblümchen zur Pfingstrose
Bericht:
Dipl.-Ing. Dr. Manuel Spaltl-Zoidl
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Das Aderhautmelanom stellt durch seine außerordentliche Behandlungsresistenz und hohe Mortalitätsrate eine große Belastung für Betroffene dar. In der Webinarreihe „How I Treat“ präsentierte Prof. Dr. Reinhard Dummer, Universitätsspital Zürich, aktuelle Fakten sowie Daten über Therapieoptionen für Patient:innen mit dieser seltenen Erkrankung.
Keypoints
-
Chemo- und zielgerichtete Monotherapien spielen für die Behandlung des metastasierten Aderhautmelanoms keine Rolle.
-
Tebentafusp stellt die Erst-linientherapie der Wahl für HLA-A2+ Patient:innen mit Aderhautmelanom dar.
-
Ein Monitoring der ctDNA-Spiegel kann wertvolle prognostische und prädiktive Informationen über den Behandlungsverlauf liefern.
Die Besonderheiten des Aderhautmelanoms
Das metastasierte Aderhautmelanom deckt etwa 5% aller Melanome ab. Ähnlich wie bei kutanen Melanomen sind unter anderem eine große Anzahl von Nävi und Sonnenbränden, ein heller Hauttyp und blaue Augen Risikofaktoren der Erkrankung. Anders als bei kutanen Melanomen spielt der Einfluss von UV-Strahlung hier jedoch keine direkte Rolle. Das Melanom befindet sich auf der Choroidea, wo es durch die Anatomie des Auges vor Strahlung abgeschirmt wird. Dies bedeutet auch, dass Aderhautmelanome außerhalb der Ophthalmologie nicht spontan erkannt werden können.1
Das Aderhautmelanom metastasiert typischerweise in die Leber. Dies ist möglicherweise der hohen Anzahl an MET-Rezeptoren an dessen Oberfläche geschuldet. Diese werden unter anderem durch den Hepatozyten-Wachstumsfaktor stimuliert, sodass die Leber ein optimales Milieu bietet. Bei Obduktionen von Patient:innen mit metastasierenden okulären Melanomen findet man, so Dummer, allerdings schockierend wenige Knoten in der Leber. Häufig unterschätzen Kliniker:innen daher die Tumorlast durch herkömmliche Bildgebung.1
Therapieoptionen bisher enttäuschend
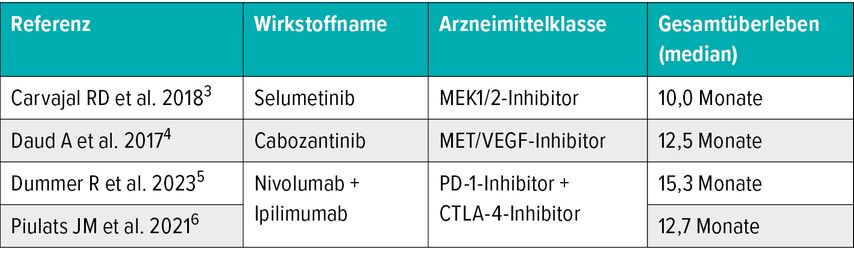
Aderhautmelanome sind äußerst behandlungsresistent, betonte Dummer. Die wichtigsten Lokalbehandlungen umfassen üblicherweise die Enukleation, Strahlentherapie und, wenn vorhanden, Protonenbestrahlung.1 Im fortgeschrittenen oder metastasierten Stadium stehen jedoch so gut wie keine wirksamen Behandlungsmöglichkeiten zur Verfügung. Aderhautmelanome sprechen praktisch nicht auf Chemotherapie oder auf Monotherapien mit Kinaseinhibitoren an. Sie haben wenig aktivierende Mutationen und sind unzureichend von T-Lymphozyten infiltriert. Selbst PD-1-Inhibitoren versagen beim Aderhautmelanom mit einer Ansprechrate unter 10% und einer medianen Überlebenszeit (mOS) von 12 Monaten dramatisch (Tab. 1).2–6
Tab. 1: Medianes Gesamtüberleben durch verschiedene Arzneimittelklassen bei der Behandlung des Aderhautmelanoms (modifiziert nach Carvajal RD et al. 2018, Daud A et al. 2017, Dummer R et al. 2023, Piulats JM et al. 2021)3–6
Vielversprechende neue Therapieoption
In Form eines bispezifischen Fusionsproteins steht heute eine vielversprechende neue Option zur Behandlung des inoperablen oder metastasierten Aderhautmelanoms zur Verfügung.7 Der Wirkstoff Tebentafusp kombiniert einen T-Zell-Rezeptor als Steuerdomäne und ein Antikörperfragment als Effektordomäne. Die Steuerdomäne bindet mit hoher Affinität an gp100. Dieses Peptid wird vom humanen Leukozyten-Antigen-A*02:01 (HLA-A*02:01) auf der Zelloberfläche von Aderhautmelanomzellen präsentiert. Die Effektordomäne bindet an CD3-Rezeptoren der polyklonalen T-Zellen. Durch die bispezifische Bindung wird eine immunologische Synapse hergestellt, welche polyklonale T-Zellen, unabhängig von deren ursprünglicher Spezifität, aktiviert. Nach der Aktivierung setzen die T-Zellen inflammatorische Zytokine und zytolytische Proteine frei und sorgen so für die Lyse der Tumorzellen.7,8
Die Sicherheit und Wirksamkeit von Tebentafusp wurden im Rahmen einer randomisierten Phase-III-Studie untersucht. 378 Patient:innen mit metastasiertem HLA-A*02:01-positivem Aderhautmelanom ohne systemische Vorbehandlung wurden im Verhältnis 2:1 randomisiert, um Tebentafusp oder ein von Prüfärzt:innen ausgewähltes Vergleichspräparat (Pembrolizumab, Ipilimumab oder Dacarbazin) zu erhalten. Primärer Endpunkt der Studie war das Gesamtüberleben.9
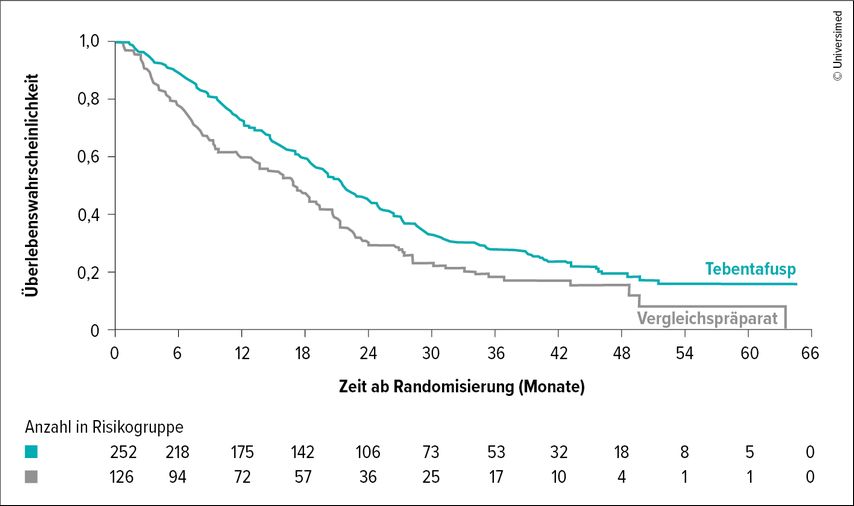
Nach drei Jahren zeigte Tebentafusp gegenüber dem Vergleichspräparat eine statistisch signifikante Risikoreduktion von 24% (HR: 0,76; 95%CI: 0,60–0,97) hinsichtlich des progressionsfreien Überlebens und 32% (HR: 0,68; 95%CI: 0,54–0,87) hinsichtlich des Gesamtüberlebens. Das mOS betrug 21,6 Monate in der Tebentafusp-Gruppe, während Patient:innen, die mit dem Vergleichspräparat behandelt wurden, im Median nur 16,9 Monate überlebten (Abb. 1).10
Abb. 1: Kaplan-Meier-Kurve der Überlebenswahrscheinlichkeit über die Zeit (modifiziert nach Hassel JC et al. 2023)10
Neben der Gesamtmortalität wurde auch der Einfluss von Biomarkern, wie beispielsweise zirkulierender Tumor-DNA (ctDNA), auf die Therapie mit Tebentafusp untersucht. 88% der Patient:innen, die mit Tebentafusp behandelt wurden, erreichten eine Reduktion des ctDNA-Spiegels von mindestens 50% nach neun Wochen. Dies war mit einem Überlebensvorteil von 68% gegenüber jener Gruppe, die keine 50%ige Reduktion des ctDNA-Spiegels erreichte, assoziiert (HR: 0,32; 95%CI: 0,21–0,50). Bei 37% der Pati-ent:innen konnte nach neun Wochen keine ctDNA mehr nachgewiesen werden. Dies war mit einer statistisch signifikanten Risikoreduktion von 69% verbunden (HR: 0,41; 95%CI: 0,25–0,67).10
Unerwünschte Ereignisse traten unter Tebentafusp in der Regel im ersten Monat auf und führten bei 2% der Patient:innen zu einem Behandlungsabbruch. Todesfälle traten während der Studie nicht auf, präsentierte Dummer.9 Zu den häufigsten beobachteten Nebenwirkungen zählen das Zytokin-Freisetzungssyndrom (88%), Ausschlag (85%), Fieber (79%), Pruritus (72%), Ermüdung (66%), Übelkeit (56%), Schüttelfrost (55%), Abdominalschmerz (49%), Ödem (49%), Hypo-/Hyperpigmentierung (48%), Hypotonie (4%), trockene Haut (35%), Kopfschmerzen (32%) und Erbrechen (34%).7
Zukünftige Therapien in frühen Studienphasen
Dummer schloss seinen Vortrag mit einem Ausblick auf vielversprechende Behandlungsansätze, die sich jedoch noch in frühen Studienphasen befinden. Das sind unter anderem die autologe T-Zell-Therapie der „preferentially expressed antigen in melanoma(PRAME)“-fortgeschrittenen Tumoren bei HLA-A*02-positiven Patient:innen.11 Auch „antibody-drug conjugates“ (ADC) werden für die Behandlung von Aderhautmelanomen und anderen GNAQ/11-mutierten Melanomen untersucht.12 Außerdem wird eine Kombination von Darovasertib plus Crizotinib für die Behandlung von Patient:innen mit metastasiertem Aderhautmelanom evaluiert.13
Quelle:
Fortbildungsreihe Onkologie virtuell „How I Treat“, 17.6.2025, online
Literatur:
1 Jager MJ et al.: Uveal melanoma. Nat Rev Dis Primers 2020; 6(1): 24 2 Pham JP et al.: Efficacy of immune checkpoint inhibition in metastatic uveal melanoma: a systematic review and meta-analysis. Melanoma Res 2023; 33(4): 316-25 3 Carvajal RD et al.: Selumetinib in combination with dacarbazine in patients with metastatic uveal melanoma: a phase III, multicenter, randomized trial (SUMIT). J Clin Oncol 2018; 36(12): 1232-9 4 Daud A et al.: Phase II randomised discontinuation trial of the MET/VEGF receptor inhibitor cabozantinib in metastatic melanoma. Br J Cancer 2017; 116(4): 432-40 5 Dummer R et al.: First-line, fixed-duration nivolumab plus ipilimumab followed by nivolumab in clinically diverse patient populations with unresectable stage III or IV melanoma: CheckMate 401. JClin Oncol 2023; 41(23): 3917-29 6 Piulats JM et al.: Nivolumab plus ipilimumab for treatment-naïve metastatic uveal melanoma: an open-label, multicenter, phase II trial by the Spanish Multidisciplinary Melanoma Group (GEM-1402). J Clin Oncol 2021; 39(6): 586-98 7 Kimmtrak® aktuelle Fachinformation. Stand März 2025 8 Hassel JC et al.: Practical guidelines for the management of adverse events of the T cell engager bispecific tebentafusp. Eur J Cancer 2023; 191: 112986 9 Nathan P et al.: Overall survival benefit with tebentafusp in metastatic uveal melanoma. N Engl J Med 2021; 385: 1196-206 10 Hassel JC et al.: Three-year overall survival with tebentafusp in metastatic uveal melanoma. N Engl J Med 2023; 389(24): 2256-66 11 Wermke M et al.: Autologous T cell therapy for PRAME+ advanced solid tumors in HLA-A*02+ patients: aphase 1 trial. Nat Med 2025; (published online 09 Apr) 12 Carlino MS et al.: A first-in-human study of DYP688, an antibody drug conjugate delivering a direct Gq/11 inhibitor, in patients with metastatic uveal melanoma (MUM) and other GNAQ/11 mutant melanomas. J Clin Oncol 2025; 43(16_suppl): 9509 13 Piperno-Neumann S et al.: A phase I trial of LXS196, a protein kinase C (PKC) inhibitor, for metastatic uveal melanoma. Br J Cancer 2023; 128(6): 1040-51
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...