Psychothérapie augmentée à la kétamine
Auteurs:
Prof. univ. Dr méd. Martin Walter
Leonard Marx
Universitätsklinik für Psychiatrie und Psychotherapie
Universitätsklinikum Jena
E-mail: martin.walter@med.uni-jena.de
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
La (S-)kétamine, antidépresseur à action rapide, est utilisée de manière efficace chez les patient·es présentant une résistance aux traitements. Pour les doses subanesthésiques, on suppose qu’une composante centrale du mécanisme d’action biphasique réside dans l’ouverture d’une fenêtre de neuroplasticité, qui devrait être exploitée sur le plan psychothérapeutique afin de transformer un soulagement rapide des symptômes en une réponse durable.
Keypoints
-
Outre son utilisation anesthésique bien établie, la kétamine est un antidépresseur à action rapide: des effets cliniques surviennent en l’espace de quelques heures, y compris chez les patient·es présentant une résistance aux traitements.
-
Environ 24 heures après son administration, la kétamine induit une fenêtre de neuroplasticité susceptible d’accroître l’efficacité des interventions psychothérapeutiques.
-
Les données probantes restent toutefois insuffisantes pour recommander des protocoles spécifiques de psychothérapie augmentée par la kétamine, ce qui rend nécessaires des études randomisées et contrôlées représentatives.
Environ 30% des patient·es souffrant de dépression remplissent, au cours de leur prise en charge, les critères d’une dépression dite résistante aux traitements (TRD), dans la mesure où aucune rémission n’est obtenue après deux essais thérapeutiques utilisant des antidépresseurs de classes pharmacologiques différentes, administrés à des doses adéquates.1Outre l’augmentation par des antipsychotiques, le lithium ou l’association avec un second antidépresseur, la (S-)kétamine peut être envisagée comme option thérapeutique, conformément aux recommandations actuelles.2
Kétamine: ancienne substance, nouveaux champs d’application
Ainsi, plus de cinquante ans après sa première autorisation en tant qu’anesthésique et plus de vingt ans après la mise en évidence de son potentiel antidépresseur – avec pour conséquence une utilisation hors indication croissante – l’énantiomère S de la kétamine, antagoniste des récepteurs NMDA, fait officiellement partie de la pharmacothérapie psychiatrique depuis environ cinq ans. Alors que son effet anesthésique nécessite des doses élevées pouvant nécessiter une association avec un hypnotique, le traitement antidépresseur repose sur des doses subanesthésiques de principe actif, ce qui améliore nettement le profil d’effets indésirables. Dans le contexte psychiatrique, la kétamine présente en outre l’avantage d’induire des taux de réponse relativement élevés, y compris chez des patient·es résistant·es à d’autres approches thérapeutiques, tandis que les antidépresseurs conventionnels sont connus pour voir leur taux de réponse diminuer à chaque changement de médicament.
Modèle d’action biphasique avec fenêtre de neuroplasticité
Le principal bénéfice de la kétamine dans le traitement de la dépression réside probablement dans sa faible latence d’action, ce qui la classe parmi les antidépresseurs à action rapide. Elle se distingue ainsi nettement des antidépresseurs monoaminergiques, dont l’effet ne se manifeste qu’après une latence de plusieurs semaines, bien qu’ils entraînent rapidement une élévation biologique des concentrations de sérotonine, de noradrénaline ou de dopamine. Cette observation soulève à son tour des questions quant au mécanisme d’action exact des antidépresseurs conventionnels et a récemment remis en question l’hypothèse sérotoninergique de la dépression. Il convient toutefois de noter que, pour l’ensemble des antidépresseurs autorisés à ce jour, un maintien prolongé de concentrations plasmatiques de la substance ou de son métabolite actif est requis.
Le mode d’action de la kétamine diffère fondamentalement de celui des traitements monoaminergiques: elle agit rapidement, généralement entre deux et 24 heures après l’administration, mais atteint son effet maximal à un moment où, en raison de son élimination rapide, aucune concentration active significative n’est attendue. Cela s’explique par le fait que l’administration est le plus souvent limitée à quelques minutes (spray nasal) ou, au maximum, à une heure (perfusion), et que la courte demi-vie d’environ 180 minutes, associée à une redistribution rapide, restreint l’effet aigu à ces périodes.
Cette dissociation entre le pic de concentration en principe actif et l’effet maximal s’explique par le blocage allostérique aigu des récepteurs NMDA (NMDAR) par la kétamine – probablement de manière préférentielle au niveau des interneurones inhibiteurs en raison de leur activité tonique – entraînant une désinhibition des synapses glutamatergiques et une activation subséquente des récepteurs AMPA. La (S-)kétamine présente une affinité environ quatre fois plus élevée pour les NMDAR que l’énantiomère R.3 Outre l’augmentation globale de la transmission synaptique, ce mécanisme induit une sécrétion accrue du facteur neurotrophique BDNF («brain-derived neurotrophic factor») qui, via sa liaison au récepteur TrkB (tropomyosin receptor kinase), déclenche de nombreux processus de neuroplasticité qui persistent après l’élimination de la substance. La kétamine induit ainsi non seulement une réorganisation aiguë de la connectivité fonctionnelle, mais exerce également des effets neuroprotecteurs et neuroplastiques par le renforcement des synapses existantes et la formation de nouvelles connexions, effets qui se prolongent au-delà de la demi-vie du médicament.4
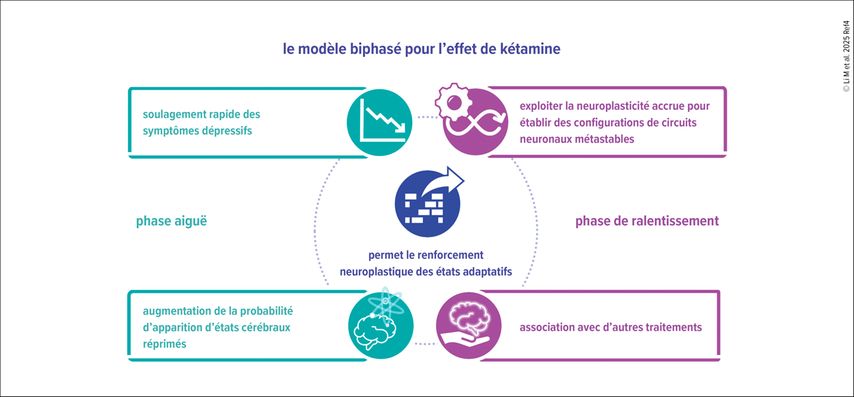
Fig. 1: Le modèle d’action biphasique permet d’expliquer à la fois les effets positifs aigus et persistants dans le traitement de la dépression résistante aux traitements (Li M et al. 2025)4
Des modèles animaux précliniques ont suggéré une évolution temporelle de l’effet antidépresseur de la kétamine, hypothèse confirmée par de nombreuses études cliniques: le soulagement des symptômes survient en l’espace de quelques heures et suit l’augmentation centrale de la neurotransmission glutamatergique. Durant cette phase, des connexions neuronales dysfonctionnelles sont temporairement interrompues – notamment l’hyperconnectivité associée aux symptômes dépressifs au sein du «default mode network»5 – tandis que la probabilité d’émergence d’états cérébraux jusque-là inhibés augmente. Cette phase aiguë ouvre, environ 24 heures après l’administration de kétamine, une fenêtre temporelle de neuroplasticité au cours de laquelle des configurations de réseau métastables favorisent l’émergence de modes de pensée et de comportement alternatifs. À ce stade, le soulagement des symptômes est maximal et une augmentation transitoire du métabolisme glutamatergique est corrélée à une élévation de la concentration des marqueurs de plasticité.6 Au cours de la phase tardive ou différée, qui s’étend globalement d’un à trois jours après l’administration, les schémas neuronaux adaptatifs précédemment inhibés peuvent être stabilisés après une phase initiale de renforcement; les patient·es continuent alors de bénéficier d’une plasticité accrue, tandis que les effets indésirables potentiels se sont estompés.7
Implications thérapeutiques de la fenêtre de neuroplasticité
Bien que les effets antidépresseurs de la kétamine persistent après son élimination complète, une administration uniques’avère souvent insuffisante; des perfusions sérielles ou des administrations intranasales sont donc indiquées afin de prolonger l’effet thérapeutique. Ces traitements d’entretien, qui prévoient généralement deux administrations par semaine sur une durée de trois semaines ou plus, peuvent prolonger le soulagement des symptômes jusqu’à 45 jours.8 Néanmoins, même en l’absence de risques clairement démontrés à ce jour – tels qu’un développement de tolérance ou un potentiel de dépendance et d’abus – un traitement prolongé par la kétamine est actuellement considéré comme inapproprié. La combinaison de la kétamine avec d’autres méthodes thérapeutiques – en particulier la psychothérapie, qui vise une modification durable des schémas interactionnels dysfonctionnels – fait donc l’objet de recherches intensives. Outre un gain en termes de sécurité, la fenêtre de neuroplasticité peut être exploitée pour cibler de manière spécifique, dans le cadre thérapeutique, des schémas de traitement et de comportement mal adaptés. En termes simplifiés, la kétamine augmente, durant une période temporelle définie, la capacité d’apprentissage, laquelle est de toute façon essentielle à l’efficacité des interventions psychothérapeutiques. Par ailleurs, un soulagement précoce des symptômes permet de contrecarrer les troubles cognitifs associés à la dépression, pouvant aller jusqu’au tableau clinique de la pseudodémence, et susceptibles d’entraver l’instauration d’une psychothérapie efficace.
En levant rapidement des schémas neuronaux rigides et en favorisant un état cérébral plus flexible et adaptable, la kétamine crée un environnement dans lequel des approches telles que la psychothérapie, d’autres interventions comportementales ou encore le neurofeedback peuvent produire des effets plus durables que la monothérapie pharmacologique.
Le terme d’augmentation désigne l’adjonction à une thérapie établie d’une procédure supplémentaire, dotée d’une efficacité propre, dans le but d’obtenir un effet additif. Afin que la psychothérapie puisse être menée dans son cadre conceptuel initial, la psychothérapie augmentée par la kétamine – contrairement aux approches dites «assistées par la kétamine» – suppose une fonction de conscience intacte. Celle-ci est généralement rétablie quelques heures seulement après l’administration de kétamine. Toutefois, en raison des effets négatifs connus des substances bloquant les récepteurs NMDA sur la consolidation mnésique pendant le sommeil, la psychothérapie est le plus souvent réalisée le lendemain.
À l’inverse, les approches dites «assistées par la kétamine» mentionnées précédemment cherchent explicitement à exploiter, à des fins thérapeutiques, les effets transitoires de modification de la conscience survenant durant l’administration. À cette fin, une phase aiguë prolongée est généralement induite au moyen de protocoles de perfusion étendus; selon le degré d’altération cognitive, différentes interventions sont alors proposées, lesquelles ne constituent toutefois pas, en tant que telles, une forme de psychothérapie reconnue. En conséquence, seule une combinaison différée avec une méthode psychothérapeutique établie peut être qualifiée d’augmentation au sens strict. Les deux modalités d’administration initiale – par perfusion intraveineuse ou par voie intranasale – sont, à cet égard, comparables. D’un point de vue clinique, il convient toutefois de souligner que seule l’administration intranasale est actuellement autorisée et remboursée.
Malgré cette autorisation, le schéma thérapeutique optimal de la psychothérapie augmentée par la kétamine doit encore être identifié et étayé par des données probantes, dans le cadre d’études randomisées et contrôlées incluant des populations aussi larges et représentatives que possible. Le «Cognitive Behavioral Analysis System of Psychotherapy» (CBASP), concept thérapeutique spécifiquement développé pour le traitement de la dépression chronique, est actuellement évalué comme option, en particulier pour ce groupe de patient·es. Les services de psychiatrie des cliniques universitaires de Jena, de Tübingen, de Berlin (Charité) et de Munich (LMU) mènent actuellement une étude multicentrique à ce sujet. L’objectif est d’évaluer si une thérapie CBASP augmentée par la kétamine entraîne une réduction plus marquée des symptômes chez les patient·es atteint·es de TRD qu’une combinaison CBASP-placebo ou que l’augmentation par la kétamine de thérapies standard établies.
Si le potentiel thérapeutique de la fenêtre de neuroplasticité peut être exploité de manière ciblée, la psychothérapie augmentée par la kétamine pourrait, à long terme, contribuer à améliorer l’efficacité et la sécurité des approches thérapeutiques existantes et ainsi réduire la fréquence des évolutions résistantes aux traitements. Une réponse plus rapide à une psychothérapie pourtant fondamentalement efficace permettrait en outre de tirer un meilleur parti de sa disponibilité très limitée. Cela optimiserait notamment son applicabilité dans des contextes thérapeutiques stationnaires spécifiques.
Littérature:
1 McIntyre RS et al.: Treatment-resistant depression: definition, prevalence, detection, management, and investigational interventions. World Psychiatry 2023; 22: 394-412 2 Bundesärztekammer (BÄK) et al.: Nationale VersorgungsLeitlinie Unipolare Depression – Langfassung, Version 3.2. 2022,dernier accès le 28.10.2025, doi: 10.6101/AZQ/000505 3 Zanos P, Gould TD: Mechanisms of ketamine action as an antidepressant. Mol Psychiatry 2018; 23(4): 801-11 4 Li M et al.: Dynamic processes induced by Ketamine and their potential for augmented treatment strategies in neuropsychiatric disorders. In: Himmelseher S.: Ketamine. Neuromethods, vol 224. Humana, New York, NY 2025, 297-232 5 Greicius MD et al.: Resting-state functional connectivity in major depression: abnormally increased contributions from subgenual cingulate cortex and thalamus. Biol Psychiatry 2007; 62(5): 429-37 6 Marx L et al.: Association between S-ketamine induced changes in glutamate levels in the pregenual anterior cingulate cortex and plasma brain-derived neurotrophic factor in healthy subjects. Front Psychiatry, Sec Mood Disorders 2025; 16: 1662051 7 Walter M et al.: Multistage drug effects of ketamine in the treatment of major depression. Eur Arch Psychiatry Clin Neurosci 2014; 264(Suppl 1): S55-S65 8 Aan het Rot M et al.: Safety and efficacy of repeated-dose intravenous ketamine for treatment-resistant depression. Biol Psychiatry 2010; 67(2): 139-45
Das könnte Sie auch interessieren:
Mécanismes d’action de l’ECT en tant que traitement alternatif de la dépression
La dépression compte parmi les troubles psychiques les plus fréquents et les plus invalidants, mais ses fondements neurobiologiques ne sont à ce jour que partiellement élucidés. L’ ...
Diagnostic de la SLA: des biomarqueursà la cognition et au comportement
L’hétérogénéité de la sclérose latérale amyotrophique (SLA) ne facilite pas le diagnostic. À cela s’ajoute le fait que la pathogenèse n’est toujours pas bien comprise et que les ...
Comment réduire le délai nécessaire jusqu’au diagnostic de la SLA?
La sclérose latérale amyotrophique (SLA) est une maladie neurodégénérative qui progresse inexorablement et conduit au décès par défaillance des muscles respiratoires en moyenne trois à ...