Tumeurs du foie et des voies biliaires
Compte-rendu:
Dre Corina Ringsell
Rédactrice
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Les lésions hépatiques focales sont souvent détectées lors d’examens par TDM, IRM ou échographie, non seulement en gastroentérologie et en hépatologie, mais aussi en médecine interne et en médecine de premier recours. Le PD Dr Dr méd. David Semela, Clinique de gastroentérologie et d’hépatologie, HOCH Health Ostschweiz, Saint-Gall, a expliqué comment les diagnostiquer et les signes indiquant une tumeur maligne.
La Swiss Association for the Study of the Liver (SASL) a publié une déclaration d’experts sur l’évaluation des lésions hépatiques focales dans le foie non cirrhotique.1 Elle décrit une procédure pertinente permettant d’éviter le surdiagnostic. Une lésion hépatique focale est souvent détectée de manière fortuite et la question se pose de savoir s’il s’agit d’une lésion pertinente, a expliqué D. Semela. La bonne nouvelle est que la plupart des lésions sont bénignes, par exemple un kyste ou un hémangiome. Dans ce cas, aucune évaluation n’est nécessaire.1
Les autres lésions hépatiques focales bénignes sont les zones de stéatose et d’épargne stéatosique focales. Selon D. Semela, environ un quart de la population suisse souffre de stéatose hépatique. Sa distribution n’est pas toujours homogène dans le parenchyme. Par exemple, une zone d’épargne stéatosique peut se présenter sous forme de foyer rond à l’échographie. L’hyperplasie nodulaire focale (HNF), également bénigne, est une modification très rare.1
Bénigne, mais pas sans danger
L’adénome hépatocellulaire, qui est globalement très rare et que l’on observe souvent chez les jeunes femmes sous contraception orale, est plus dangereux, mais n’est pas encore malin. Il doit être évalué par des spécialistes, a souligné D.Semela. Il doit toujours être retiré chez l’homme, car il existe un risque élevé qu’il progresse vers un cancer du foie.
L’échinococcose est une infection pertinente. L’expert a expliqué que la Suisse était une zone d’endémie de l’Echinococcus multilocularis, l’un des parasites responsables de l’infection. Bien que l’échinococcose ne soit pas une tumeur, elle se comporte comme telle en infiltrant le foie et d’autres organes. Si elle n’est pas diagnostiquée ni traitée à temps, elle présente un pronostic très défavorable, selon D. Semela.
L’abcès du foie est également dangereux et touche principalement les patient·es sous immunosuppression, très âgé·es ou souffrant de bactériémie.
Tumeurs hépatiques malignes
Outre les tumeurs hépatiques primitives comme le carcinome hépatocellulaire (CHC), le cholangiocarcinome (CCA) et l’angiosarcome extrêmement rare, le foie est souvent le lieu de métastases d’autres tumeurs.1
Diagnostic par imagerie
L’imagerie, en premier lieu l’échographie, si nécessaire avec produit de contraste («contrast-enhanced ultrasound», CEUS), aide à évaluer une lésion focale. En cas de tomodensitométrie (TDM), il convient de procéder à une TDM en quatre phases, le cas échéant. Elle se compose de la phase pré-contraste, suivie de la phase artérielle, de la phase veineuse portale et de la phase veineuse tardive.1 Elle permet une différenciation très précise des lésions. Enfin, une imagerie par résonance magnétique (IRM) peut également être réalisée. En combinaison avec un produit de contraste qui se diffuse dans les hépatocytes et les voies biliaires après 20 à 30 minutes, il est possible de poser un diagnostic plus différencié des lésions hépatiques, a déclaré l’expert.
«Red Flags» d’une tumeur maligne potentielle
Cirrhose du foie ou hépatopathie chronique
Taux élevés des marqueurs tumoraux (AFP, ACE, CA 19-9)
Antécédents personnels de tumeur maligne
Antécédents familiaux de tumeur maligne
Symptômes B
Lésion hépatique nouvelle ou dont la taille progresse
Âge >40 ans
Le comportement du produit de contraste dans les lésions hépatiques est souvent diagnostique, par exemple dans le cas de ce que l’on appelle un «wash out» en phase veineuse, a-t-il expliqué. Dans ce cas, le produit de contraste absorbé par la lésion est éliminé plus rapidement que par le reste du foie. Ce comportement amène toujours à une forte suspicion de tumeur maligne. Il peut s’agir d’une métastase, d’un CHC ou d’un CCA, explique D. Semela.
Il a toutefois averti qu’on observe de plus en plus d’effets secondaires sous le produit de contraste utilisé en Suisse depuis 2021, notamment des chocs anaphylactiques d’issue parfois fatale.2,3 On étudie actuellement un lien possible avec les vaccins contre la Covid-19, car le produit de contraste et les vaccins à ARNm contiennent tous deux du polyéthylène glycol. Une réactivité croisée est alors possible chez certain·es patient·es et il faut s’y préparer, notamment en disposant d’une trousse d’urgence pour anaphylaxie avec auto-injecteur d’adrénaline et d’un personnel formé, a déclaré D. Semela.
Autres options de diagnostic
En cas de suspicion de tumeur, le dosage des marqueurs tumoraux donne de précieuses indications: alpha-fœtoprotéine (AFP) en cas de CHC, antigène carcinoembryonnaire (ACE) en cas de métastases hépatiques et CA 19-9 plus ACE en cas de CCA.1
On dispose d’examens sérologiques spécifiques pour exclure une échinococcose. Fièvre, sueurs nocturnes, leucocytose et augmentation de la protéine C-réactive (CRP) indiquent un abcès du foie.1
Si une lésion ne peut pas être évaluée avec certitude ou si sa position est centrale, il convient alors de réaliser une biopsie hépatique du foyer rond et de l’examiner histologiquement.1 «C’est un bon instrument entre des mains expérimentées. Il existe bien sûr un certain risque de saignement et aussi de propagation de cellules tumorales. Je recommande de réaliser une biopsie hépatique du foyer rond avec une aiguille, en évitant de toucher la lésion et en obturant ensuite le canal de ponction avec une éponge hémostatique»», a déclaré D. Semela.4 Selon lui, il est possible de réaliser une biopsie de très petites lésions, même en dessous d’un centimètre, de manière sûre et précise sous guidage échographique.4
De manière générale, l’évaluation des lésions hépatiques focales doit toujours se faire dans un contexte clinique. Les principaux signaux d’alerte sont énumérés dans l’encadré ci-dessus.1
Carcinome hépatocellulaire (CHC)
La cirrhose du foie et les hépatopathies chroniques sont des facteurs de risque de survenue d’un CCA ou d’un CHC. Le CHC est la sixième tumeur maligne la plus fréquente dans le monde, avec une incidence croissante, et la troisième cause de décès par cancer. S’il est diagnostiqué à un stade précoce, le CHC peut être traité de manière curative, avec un taux de survie à 5 ans >70%, a déclaré D. Semela. À un stade avancé, la survie moyenne est cependant inférieure à deux ans.
Selon l’Organe national d’enregistrement du cancer (ONEC), près de 1000 personnes ont été nouvellement diagnostiquées d’un CHC en Suisse en 2020 et plus de 720 en sont décédées, ce qui signifie que le cancer a été détecté à un stade avancé et qu’il n’y avait plus d’options curatives. C’est pourquoi le dépistage du CHC ou la détection précoce sont essentiels, a souligné l’expert.
Les principaux facteurs déclenchants d’un CHC sont la forte consommation d’alcool, le syndrome métabolique, les hépatites B et C. La nicotine et les troubles métaboliques comme l’hémochromatose favorisent également le CHC.5
Dépistage du CHC: pour qui et quelle méthode?
Les patient·es atteint·es de fibrose hépatique n’ont pas tou·tes besoin d’effectuer un dépistage du CHC, a déclaré D. Semela. Cela est particulièrement important pour les patient·es présentant un stade de fibrose F3, c’est-à-dire le stade précédant la cirrhose, et en cas de cirrhose du foie.6,7 L’expert a mentionné le cas particulier de l’hépatite B chronique, qui peut déclencher un CHC, même à un stade précoce de cirrhose.
Alors que le dépistage comprend un seul examen, la surveillance consiste en des contrôles répétés des patient·es. Les directives courantes recommandent à cet effet une échographie hépatique tous les six mois. En Suisse, il est en outre conseillé de doser l’AFP tous les six mois.6,7
L’hépatite C ayant été presque entièrement éliminée et la maladie hépatique stéatosique associée à un dysfonctionnement métabolique (MASLD) étant en augmentation dans le cadre du syndrome métabolique, la stratégie de surveillance a changé: il est plus difficile de réaliser une échographie chez les patient·es souffrant d’obésité et, par conséquent, le nombre de CHC non détectés au stade précoce a augmenté, a expliqué D. Semela. En cas de mauvaise visibilité à l’échographie, il convient d’avoir recours à une TDM ou une IRM. Il a souligné que le seul dosage de l’AFP ne suffisait pas, car environ la moitié des patient·es atteint·es de CHC présentent un taux d’AFP normal. Même si le taux dépasse la valeur normale, il faut procéder à une imagerie en coupes.
Surveillance du CHC dans des cas particuliers
Hépatite B chronique
Le virus de l’hépatite B peut également entraîner un CHC en l’absence de cirrhose. Un outil simple, le score PAGE-B, peut aider à évaluer le risque de CHC. Des points sont attribués et additionnés sur la base du nombre de thrombocytes/mm3, de l’âge et du sexe. Le score total va de 0 (risque extrêmement faible) à 25 (risque extrêmement élevé), sachant que l’incidence cumulée d’un CHC à 5 ans est de 4% avec un score de 10–17 et atteint déjà 16% avec un score >18.8 La quintessence est que toutes les personnes ayant un score PAGE-B >10 doivent être incluses dans un programme de dépistage du CHC, selon D. Semela.
Hépatite C guérie
L’hépatite C peut aujourd’hui être traitée avec succès. «La question est la suivante: est-ce que tout va bien désormais? Les patient·es sont-il·elles tiré·es d’affaire en ce qui concerne le CHC? Pas tout à fait», a répond D. Semela. Les patient·es qui présentaient une fibrose avancée (stade F3) ou une cirrhose avant le traitement doivent rester dans le programme de dépistage des années après l’élimination avec succès de l’hépatite C, car il·elles continuent à présenter un risque accru. Cela signifie que le stade de fibrose doit être évalué par élastographie ou biopsie hépatique avant le début du traitement, explique-t-il. En outre, tou·tes les patient·es guéri·es d’une hépatite C sans fibrose avancée, mais qui ont une consommation excessive d’alcool ou souffrent de MASLD, doivent être régulièrement examiné·es, car la fibrose peut évoluer et entraîner un risque accru de CHC.9
Maladie hépatique stéatosique associée à un dysfonctionnement métabolique (MASLD)
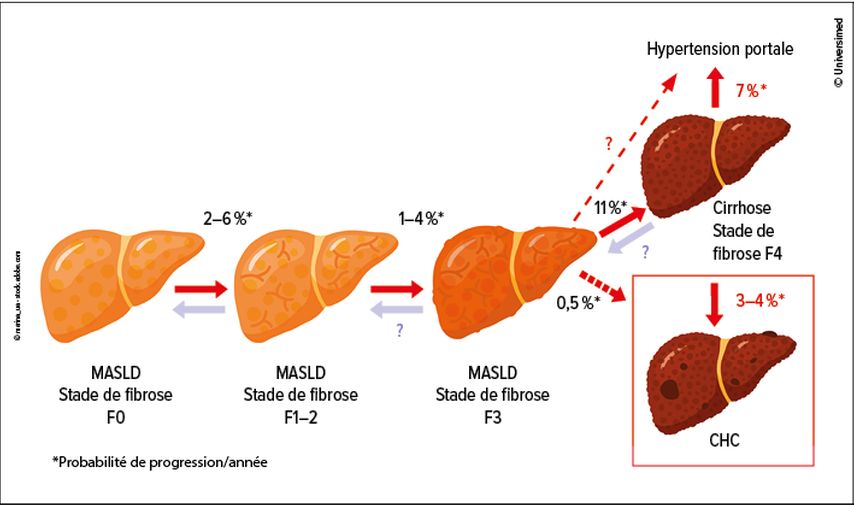
Environ 25% de la population générale est atteinte de stéatose ou de MASLD, 65% des patient·es atteint·es de diabète de type 2 et 80% des personnes souffrant d’obésité.10 En Suisse, selon l’Office fédéral de la santé publique (OFSP), plus de 50% des hommes et 33% des femmes sont en surpoids ou souffrent d’obésité et sont donc concerné·es.11 Tou·tes ne développent cependant pas un CHC. Ce sont surtout les personnes atteintes de fibrose de haut grade qui courent un risque (Fig.1)12, et il convient de les identifier. Un dépistage non invasif en deux étapes est approprié à cet effet. La première étape consiste à calculer le score FIB-4 sur la base de l’âge, des taux de transaminases et du nombre de thrombocytes. S’il est <1,3, la deuxième étape doit consister en un examen plus approfondi, par exemple une élastographie hépatique.13
Fig.1: Progression des hépatopathies chroniques (p.ex. MASLD) jusqu’au stade terminal avec cirrhose et carcinome hépatocellulaire (CHC)
L’échographie hépatique seule permet de détecter moins de 50% des CHC à un stade précoce, tandis que la combinaison avec le dosage de l’AFP permet d’en détecter environ 63%, a expliqué D. Semela. L’IRM avec produit de contraste a la plus grande sensibilité, avec près de 90%. En raison des coûts élevés, elle ne peut pas être réalisée chez tou·tes les patient·es, a-t-il précisé. Elle est cependant pertinente chez les patient·es à haut risque atteint·es de cirrhose, d’hépatite virale non guérie ou ayant une consommation excessive d’alcool.14 Une autre possibilité est d’utiliser un protocole d’IRM abrégé, par exemple sans produit de contraste. À l’Université de Lausanne, on étudie actuellement le protocole consistant à injecter le produit de contraste, mais à ne commencer l’examen IRM qu’après 20 à 30 minutes, c’est-à-dire dans la phase tardive.15
Enfin, des recherches sont en cours sur des biomarqueurs autres que l’AFP, a déclaré D. Semela. Le score GA(L)AD est en cours d’autorisation et sera probablement bientôt disponible en Suisse. L’acronyme désigne le sexe, l’âge, (L3-AFP), l’AFP et la DCP (des-gamma-carboxyprothrombine = marqueur tumoral PIVKA II).16
Options thérapeutiques dans le CHC
En principe, les patient·es atteint·es de CHC doivent être évalué·es dans le cadre d’un «tumor board» interdisciplinaire, a déclaré D. Semela. La décision thérapeutique repose sur le stade de la tumeur: alors qu’un traitement curatif est possible au stade précoce, des traitements palliatifs sont la référence au stade avancé. La fonction hépatique doit également être prise en compte. Au stade de cirrhose décompensée (Child-Pugh C), aucun traitement du CHC ne doit être initié, car tout traitement aggrave davantage la fonction hépatique.7
Interventions chirurgicales
Au stade précoce (1 tumeur ≤5cm ou 3 tumeurs ≤3cm, limitée·s au foie, sans invasion vasculaire), un traitement curatif est possible, par exemple par ablation percutanée par micro-ondes (MWA). Les lésions de taille plus importante doivent être réséquées.7 Cela est difficile chez les patient·es atteint·es de cirrhose, car on observe souvent une décompensation par la suite, a déclaré D. Semela. La transplantation hépatique constitue le dernier recours. Cependant, il y a plus de patient·es que d’organes disponibles. Selon le rapport annuel 2023 de Swisstransplant, 492 personnes étaient en attente d’un foie en Suisse, 146 d’entre elles ont reçu un nouvel organe, 48 sont décédées parce qu’aucun organe n’était disponible.17 «Cela représente un·e patient·e par semaine qui attend et qui ne reçoit pas d’organe«, a souligné D. Semela.
Traitements palliatifs
Les options de traitement palliatif permettent de prolonger la vie, mais visent seulement à soulager les patient·es, a-t-il ajouté. L’embolisation intra-artérielle (TAE) est une méthode mini-invasive. Il s’agit d’introduire un cathéter par voie inguinale, de le pousser jusqu’à la lésion et d’injecter ensuite un agent embolique qui oblitère les vaisseaux vascularisant la tumeur. La TAE peut être associée à une chimiothérapie (TACE) ou à un émetteur bêta (TARE/SIRT).7
Des traitements systémiques palliatifs sont en outre disponibles. Depuis 2021, les immunothérapies par atézolizumab/bévacizumab et trémélimumab/durvalumab sont autorisées en Suisse. Les inhibiteurs de tyrosine kinase (ITK) tels que le sorafénib et le lenvatinib existent déjà depuis 20086, mais ils sont désormais relégués au second plan en termes de survie globale en raison de la supériorité des immunothérapies, a conclu D. Semela.
Source:
FOMF, Médecine interne Update Refresher, le 4 décembre 2024, à Zurich
Littérature:
1 Sawatzki M et al.: Swiss Med Wkly 2023; 153: 40099 2WHO: www.vigiaccess.org 3 FAERS Database: www.fda.gov/drugs/fdas-adverse-event-reporting-system-faers/fda-adverse-event-reporting-system-faers-public-dashboard 4 Müller S et al.: Swiss Med Wkly 2023; 153(Suppl. 272): 5 5 Krebsinformationsdienst, DKFZ: www.krebsinformationsdienst.de/leberkrebs#c33646 Goossens N et al.: Swiss Med Wkly 2020; 150: w20296 7 EASL Clinical Practice Guidelines on the management of hepatocellular carcinoma. J Hepatol 2025; 82: 315-74 8 Papatheodoridis G et al.: J Hepatol 2016; 64: 800-6 9 Bobzin C et al.: Swiss Medical Forum – Schweizerisches Medizin-Forum 2021; 21: 184-6 10 Francque SM et al.: JHEP Rep 2021; 3: 100322 11 www.bag.admin.ch/dam/bag/de/dokumente/npp/forschungsberichte/forschungsberichte-e-und-b/schlussbericht-menuch-chuv.pdf.download.pdf/MenuCH1_Report_March2017.pdf 12 Sanyal AJ et al.: N Engl J Med 2021; 385: 1559-69 13 EASL-EASD-EASO Clinical Practice Guidelines on the management of metabolic dysfunction-associated steatotic liver disease (MASLD). J Hepatol 2024; 81: 492-542 14 Singal AG et al.: J Hepatol. 2023; 79: 226-39 15 Ringe KI et al.: J Magn Reson Imaging 2024; 59: 58-69 16 Marsh TL et al.: Gastroenterology 2025; 168: 316-26.e6 17 Swisstransplant Jahresbericht 2023 ( www.swisstransplant.org )
Das könnte Sie auch interessieren:
BPCO: identification de patients non diagnostiqués
De nombreuses personnes atteintes de BPCO et/ou d’asthme n’ont jamais été diagnostiquées et ne sont donc pas traitées. Plusieurs études publiées ces derniers mois se penchent sur ce ...
Diarrhée chronique: déroulement de l’examen
La diarrhée chronique est le symptôme de différentes maladies. Le Pr Alain Schoepfer a expliqué comment rechercher au mieux le facteur déclenchant dans son exposé lors du congrès annuel ...
Réduction, voire arrêt des corticoïdes grâce à la biothérapie?
Les corticoïdes oraux constituent le traitement de référence des exacerbations de l’asthme et sont également utilisés pour celles de la BPCO. Cette norme s’appuie toutefois sur des ...