Neue endokrine Targets in der post-menopausalen Osteoporosetherapie
Autorin:
Dr. Laura Handgriff
Fachärztin für Innere Medizin, Endokrinologie und Diabetologie
Medizinische Abteilung, Klinik Landstraße (Diabetologie, Endokrinologie und Nephrologie)
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die postmenopausale Osteoporose ist eine häufige, jedoch oft unterschätzte endokrine Erkrankung mit erheblicher klinischer Relevanz. Neben klassischen antiresorptiven Therapien stehen heute innovative osteoanabole Behandlungsansätze zur Verfügung, die gezielt den Knochenaufbau stimulieren. Insbesondere bei Patientinnen mit hohem Frakturrisiko eröffnen diese Therapien neue Möglichkeiten zur effektiven Frakturprävention.
Postmenopausale Osteoporose – eine unterschätzte endokrine Erkrankung
Klinische Bedeutung
Die Osteoporose, insbesondere die postmenopausale Form, zählt zu den häufigsten systemischen Stoffwechselerkrankungen des Skeletts. Charakteristisch sind eine Abnahme der Knochenmineraldichte und -masse sowie eine Störung der Knochenmikroarchitektur, was zu erhöhter Knochenfragilität und gesteigertem Frakturrisiko führt. Zur primären Osteoporose zählen die postmenopausale Osteoporose (Typ I), die senile Osteoporose (Typ II) sowie seltene idiopathische Formen im Jugendalter.1 Mit zunehmendem Lebensalter steigt die Prävalenz deutlich an; Prognosen zufolge wird der Anteil der Weltbevölkerung über 65 Jahre bis 2050 auf etwa 16% anwachsen, mit einer geschätzten Zahl von über 220 Millionen Betroffenen weltweit.2
Als Fragilitätsfraktur gilt eine Fraktur infolge eines inadäquaten Traumas, typischerweise nach einem Sturz aus dem Stand oder aus geringer Höhe. Sie definiert unabhängig vom T-Score eine manifeste Osteoporose und stellt den stärksten Prädiktor für weitere Frakturen dar.3,4
Die Weltgesundheitsorganisation definiert Osteoporose densitometrisch anhand eines T-Scores ≤−2,5. Die klinische Bedeutung reicht jedoch weit über diese Definition hinaus, da osteoporotische Frakturen mit erhöhter Morbidität, Mortalität und erheblicher sozioökonomischer Belastung assoziiert sind.3,5
Der menopausale Übergang ist mit einer beschleunigten Knochenresorption verbunden, die die Kapazität der Knochenneubildung übersteigt. In den ersten fünf bis zehn Jahren nach der Menopause beträgt der jährliche Knochenverlust etwa 2–3%, verglichen mit 0,5–1% im altersassoziierten Verlauf. Diese Phase betrifft vor allem trabekulären Knochen und erklärt das frühe Auftreten vertebraler Frakturen.6
Weltweit ereignen sich jährlich rund neun Millionen osteoporotische Frakturen. Hüftfrakturen sind mit einer Einjahresmortalität von etwa 20% und hoher funktioneller Einschränkung verbunden. Auch klinisch stumme Wirbelkörperfrakturen sind prognostisch relevant, da sie das Risiko weiterer Frakturen – insbesondere in den ersten zwei Jahren – deutlich erhöhen.3,6–8 Trotz wirksamer diagnostischer und therapeutischer Optionen bleibt die Osteoporose häufig unterdiagnostiziert und untertherapiert. Weniger als 20% der Hochrisikopatientinnen erhalten nach einer Fragilitätsfraktur eine adäquate Therapie. Ursachen sind unzureichendes Screening, unterschätzte prognostische Relevanz von Frakturen, Sicherheitsbedenken und fragmentierte Versorgung.9
Pathophysiologie in der Menopause
Östrogene regulieren den Knochenstoffwechsel über direkte Effekte auf Osteoblasten, Osteoklasten und Osteozyten. Der postmenopausale Östrogenentzug stört das Gleichgewicht zwischen Knochenaufbau und -abbau nachhaltig.10
Zentral ist die Verschiebung der RANKL-OPG-Achse. Der Receptor Activator of Nuclear Factor KB Ligand (RANKL) stimuliert die Osteoklastenbildung. Unter Östrogeneinfluss wird RANKL gehemmt und Osteoprotegerin (OPG) gefördert. Nach der Menopause steigt das RANKL-OPG-Verhältnis, was Osteoklastenaktivität und Knochenresorption verstärkt.11
Zusätzlich entsteht ein proinflammatorisches Knochenmarkmilieu mit erhöhter Produktion von Interleukin 1, 6 und 7, TNF-α und M-CSF, die die Osteoklastogenese weiter fördern.12 Altersbedingte Veränderungen des Kalzium- und Vitamin-D-Stoffwechsels begünstigen zudem einen sekundären Hyperparathyreoidismus.13
Osteozyten, die den Knochenumbau koordinieren, unterliegen postmenopausal einer erhöhten Apoptose. Die gesteigerte Sklerostinexpression hemmt zusätzlich den Wnt-Signalweg und damit die osteoblastäre Knochenneubildung.14,15 Der Knochenverlust verläuft biphasisch: initial beschleunigt, später durch altersabhängige Faktoren mit zunehmender kortikaler Ausdünnung und steigendem Hüftfrakturrisiko.16,17 Genetische Faktoren erklären 50–85% der Variabilität der maximalen Knochenmasse.18
Klinische und diagnostische Evaluation
Die Diagnostik basiert auf klinischen Risikofaktoren, Knochendichtemessung, Frakturerfassung und dem Ausschluss sekundärer Ursachen (Tab.1). Zu den wichtigsten Risikofaktoren zählen höheres Lebensalter, vorausgegangene Fragilitätsfraktur, familiäre Hüftfrakturanamnese, Glukokortikoidtherapie, entzündlich-rheumatische Erkrankungen, Rauchen und Alkoholkonsum.19
Sekundäre Ursachen sollten insbesondere bei unerwartet niedriger Knochendichte, Frakturen vor dem 60. Lebensjahr oder Z-Scores ≤−2,0 ausgeschlossen werden.20 Die klinische Untersuchung umfasst serielle Größenmessungen; ein Größenverlust >2cm im Verlauf oder >4cm anamnestisch weist auf okkulte Wirbelfrakturen hin.21 Basislaboruntersuchungen dienen dem Ausschluss sekundärer Ursachen und der Therapiekontrolle.22
Das FRAX-Tool schätzt das Zehnjahres-Frakturrisiko, berücksichtigt jedoch weder die LWS-Knochendichte noch das imminente Risiko nach frischer Fraktur. Klinisch relevant ist, dass viele Patientinnen trotz osteopenischer T-Scores bereits Fragilitätsfrakturen erlitten haben und definitionsgemäß eine manifeste Osteoporose aufweisen. Therapieentscheidungen sollten daher immer klinisch integriert erfolgen.23–25
Therapieindikation und Risikostratifizierung
Eine medikamentöse Therapie ist indiziert bei T-Score ≤−2,5, bei osteopenischen Werten mit Fragilitätsfraktur oder bei erhöhtem FRAX-Risiko. Unabhängig davon ist eine systematische Sturzrisikobeurteilung essenziell, da über 90% der Hüftfrakturen sturzbedingt auftreten.
Bei hohem Frakturrisiko stellen Bisphosphonate weiterhin eine geeignete Erstlinientherapie dar. Bei sehr hohem oder imminentem Frakturrisiko – etwa nach kürzlich erlittener Fraktur, bei sehr niedriger Knochendichte oder Frakturen unter Therapie – profitieren Patientinnen besonders von einem initial osteoanabolen Therapieansatz.26–29
Pharmakologische Therapieoptionen
Menopausale Hormontherapie und SERMs
Östrogene besitzen ausgeprägte antiresorptive Effekte und können das Frakturrisiko senken. Der routinemäßige Einsatz der menopausalen Hormontherapie ist jedoch aufgrund potenzieller kardiovaskulärer und onkologischer Risiken limitiert. Heute wird sie primär bei jüngeren postmenopausalen Frauen mit klimakterischen Beschwerden eingesetzt, wenn nichtöstrogene Alternativen nicht geeignet sind.30–35
Selektive Estrogenrezeptor-Modulatoren (SERMs) wie Raloxifen oder Bazedoxifen reduzieren vor allem vertebrale Frakturen, zeigen jedoch keinen konsistenten Effekt auf Hüft- oder nichtvertebrale Frakturen. Insgesamt spielen die HRT und SERMs in der modernen Osteoporosetherapie jedoch eine nachgeordnete Rolle und sind insbesondere bei Patientinnen mit hohem oder sehr hohem Frakturrisiko den wirksameren antiresorptiven oder osteoanabolen Therapien unterlegen und nicht als primäre spezifische Therapie der postmenopausalen Osteoporose geeignet.35–38
Bisphosphonate und Denosumab
Bisphosphonate bilden seit Jahrzehnten eine tragende Säule der Osteoporosetherapie und zeichnen sich durch gute Wirksamkeit, breite Verfügbarkeit und Kosteneffektivität aus. Große randomisierte Studien und Metaanalysen belegen eine signifikante Reduktion vertebraler Frakturen sowie – abhängig von Substanz und Applikationsform – auch nichtvertebraler und hüftnaher Frakturen. Für Alendronat, Risedronat und Zoledronat liegt eine robuste Evidenz zur Reduktion von vertebralen, nichtvertebralen und Hüftfrakturen vor. Ibandronat hingegen zeigt eine gesicherte Wirksamkeit ausschließlich bei vertebralen Frakturen, ohne konsistenten Nachweis einer Reduktion von Hüft- oder anderen nichtvertebralen Frakturen, und ist daher bei Patientinnen mit erhöhtem Hüftfrakturrisiko nur eingeschränkt geeignet.39
Limitiert wird der Einsatz oraler Bisphosphonate durch gastrointestinale Nebenwirkungen sowie eine oft eingeschränkte Therapieadhärenz bei wöchentlicher Einnahme. In diesen Fällen stellt intravenöses Zoledronat (5mg i.v. einmal jährlich) eine effektive Alternative dar. Aufgrund der renalen Elimination sollten Bisphosphonate bei eingeschränkter Nierenfunktion mit einer glomerulären Filtrationsrate (eGFR) unter 30–35ml/min nicht eingesetzt werden, da ein Risiko der Akkumulation und potenzieller Nephrotoxizität besteht.40,41
Denosumab (Gabe s.c. alle 6 Monate) stellt eine potente alternative antiresorptive Therapie dar, insbesondere bei Patientinnen mit eingeschränkter Nierenfunktion oder fehlender Adhärenz für orale Therapien. Es reduziert vertebrale, nichtvertebrale und Hüftfrakturen effektiv.42 Limitiert wird der Einsatz durch den Rebound-Effekt nach Absetzen mit raschem Knochenverlust und erhöhtem Frakturrisiko, weshalb eine konsequente antiresorptive Anschlussbehandlung (z.B. mit Zoledronat) zwingend erforderlich ist.42
Zusammenfassend sind antiresorptive Therapien wirksam zur Frakturprävention und für viele Patientinnen mit hohem Frakturrisiko geeignet. Ihre Limitation besteht jedoch darin, dass sie primär den Knochenabbau hemmen, ohne die geschädigte Knochenmikroarchitektur aktiv wiederherzustellen. Insbesondere bei Patientinnen mit sehr hohem oder imminentem Frakturrisiko kann dies unzureichend sein und den Bedarf an initial osteoanabolen Therapiestrategien begründen.26,27
Osteoanabole Therapie: „new players on the block“
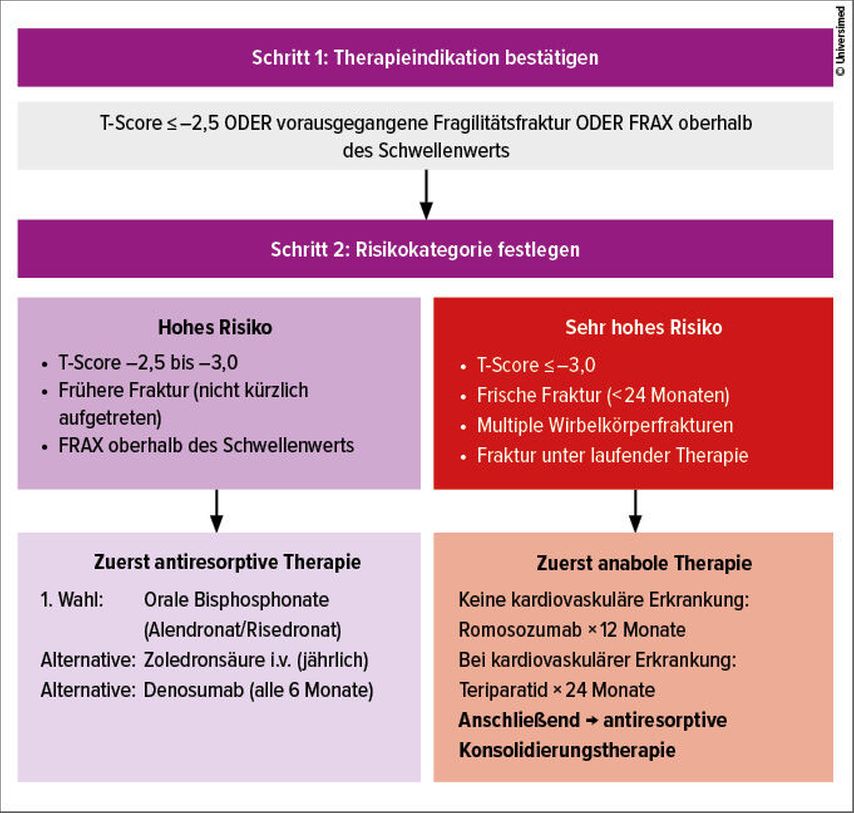
Osteoanabole Therapien markieren einen wesentlichen Fortschritt in der Osteoporosetherapie, da sie gezielt den Knochenaufbau stimulieren und nicht nur den Knochenabbau hemmen. Sie ermöglichen einen raschen Zugewinn an Knochenmasse und -qualität und sind insbesondere für Patientinnen mit sehr hohem oder imminentem Frakturrisiko von klinischer Bedeutung, bei denen antiresorptive Therapien allein häufig nicht ausreichen.28,29 Die Früherkennung dieses Patientenkollektivs ist essenziell, um die korrekte Therapie zu etablieren (Abb. 1).
Abb. 1: Risikoadaptierter Therapiealgorithmus bei Osteoporose (modifiziert nach Ena G und Soyfoo M)61
Parathormonbasierte Osteoanabolika
Teriparatid (20µg/Tag s.c.) ist ein rekombinantes Analogon des Parathormons (PTH 1–34) und wirkt osteoanabol über eine überwiegend Remodeling-basierte Stimulation der Knochenformation.43 Bereits innerhalb des ersten Therapiemonats kommt es zu einer deutlichen Aktivierung der Osteoblasten, gefolgt von einer moderaten Zunahme der Knochenresorption nach drei bis sechs Monaten. Während des anabolen Fensters von etwa 18 Monaten überwiegt die Knochenformation, sodass ein relevanter Anteil der Knochendichtezunahme frühzeitig erreicht wird. Spätere Dichtegewinne resultieren vor allem aus der Mineralisierung neu gebildeten Knochens.44–46
Klinisch zeigen parathormonbasierte Therapien eine stärkere Frakturreduktion als antiresorptive Substanzen, insbesondere bei Patientinnen mit schwerer Osteoporose oder bereits stattgehabten Fragilitätsfrakturen.17,47 Die empfohlene Therapiedauer beträgt 18–24 Monate. Danach ist eine antiresorptive Anschlussbehandlung zwingend erforderlich, um den Verlust der neu gebildeten Knochenmasse zu verhindern.46,51–53 Teriparatid ist insbesondere bei glukokortikoidinduzierter Osteoporose von großer Bedeutung, da hier auch bei längerer Anwendung anhaltende Zuwächse der Knochenmineraldichte beobachtet werden.48–50
Romosozumab
Romosozumab (210µg s.c. einmal monatlich über 12 Monate) ist ein monoklonaler Antikörper gegen Sklerostin und stellt ein neues endokrines Target in der Osteoporosetherapie dar. Durch die Inhibition von Sklerostin wird der Wnt-Signalweg aktiviert, was zu einer ausgeprägten osteoblastären Aktivierung führt. Gleichzeitig wird die RANKL-Expression reduziert, sodass Romosozumab neben seinem starken osteoanabolen auch einen moderaten antiresorptiven Effekt entfaltet.54,55
Charakteristisch ist der sehr rasche Wirkungseintritt: Knochenformationsmarker steigen innerhalb weniger Wochen deutlich an, während die Knochenresorption über die gesamte Therapiedauer supprimiert bleibt. Klinische Studien zeigen eine signifikante Reduktion von vertebralen, nichtvertebralen und Hüftfrakturen bereits innerhalb der ersten sechs Monate. Im direkten Vergleich zu Teriparatid erzielt Romosozumab stärkere Zuwächse der Knochenmineraldichte, insbesondere im kortikalen Knochen, was für die Prävention von Hüftfrakturen von besonderer Relevanz ist.54,56
Aufgrund der zeitlich begrenzten osteoanabolen Wirkung und des raschen Abfalls der Knochendichte nach Absetzen ist auch bei Romosozumab eine anschließende antiresorptive Konsolidierungstherapie obligat.57 Nach der ARCH-Studie wurden Sicherheitsbedenken hinsichtlich eines möglichen erhöhten Risikos kardiovaskulärer Ereignisse diskutiert. Dieses Signal zeigte sich jedoch nicht konsistent über alle Studien hinweg und wurde weder in der placebokontrollierten FRAME-Studie noch in weiteren Untersuchungen eindeutig bestätigt. Bis zur weiteren Klärung wird empfohlen, Romosozumab nicht bei Patientinnen mit kürzlich stattgehabtem Myokardinfarkt oder Schlaganfall beziehungsweise sehr hohem kardiovaskulärem Risiko einzusetzen.54,56,58,59
Unter Berücksichtigung der verfügbaren Evidenz stellt Romosozumab bei postmenopausalen Frauen mit sehr hohem oder imminentem Frakturrisiko heute die bevorzugte osteoanabole Erstlinientherapie dar.54–56
Im Gegensatz zur glukokortikoidinduzierten Osteoporose, bei der Teriparatid weiterhin eine zentrale Rolle spielt, spricht das Wirkprofil von Romosozumab – insbesondere die ausgeprägte und rasche Frakturreduktion auch an der Hüfte – für seinen primären Einsatz in der postmenopausalen Hochrisikopopulation.54–56
Zusammenfassung
Die postmenopausale Osteoporose erfordert ein frühzeitiges Screening, eine klinisch orientierte Risikostratifizierung und eine konsequente Therapie. Während antiresorptive Therapien bei hohem Frakturrisiko weiterhin wirksam sind, profitieren Patientinnen mit sehr hohem oder imminentem Frakturrisiko von einem frühzeitigen osteoanabolen Therapieansatz. Der gezielte Einsatz moderner osteoanaboler Therapien stellt einen entscheidenden Fortschritt dar, um Frakturen effektiv zu verhindern und die Lebensqualität postmenopausaler Frauen nachhaltig zu verbessern.
Literatur:
1 Ena G et al.: Front Pharmacol 2024; 15: 1456796 2 Mukherjee D, Chattopadhyay N: J Endocrinol Invest 2016; 39(10): 1129-44 3 Kanis JA et al.: J Clin Endocrinol Metab 2001; 86(12): 5503-10 4 Hernlund E et al.: Arch Osteoporos 2013; 8(1): 136 7 Johansson H et al.: Osteoporos Int 2017 5 Johnell O, Kanis JA: Osteoporos Int 2006; 17(12): 1726-33 6 Riggs BL et al.: J Bone Miner Res 2002; 17(1): 14-24 7 Johansson H et al.: Osteoporos Int 2017; 28: 775-80 8 Kannegaard PN et al.: Age Ageing 2010; 39(2): 203-9 9 Solomon DH et al.: J Bone Miner Res 2014; 29: 1929-37 10 Khosla S, Monroe DG: Cold Spring Harb Perspect Med 2018; 8(1): a031211 11 Manolagas SC: Endocr Rev 2010; 31(3): 266-300 12 Weitzmann MN, Pacifici R: J Clin Invest 2006; 116(5): 1186-94 13 Corbetta S: Front Horm Res 2019; 51: 23-39 14 Pacifici R: Ann N Y Acad Sci 2016; 1364(1): 11-24 15 Robling AG, Bonewald LF: Annu Rev Physiol 2020; 82: 485-506 16 Riggs BL et al.: Endocr Rev 2002; 23(3): 279-302 17 Tella SH, Gallagher JC: J Steroid Biochem Mol Biol 2014; 142: 155-70 18 Delgado-Calle J, Riancho JA: Biology 2012; 1(3): 698-713 19 Kanis JA et al.: Arch Osteoporos 2018; 13(1): 118 20 Mirza F, Canalis E: Eur J Endocrinol 2015; 173(3): R131-51 21 Cosman F et al.: Osteoporos Int 2014; 25: 2359-81 22 Harvey NC et al.: Bone 2015; 78: 216-24 23 Kanis JA et al.: J Clin Densitom 2017; 20: 360-7 24 Silva BC et al.: J Bone Miner Res 2014; 29: 518-30 25 US Preventive Services Task Force: JAMA 2018; 319: 2521-31 26 Kanis JA et al.: Osteoporos Int 2020; 31: 1-12 27 Johansson H et al.: Osteoporos Int 2017; 28: 775-80 28 Shoback D et al.: J Clin Endocrinol Metab 2020; 105: 587-94 29 Cosman F et al.: N Engl J Med 2016; 375: 1532-43 30 Rossouw JE et al.: JAMA 2002; 288: 321-33 31 Zhou J et al.: Maturitas 2013; 76: 129-33 32 Hodis HN et al.: N Engl J Med 2016; 374: 1221-31 33 Schierbeck LL et al.: BMJ 2012; 345: e6409 34 Salpeter SR et al.: J Gen Intern Med 2004; 19(7): 791-804 35 Silverman SL et al.: J Bone Miner Res 2008; 23: 1923-34 36 Cummings SR et al.: JAMA 1999; 281: 2189-97 37 Barrett-Connor E et al.: N Engl J Med 2006; 355: 125-37 38 Cummings SR et al.: JAMA 1998; 280: 2077-82 39 Barrionuevo P et al.: J Clin Endocrinol Metab 2019; 104(5): 1623-30 40 Camacho PM et al.: Endocr Pract 2020; 26(Suppl_1): 1-46 41 Shoback D et al.: J Clin Endocrinol Metab 2020; 105: 587-94 42 Bone HG et al.: Lancet Diabetes Endocrinol 2017; 5: 513-23 43 Dempster DW et al.: J Bone Miner Res 2018; 33: 298-306 44 Eastell R et al.: Osteoporos Int 2019; 30: 667-73 45 McClung MR et al.: Arch Intern Med 2005; 165: 1762-8 46 Stepan JJ et al.: Osteoporos Int 2010; 21: 2027-36 47 Miller PD et al.: JAMA 2016; 316: 722-33 48 Neer RM et al.: N Engl J Med 2001; 344: 1434-41 49 Gilsenan A et al.: J Bone Miner Res 2021; 36(2): 244-51 50 Saag KG et al.: Arthritis Rheum 2009; 60: 3346-55 51 Eastell R et al.: J Bone Miner Res 2009; 24: 726-36 52 Bone HG et al.: J Clin Endocrinol Metab 2018; 103(8): 2949-57 53 Black DM et al.: N Engl J Med 2003; 349: 1207-15 54 Saag KG et al.: N Engl J Med 2017; 377: 1417-27 55 McClung MR et al.: J Bone Miner Res 2018; 33: 1397-406 56 Cosman F et al.: N Engl J Med 2016; 375: 1532-43 57 Poole KE et al.: J Bone Miner Res 2022; 37: 256-64 58 Reinhold S, Blankesteijn WM: Arterioscler Thromb Vasc Biol 2019; 39(2): 121-3 59 Go GW: Nutrients 2015; 7: 4453-64 60 Tyson J et al.: Bioengineering (Basel) 2020; 7: 88 61 Ena G, Soyfoo M: J Clin Med 2025; 15(1): 102
Das könnte Sie auch interessieren:
Menopause: Rettung oder Gefahr bei Endometriose?
Die Endometriose wird klassischerweise als östrogenabhängige Erkrankung des reproduktiven Alters betrachtet. Die weitverbreitete Annahme, dass sie mit Eintritt der Menopause verschwindet ...
Resilienz in den Wechseljahren: Strategien gegen Stimmungsschwankungen
Stimmungsschwankungen gehören zu den häufigsten und zugleich am meisten unterschätzten Symptomen der menopausalen Transition. Neben pharmakologischen Therapien gewinnen daher zunehmend ...
Physiotherapie als zentraler Baustein im Behandlungsmanagement
Der Beckenboden spielt in der Menopause eine zentrale Rolle für Kontinenz, Stabilität und Lebensqualität. Hormonelle Veränderungen können zu einer Schwächung der Beckenbodenmuskulatur ...