Hormonelle Veränderungen erkennen und begleiten
Autorin:
Univ.-Prof. Dr. Doris Maria Gruber
Fachärztin für Frauenheilkunde und Gynäkologische Endokrinologie
Wien
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
In Österreich sind rund 56% aller Frauen über 40 Jahre alt, die Menopause tritt im Mittel mit 51,7 Jahren ein. Damit verbringen Frauen etwa ein Drittel ihres Lebens in der Postmenopause. Mit der steigenden Lebenserwartung von Frauen gewinnt das Klimakterium zunehmend an gesundheitspolitischer und klinischer Bedeutung. Diese Lebensphase ist nicht allein durch vasomotorische Symptome gekennzeichnet, sondern stellt ein komplexes endokrinologisches, metabolisches und kardiovaskuläres Umbruchstadium dar.
Derzeit befinden sich etwa 1,2 Millionen Österreicherinnen im Alter zwischen 45 und 64 Jahren im Wechsel. Rund zwei Drittel dieser Frauen berichten über klimakterische Beschwerden, etwa ein Drittel davon über ausgeprägte Symptome, und rund 10% leiden länger als zehn Jahre unter Beschwerden. Diese epidemiologischen Daten unterstreichen, dass die Menopause ein zentrales Versorgungsfeld der gynäkologischen Praxis darstellt.
Chronologie der Menopause
Die hormonellen Veränderungen beginnen häufig bereits Jahre (ca. ab 45 Jahren) vor der finalen Menopause. Durch einen Mangel an Progesteron kann es zu Zyklusunregelmäßigkeiten, Mastalgien, Wassereinlagerungen, Schlafstörungen und Depressionen kommen. Im weiteren Verlauf kommt es zum Östrogenmangel, typischerweise zwischen dem 50. und 55. Lebensjahr, welcher durch vasomotorische Symptome (Hitzewallungen, Schweißausbrüche), Osteoporose und Harninkontinenz gekennzeichnet sein kann. Im höheren Lebensalter kann zusätzlich ein Androgenmangel auftreten, der unter anderem mit Libidoverlust, Fatigue, Adipositas und verminderter Vigilanz assoziiert ist.
Effekte von Östrogen auf die Gefäße
Östrogene wirken direkt auf das kardiovaskuläre System. Östrogenrezeptoren sind in Endothel- und glatten Muskelzellen zahlreicher Gefäßsysteme exprimiert. In vitro zeigen sich vasodilatatorische Effekte durch gesteigerte NO- und Prostazyklinfreisetzung sowie eine Reduktion des arteriellen Tonus über cGMP-abhängige Mechanismen. Zusätzlich wirken Östrogene antiapoptotisch auf Endothelzellen und fördern die angiogenetische Aktivität von Endothelzellen.
In vivo konnte gezeigt werden, dass die Östrogenapplikation vs. Placebo eine signifikante Reduktion neu entstehender atheromatöser Plaques bei oophorektomierten Affen, die mit einer atherogenen Diät gefüttert wurden, zur Folge hatte. Allerdings konnte kein Effekt auf präexistierende Plaques nachgewiesen werden. Dies unterstreicht, dass der Zeitpunkt der Hormongabe entscheidend ist.
Osteoporose – Prävention im „window of opportunity“
Die Osteoporose stellt eine der wichtigsten Langzeitfolgen des postmenopausalen Östrogenmangels dar. Frauen sind etwa viermal häufiger betroffen als Männer. Der maximale Knochenaufbau wird um das 30. Lebensjahr erreicht, danach überwiegt der Knochenabbau. Ursachen der Osteoporose umfassen mangelnde Bewegung, falsche Ernährung, Gewichtsschwankungen, Hormonschwankungen, Medikamente, Nikotin, Störungen im Säure-Basen-Haushalt und maligne Erkrankungen (Krebs, Metastasen).
Besonders ausgeprägt ist der Verlust der Knochenmasse im Alter von ca. 50 Jahren. Diese Zeit stellt daher ein entscheidendes präventives Zeitfenster dar, das sogenannte „window of opportunity“ zur Behandlung menopausaler Beschwerden und Primärprävention der Osteoporose. Ab dem 65. Lebensjahr ist eine präventive Therapie, insbesondere mit Hormonen, meist weniger effektiv. Diagnostisch stehen die Knochendichtemessung sowie das Skelettröntgen im Vordergrund.
Therapeutisch lässt sich die Osteoporose mit ausreichend Bewegung, gesunder Ernährung, Kalzium und Vit. D3, Spurenelementen (Zn, Cu, Mn, Vit. K, Vit. B), einem Ausgleich des Säure-Basen-Haushalts und verschiedenen Medikamenten behandeln. Dazu zählen neben der Hormonersatztherapie die Substitution von Kalzium und Vitamin D3, die Androgentherapie, Bisphosphonate, Strontiumranelat, Calcitonin, Parathormon und Denosumab.
Östrogene und Haut
Östrogene spielen eine wichtige Rolle für die Hautgesundheit. Neben Östradiol und Östriol setzen auch Androgene in der Haut an. Eine HET kann das Hautbild sichtbar verbessern. In Studien wurde immer wieder auf den Vorteil von Östrogen auf die Haut hingewiesen; Frauen, die eine HET einnahmen, wurden dabei von Männern als attraktiver wahrgenommen. In der Menopause verändert sich aber die Haut nicht nur im Gesicht und im Bereich des Dekolletés, sondern auch im Bereich der Schleimhäute der Vulva und Vagina, des Mundes und des Gastrointestinaltraktes. Stellt die Atrophie der Vagina das Hauptproblem der Patientin dar, besteht die Möglichkeit eines lokal verabreichten Östrogens.
Menopause und Schilddrüse
Die Schilddrüse hat über das gesamte Leben der Frau hinweg eine große Bedeutung, insbesondere auch in der Peri- und Menopause. In dieser Phase treten sowohl Über- als auch Unterfunktionen auf, ebenso wie autoimmune und entzündliche Veränderungen. Wichtig sind in diesem Zusammenhang die Laborparameter TSH, ft3 und ft4, aber auch die Schilddrüsenantikörper TPO, TRAK und TGAK bei Verdacht auf einen autoimmunen Prozess.
Menopausale Hormontherapie: differenzierte Risiko-Nutzen-Abwägung
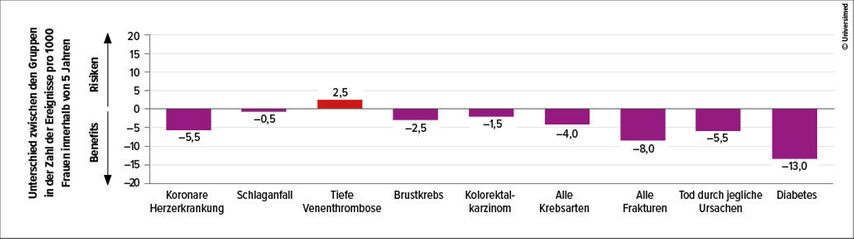
Die Bewertung des Nutzens der menopausalen Hormontherapie erfordert eine individualisierte Betrachtung. Die Indikation zur Hormonersatztherapie (HET) ergibt sich primär aus subjektiven Beschwerden und deren Schweregrad, ist jedoch nicht strikt altersabhängig. Darüber hinaus spielen präventive Aspekte und familiäre Belastungen zunehmend eine Rolle in der Therapieentscheidung (Abb. 1).
Abb. 1: Benefits und Risiken der Hormonersatztherapie (modifiziert nach Manson E und Kaunitz AM: N Engl J Med 2016; 374[9]: 803-6)
Die Dauer der HET ist individuell unterschiedlich, abhängig von Beschwerden. Es besteht die Möglichkeit von Einnahmepausen sowie von Ausschleichversuchen. Ggf. können auch Dosisanpassungen vorgenommen werden.
Therapieoptionen und Applikationswege
Zur Verfügung stehen Östrogene, Progesteron, Androgene (insbesondere Testosteron), DHEA sowie in ausgewählten Fällen Schilddrüsenhormone und Phytotherapeutika. Die Therapie kann als Mono- oder Kombinationstherapie, kontinuierlich oder sequenziell erfolgen.
Östrogene werden oral oder transdermal appliziert, wobei transdermale Applikationsformen aufgrund des geringeren hepatischen First-Pass-Effekts zunehmend bevorzugt werden. Progesteron kann oral, vaginal oder transdermal eingesetzt werden. Die Dosierung sollte symptomorientiert titriert werden, möglich sind Ultra-Low- oder Low-Dose-Regimen (z.B. 0,5–1mg Estradiol oral oder 25–50µg transdermal) bis hin zur Standard-HET mit 1–2, manchmal 4mg Östradiol in Kombination mit Progesteron 50–400mg.
Voruntersuchungen
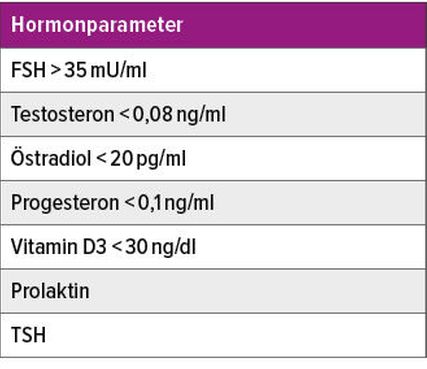
Vor Einleitung einer HET ist eine sorgfältige Basisdiagnostik erforderlich. Neben einer ausführlichen Anamnese und gynäkologischen Untersuchung gehören hormonelle Parameter wie FSH, Prolaktin, TSH (in Kombination mit Prolaktin), Östradiol, Testosteron, Progesteron sowie Vitamin-D-Spiegel zur Basisabklärung (Tab. 1). Ergänzend können ein transvaginaler Ultraschall der Ovarien und Gebärmutter, Mammografie, Osteodensitometrie und ggf. ein Ultraschall der Karotis sinnvoll sein. Die Therapiekontrolle erfolgt individuell und orientiert sich primär an der klinischen Symptomatik. Insbesondere bei adipösen Patientinnen ist auf die Hormonbestimmung und eine genaue Anamnese (Vorhandensein der Trias Myome, Adipositas und Diabetes mellitus) zu achten.
Fazit
Aktuelle Daten zeigen, dass eine frühzeitig begonnene, korrekt dosierte HET bei geeigneter Patientinnenselektion ein günstiges Nutzen-Risiko-Profil aufweist. Neben der effektiven Symptomkontrolle bestehen positive Effekte auf Knochenstoffwechsel, Haut, urogenitale Gesundheit und möglicherweise auf das kardiovaskuläre System. Die Wahl humanidenter Hormone und individualisierter Applikationswege trägt wesentlich zur Sicherheit der Therapie bei.
Literatur:
bei der Verfasserin
Das könnte Sie auch interessieren:
Menopause: Rettung oder Gefahr bei Endometriose?
Die Endometriose wird klassischerweise als östrogenabhängige Erkrankung des reproduktiven Alters betrachtet. Die weitverbreitete Annahme, dass sie mit Eintritt der Menopause verschwindet ...
Resilienz in den Wechseljahren: Strategien gegen Stimmungsschwankungen
Stimmungsschwankungen gehören zu den häufigsten und zugleich am meisten unterschätzten Symptomen der menopausalen Transition. Neben pharmakologischen Therapien gewinnen daher zunehmend ...
Physiotherapie als zentraler Baustein im Behandlungsmanagement
Der Beckenboden spielt in der Menopause eine zentrale Rolle für Kontinenz, Stabilität und Lebensqualität. Hormonelle Veränderungen können zu einer Schwächung der Beckenbodenmuskulatur ...