Ustékinumab: données à 3 ans pour la CU et données en situation réelle pour la MC
Compte-rendu:
Reno Barth
Journaliste médical
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Les patients atteints de colite ulcéreuse qui présentent une cicatrisation muqueuse à la fois histologique et endoscopique après le traitement d’induction par l’ustékinumab ont également de meilleures chances de rémission à long terme. C’est ce que montrent des données issues du programme d’études d’extension de phase III UNIFI. Les données qui ont été présentées au congrès de l’ECCO concernant l’ustékinumab dans le traitement de la maladie de Crohn démontrent une bonne efficacité en conditions cliniques réelles.
La cicatrisation muqueuse: un facteur prédictif à long terme pour la colite ulcéreuse
L’anticorps monoclonal ustékinumab se lie à la sous-unité p40 de l’interleukine (IL)-12 et de l’IL-23, qui jouent un rôle important dans le processus d’inflammation chronique de la muqueuse intestinale dans le cadre des maladies inflammatoires chroniques de l’intestin. L’autorisation pour l’indication de la colite ulcéreuse (CU) repose sur le programme d’études UNIFI de phase III, multicentriques, effectuées en double aveugle et contrôlées contre placebo. Le programme d’études UNIFI comprenait une étude d’induction d’au moins 8 semaines (UNIFI-I) et une étude d’entretien de 44 semaines (UNIFI-M). Les patients ont reçu un traitement d’induction par voie i.v. soit à la dose de 130mg, soit à la dose de 6mg/kg, soit un placebo administré par voie i.v. L’ustékinumab s’est révélé supérieur en termes d’obtention d’une rémission clinique (score de Mayo ≤2).
D’autres évaluations ont notamment montré, selon Rupert Leong de l’Hôpital Concord à Sydney, que les patients ayant obtenu une cicatrisation muqueuse histo-endoscopique («histo-endoscopic mucosal healing», HEMH) – à savoir une amélioration à la fois histologique et endoscopique de la muqueuse – après la phase d’induction du programme d’études UNIFI avaient de meilleures chances d’obtenir une rémission clinique et une rémission sans stéroïdes sur une période d’un an que les patients chez lesquels seules soit une amélioration histologique soit une amélioration endoscopique de la muqueuse avaient été constatées. Leong a présenté des données sur l’effet d’une HEMH post-induction sur l’évolution de la maladie pendant trois ans.1
Les patients présentant une réponse clinique à la semaine 8 ont été randomisés pour recevoir soit 90mg d’ustékinumab administrés par voie s.c. toutes les 8 ou 12 semaines, soit un placebo dans le cadre de l’étude d’entretien de 44 semaines. Les patients qui n’ont pas répondu au traitement à la semaine 8 ont reçu une dose unique de 90mg d’ustékinumab administrés par voie s.c. à la semaine 8, ont été réévalués à la semaine 16 et, en cas de réponse, ont été inclus dans l’étude d’entretien. Après la semaine 44, il a été proposé aux patients de poursuivre le traitement dans le cadre d’une étude d’extension ouverte.
Données aux semaines 92 et 152
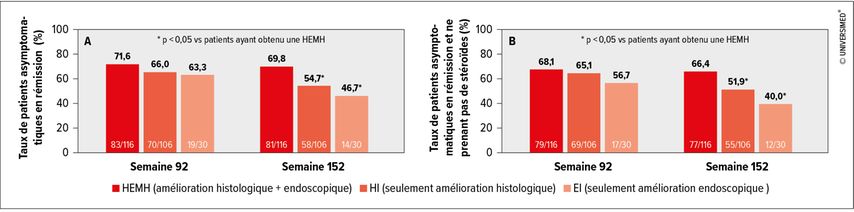
Sur les 438 patients qui ont présenté une réponse à la semaine 8 ou 16 et qui ont été inclus dans l’étude d’entretien, 116 (26,5%) ont obtenu une HEMH, tandis que 30 (6,8%) ont obtenu seulement une amélioration endoscopique («endoscopic improvement», EI) et 106 (24,2%) uniquement une amélioration histologique («histologic improvement», HI). Les patients chez qui une HEMH a été constatée étaient plus susceptibles de présenter une rémission symptomatique (semaine 92: 71,6%; semaine 152: 69,8%; Fig. 1A) et/ou une rémission symptomatique sans stéroïdes (semaine 92: 68,1%; semaine 152: 66,4%; Fig. 1B) à la fois à la semaine 92 et à la semaine 152. Cette différence par rapport aux patients ayant obtenu une EI ou une HI a atteint une signification statistique à la semaine 152. La différence était principalement due à un taux plus élevé de rémissions symptomatiques au cours des semaines 92 à 152.
Chez les patients présentant uniquement une EI ou une HI, la proportion de patients en rémission a constamment diminué: à la semaine 92, 63,3% des patients ayant obtenu une EI présentaient une rémission symptomatique, 56,7% une rémission sans stéroïdes; à la semaine 152, les taux avaient chuté et atteignaient respectivement 46,7% et 40,0%. Également les patients ayant obtenu une HI présentaient un taux de rémission plus faible (patients asymptomatiques: semaine 92: 66,0%; semaine 152: 54,7%; patients asymptomatiques et ne prenant pas de stéroïdes: semaine 92: 65,1%; semaine 152: 51,9%; Fig. 1).
Fig. 1: Rémission symptomatique (A) et rémission symptomatique sans stéroïdes (B) aux semaines 92 et 152 (modifié d’après Leong R et al.)1
Conclusion
Les patients atteints de CU qui obtiennent une cicatrisation muqueuse à la fois histologique et endoscopique (HEMH) après l’induction par l’ustékinumab ont davantage de chances de rester en rémission symptomatique ou de ne pas prendre de stéroïdes pendant deux à trois ans sous traitement d’entretien que les patients qui n’obtiennent qu’une amélioration soit endoscopique soit histologique après l’induction.
Données en situation réelle sur la persistance et la modification de la maladie de Crohn
L’ustékinumab est recommandé dans la directive de l’ECCO sur la prise en charge médicamenteuse de la maladie de Crohn (MC), publiée en 2020, chez les patients atteints d’une maladie modérée ou sévère qui n’ont pas répondu de manière adéquate à un traitement conventionnel et/ou à un agent biologique anti-TNF. Des données sur l’efficacité et la sécurité de l’ustékinumab en conditions cliniques réelles sont désormais disponibles. Elles proviennent entre autres de l’étude STOCUSTE menée dans plusieurs hôpitaux universitaires suédois.2 Les résultats sur 12 mois ont été présentés dans le cadre du congrès de l’ECCO 2022 par Francesca Bello de l’Hôpital Karolinska à Stockholm.
Étude STOCUSTE
Pour cette étude rétrospective, 120 patients ont pu être identifiés et suivis jusqu’à l’arrêt de l’ustékinumab ou jusqu’à la fin du suivi de 12 mois. Il s’agissait d’une population difficile à traiter: ainsi, 19 patients souffraient de fistules, 109 (91%) n’avaient pas répondu de manière adéquate à au moins un et 59 (49%) à au moins deux anti-TNF biologiques. À l’inclusion dans l’étude, 106 (88%) avaient une maladie active, 40 (33%) recevaient des corticostéroïdes et 22 (18%) des thiopurines. L’évaluation a mis en évidence une forte persistance de l’ustékinumab: après 3 mois, 93% des patients poursuivaient le traitement, et à 12 mois, ils étaient encore 56%. Parmi les patients qui étaient encore traités par l’ustékinumab après 3 mois, 38% étaient en rémission et 53% l’étaient après un an. En outre, 26% étaient considérés comme répondeurs au traitement après 12 mois. Sur les 40 patients traités par des corticostéroïdes à l’inclusion dans l’étude, 17 (43%) ont pu arrêter les stéroïdes au 3e mois et 28 (70%) au 12e mois. La calprotectine fécale médiane a diminué, passant de 272µg/g (90–1763) au début de l’étude à 75µg/g (49–99) après 3 mois de traitement. La principale raison de l’arrêt du traitement était la persistance de l’activité de la maladie, seuls 4 patients ont interrompu le traitement par l’ustékinumab en raison d’effets secondaires.2
Étude STARDUST
L’utilisation de l’ustékinumab dans la prise en charge de la MC a été évaluée en ayant recours à deux stratégies thérapeutiques différentes dans l’étude STARDUST: d’une part, dans le cadre d’un traitement standard (SoC) et, d’autre part, dans le cadre d’une stratégie treat-to-target (T2T), qui comprenait une évaluation endoscopique précoce. Dans le groupe SoC, les patients ont reçu de l’ustékinumab administré par voie s.c. toutes les 12 ou 8 semaines après la semaine 16 de l’étude, conformément au résumé des caractéristiques du produit de l’UE. Dans le groupe T2T, l’ustékinumab pouvait être administré jusqu’à toutes les 4 semaines si les valeurs cibles définies pour le SES-CD («simple endoscopic score for Crohn disease»), le CDAI («Crohn’s disease activity index»), la CRP et la calprotectine fécale n’étaient pas atteintes.
Les évaluations présentées à ce jour ont mis en évidence la bonne efficacité de l’ustékinumab dans les deux bras de l’étude, sans avantage significatif pour l’une ou l’autre stratégie,3,4 mais en partie un avantage numérique pour la stratégie T2T. Les observations à long terme sont en cours. Dans le cadre du congrès de l’ECCO 2022, une évaluation concernant les événements modifiant la maladie («disease modifying», DM) de la semaine 48 à 104 a été présentée.5 Selon la définition usuelle, les événements DM étaient les suivants:
-
lésions intestinales (définies par de nouvelles sténoses, des fistules ou l’apparition d’un abcès intra-abdominal),
-
hospitalisation en raison de la MC ou
-
interventions chirurgicales nécessaires en raison de la MC.
L’évaluation a mis en évidence un avantage numérique pour la stratégie T2T concernant le critère d’évaluation composite, un traitement chirurgical n’ayant été que très rarement nécessaire dans les deux bras. La survenue de lésions intestinales et/ou le nombre d’hospitalisations ont été réduits de moitié environ dans le groupe T2T. Il est possible que ceci soit lié à la proportion numériquement plus élevée de répondeurs à l’endoscopie à la semaine 48.3
Selon les auteurs, ces résultats plaident en faveur d’une approche treat-to-target optimisée, qui a recours non seulement à des marqueurs cliniques et des biomarqueurs, mais qui comprend aussi des objectifs strictement définis tels que la réponse endoscopique, afin de faciliter la prise de décision dans la pratique clinique.
Source:
ECCO’22 Congress, 16 au 19 février 2022
Littérature:
1 Leong R et al.: Long-term outcomes after histologic-endoscopic mucosal healing: results from the UNIFI study in ulcerative colitis. ECCO’22 Congress, DOP55 2 Bello F et al.: Long-term real-world data of ustekinumab in Crohn’s Disease – the Stockholm ustekinumab study – STOCUSTE. ECCO’22 Congress, DOP88 3 Danese S et al.: United European Gastroenterol J 2020; 8: 1264-5; LB11 4 D’Haens G et al.: United European Gastroenterol J 2021; 9(Suppl 8): 542 (P0459) 5 Peyrin-Biroulet L et al.: Efficacy of the treat-to-target approach in modifying disease course with ustekinumab in patients with moderate-to-severe Crohn’s Disease: results from the STARDUST trial. ECCO’22 Congress, DOP90
Das könnte Sie auch interessieren:
Études actuelles sur le traitement de l’ILD
Le terme pneumopathie interstitielle (ILD) est un terme générique désignant un groupe important et hétérogène de maladies qui se manifestent principalement dans l’espace broncho- ...
Mise à jour 2026: vers la modification de la maladie
Un grand nombre de médicaments biologiques immunomodulateurs et de «small molecules» ont considérablement élargi l’éventail des options thérapeutiques dans les maladies inflammatoires ...
Schémas thérapeutiques de référence plus courts dans la tuberculose
La tuberculose (TB) constitue toujours un défi majeur à l’échelle mondiale. Malgré les progrès, le besoin de schémas thérapeutiques plus efficaces, plus courts et mieux tolérés reste ...