Traitement ostéoanabolique: quels médicaments, quand et pendant combien de temps?
Compte-rendu:
Regina Scharf, MPH
Rédactrice
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Actuellement, trois médicaments ostéoanaboliques sont autorisés en Suisse dans le traitement de l’ostéoporose sévère. Le Pr Dr méd. Christian Meier de l’Hôpital universitaire de Bâle a présenté de manière claire et pratique les principaux aspects du traitement par ces médicaments lors du congrès annuel de la Société Suisse d’Endocrinologie et de Diabétologie.
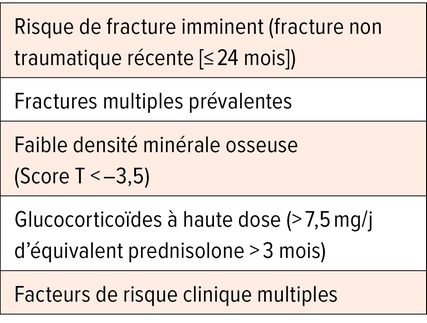
Alors qu’on utilise surtout des médicaments antirésorptifs tels qu’un traitement hormonal substitutif, des bisphosphonates par voie orale et le dénosumab en cas d’ostéoporose avec risque de fracture modéré à élevé, on a recours à des médicaments ostéoanaboliques en cas de risque de fracture très élevé ou imminent (Tab. 1).1 Actuellement, trois médicaments ostéoanaboliques sont autorisés dans le traitement de l’ostéoporose: le tériparatide, l’abaloparatide et le romosozumab. Ils ont un effet plus ou moins important sur la densité minérale osseuse («bone mineral density», BMD), qui est un marqueur de substitution important du risque de fracture et peut être utilisé pour évaluer l’efficacité d’un traitement contre l’ostéoporose.2
Le tériparatide et l’abaloparatide sont des analogues de la PTH. Ils stimulent les ostéoblastes et les ostéoclastes, l’effet de formation l’emportant sur celui de résorption. L’abaloparatide, en particulier, présente une action ostéoanabolique significative en raison de son effet de résorption plus faible.3 L’anticorps monoclonal dirigé contre la sclérostine romosozumab dispose d’un double mécanisme d’action: il augmente la formation osseuse tout en inhibant la résorption osseuse.
Utilisation séquentielle recommandée
«Les médicaments ostéoanaboliques sont aujourd’hui utilisés de manière séquentielle», a déclaré C. Meier. Cela s’explique par le fait que leur utilisation est limitée dans le temps. «Un traitement séquentiel permet en outre de renforcer l’effet à long terme», a-t-il ajouté.
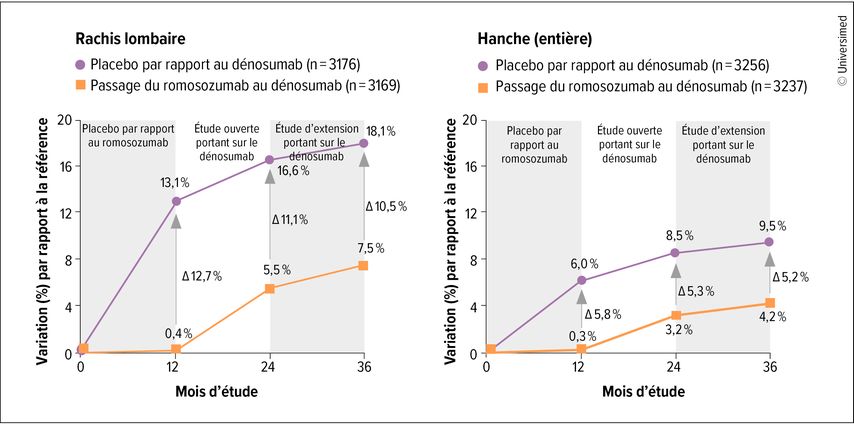
Cela a été démontré, entre autres, dans l’étude FRAME. Elle a révélé que la BMD des patientes initialement traitées par le romosozumab sur 12 mois augmentait fortement et continuait à augmenter lors du traitement ultérieur par le dénosumab, alors que l’augmentation de la BMD sous dénosumab en monothérapie était nettement plus faible (Fig. 1).4,5 Dans l’étude ARCH, un traitement séquentiel par le romosozumab, suivi de l’alendronate a permis de réduire le risque de nouvelles fractures vertébrales de 48% pendant les 24 mois de traitement par rapport à l’alendronate en monothérapie.6
Fig.1: Un traitement par le romosozumab sur un an, suivi du dénosumab sur deux ans réduit durablement le risque de fracture (adaptée selon Lewiecki EM et al. 2019)4
«En raison de l’effet bénéfique d’un traitement ostéoanabolique initial, nous recommandons d’utiliser ces médicaments comme traitement de première intention chez les patients atteints d’ostéoporose et présentant un risque de fracture très élevé», a-t-il déclaré. De plus, un traitement antirésorptif préalable affaiblirait l’effet du romosozumab sur la BMD. Cela a été observé après le traitement par l’alendronate et était encore plus marqué lorsque les patientes avaient reçu un traitement préalable par le dénosumab.7
En cas de passage du dénosumab à un traitement ostéoanabolique, le romosozumab doit néanmoins être privilégié à l’analogue de la PTH tériparatide. L’étude DATA-Switch a révélé que le passage au tériparatide a entraîné une diminution de la BMD au niveau du col du fémur et de la colonne vertébrale en raison d’un effet de rebond.8 Après le passage au romosozumab, la BMD s’est maintenue au niveau de la colonne vertébrale, alors qu’elle a temporairement diminué au niveau de la hanche.9
C. Meier a rappelé qu’un médicament antirésorptif doit être utilisé après le traitement ostéoanabolique pour la minéralisation osseuse secondaire. «Si nous ne le faisons pas, l’augmentation de la densité osseuse obtenue précédemment sera à nouveau perdue», a-t-il précisé.
Choix du médicament approprié
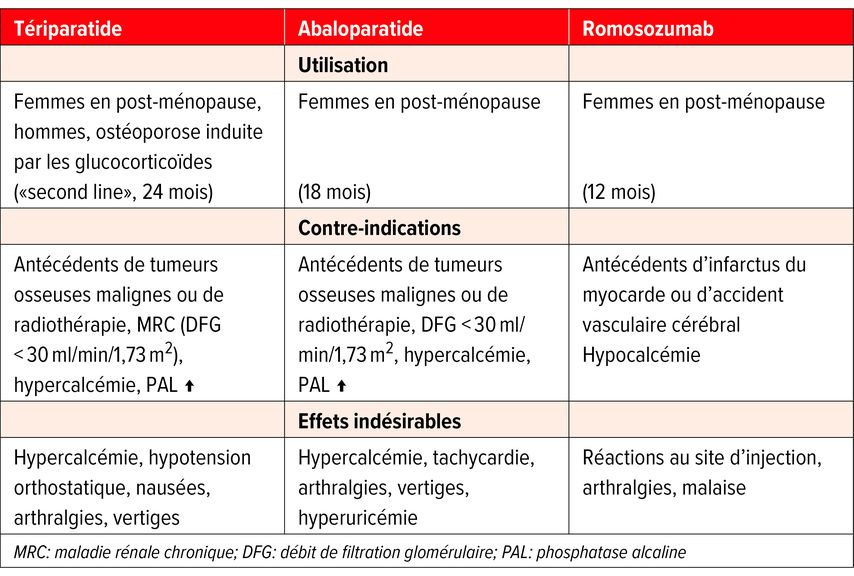
Le romosozumab et l’abaloparatide sont autorisés comme traitement de première intention dans l’ostéoporose sévère avec risque de fracture imminent ou très élevé, ou des antécédents d’au moins deux fractures ostéoporotiques. La durée maximale du traitement par le romosozumab est de 12 mois et celle du traitement par l’abaloparatide de 18 mois. Pour ces deux médicaments, une demande de garantie de prise en charge des coûts doit être effectuée par un médecin spécialisé en endocrinologie ou en rhumatologie, ou par un spécialiste des maladies osseuses. Selon le spécialiste, des critères tels qu’une hypercalcémie, une hypercalciurie ou une tachycardie plaident en faveur d’un traitement par le romosozumab. Il en va de même en cas de risque de fracture de la hanche élevé ou chez les patients ayant reçu un traitement préalable par le dénosumab. En cas de risque cardiovasculaire élevé, il convient cependant de privilégier l’utilisation du tériparatide ou de l’abaloparatide. Les analogues de la PTH constituent également le traitement de première intention dans les maladies liées à un trouble du métabolisme osseux, telles que l’ostéoporose induite par les glucocorticoïdes ou le diabète (Tab. 2).
Tab. 2: Utilisation, contre-indications et effets indésirables des médicaments ostéoanaboliques actuels
Source:
Congrès annuel de la SSED, du 13 au 14 novembre 2025, à Lucerne
Littérature:
1 Ferrari S et al.: 2020 recommendations for osteoporosis treatment according to fracture risk from the Swiss Association against Osteoporosis (SVGO). Swiss Med Wkly 2020; 150: w20352 2 Black D et al.: Bone mineral density as a surrogate endpoint for fracture risk reduction in clinical trials of osteoporosis therapies: an update on SABRE. Lancet Diab Endocrinol 2024 ; 12: 371-73 3 Tabacco G, Bilezikian JP: Osteoanabolic and dual action drugs. Br J Clin Pharmacol 2019; 85: 1084-94 4 Cosman F et al.: FRAME Study: The foundation effect of building bone with 1 year of romosozumab leads to continued lower fracture risk after transition to denosumab. J Bone Miner Res 2018; 33: 1219-26 5 Lewiecki EM et al.: One year of romosozumab followed by two years of denosumab maintains fracture risk reductions: results of the FRAME extension study. J Bone Miner Res 2019; 34: 419-28 6 Saag KG et al.: Romosozumab or alendronate for fracture prevention in women with osteoporosis. N Engl J Med 2017; 377: 1417-27 7 Cosman F et al.: Romosozumab and antiresorptive treatment: the importance of treatment sequence. Osteoporos Int 2022; 33: 1243-56 8 Leder BZ et al.: Denosumab and teriparatide transitions in postmenopausal osteoporosis (the DATA-Switch study): extension of a randomised controlled trial. Lancet 2015; 386: 1147-55 9 Langdahl BL et al.: Romosozumab (sclerostin monoclonal antibody) versus teriparatide in postmenopausal women with osteoporosis transitioning from oral bisphosphonate therapy: a randomised, open-label, phase 3 trial. Lancet 2017; 390: 1585-94
Das könnte Sie auch interessieren:
L’obésité et ses conséquences sur les reins
L’obésité est devenue l’un des principaux problèmes de santé dans le monde. Elle a des conséquences directes et indirectes sur les reins. Outre le risque de glomérulopathie et l’ ...
Une perte de poids précoce peut favoriser la rémission du diabète de type 2
De nouveaux concepts physiopathologiques remettent en question la compréhension actuelle du diabète de type 2 (DT2). L’accent n’est plus mis sur l’augmentation de la glycémie, mais sur ...
Suivi à long terme après un cancer de l’enfant ou de l’adolescent: points pertinents pour les internistes et les médecins de famille
En raison de l’augmentation de la survie globale après un cancer de l’enfant ou de l’adolescent, la population de patients ayant survécu à un cancer de l’enfant ne cesse de croître et de ...