Suivi à long terme après un cancer de l’enfant ou de l’adolescent: points pertinents pour les internistes et les médecins de famille
Auteure:
Dre méd. Maria Otth, PhD
Zentrum für Hämatologie/Onkologie
Stiftung Ostschweizer Kinderspital
St. Gallen
E-mail: maria.otth@kispisg.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
En raison de l’augmentation de la survie globale après un cancer de l’enfant ou de l’adolescent, la population de patients ayant survécu à un cancer de l’enfant ne cesse de croître et de vieillir. Parallèlement, le suivi à long terme prend de plus en plus d’importance, y compris pour ces patients qui sont désormais adultes. Nombre d’internistes, de médecins de famille et de spécialistes (p.ex. en endocrinologie, cardiologie, néphrologie) traitent des patients ayant survécu à un cancer de l’enfant, qu’ils en aient connaissance ou non. Cet article donne un aperçu des besoins spécifiques de ces patients, résume la situation actuelle en Suisse et présente les offres existantes.
Keypoints
-
Les patients ayant survécu à un cancer de l’enfant peuvent développer des séquelles tardives liées au traitement oncologique, qui peuvent potentiellement toucher n’importe quel système d’organes. Toutes les disciplines de la médecine adulte doivent y être sensibilisées.
-
Le risque de survenue des séquelles à long terme dépend du traitement oncologique et peut être évalué individuellement pour chaque patient ayant survécu à un cancer de l’enfant.
-
Un suivi à long terme personnalisé et adapté au risque est recommandé pour la majeure partie de ces patients, même à l’âge adulte.
En Suisse, environ 350 enfants et adolescents (<18 ans) sont atteints d’un cancer chaque année. Les progrès réalisés dans le traitement oncologique dans ces groupes d’âge ont permis d’améliorer le taux de survie à 5 ans, qui est passé de 5 à 30% au début des années 1970 à environ 85% aujourd’hui dans le monde.1–3La Suisse est l’un des pays enregistrant le meilleur résultat au niveau international avec un taux de survie à 10 ans de 88%, tous diagnostics confondus.4 Les facteurs déterminants de ces progrès concernent la stratification du risque et l’intensité du traitement, les mesures de support et, de plus en plus, les nouveaux médicaments.
Une meilleure stratification du risque a permis de réduire parfois considérablement le traitement chez les patients présentant un faible risque de récidive. Le lymphome de Hodgkin en est un exemple. Dans l’étude européenne GPOH-HD-2002, environ 85% des enfants et des adolescents diagnostiqués entre 2002 et 2005 ont subi une radiothérapie. Une radiothérapie a pu être évitée chez environ 50% des patients (<18 ans) diagnostiqués d’un lymphome de Hodgkin classique de stade IA, IB ou IIA dans l’étude EuroNet-PHL-C1 qui a suivi.5 Malgré la réduction de l’intensité du traitement, la survie élevée à 5 ans a été maintenue.Dans l’étude de suivi EuroNet-PHL-C2, dont les analyses ne sont pas encore terminées, la radiothérapie a pu être réduite jusqu’à 85% dans certains groupes à risque (communication personnelle de la Pre Mauz-Körholz). Étant donné que la radiothérapie thoracique chez l’enfant et l’adolescent augmente considérablement le risque de tumeures secondaires mammaires, en particulier chez les femmes (risque équivalent à celui des porteuses de la mutation dans le gène BRCA), celui-ci peut également être significativement réduit par la suite. L’amélioration de la stratification du risque permet toutefois également d’identifier les patients présentant un risque élevé de récidive. Ces derniers peuvent bénéficier d’une intensification précoce du traitement ou de l’utilisation précoce de nouveaux médicaments, la survie pouvant là aussi être prolongée. Les progrès réalisés dans les mesures de soutien (p.ex. antiémétiques, prophylaxie des infections, alimentation) contribuent à la bonne tolérance des traitements souvent intensifs par les patients, ce qui participe également à la survie globale élevée. Ces dernières années, de nouvelles approches thérapeutiques (p.ex. immunothérapies, traitements ciblés) jouent un rôle de plus en plus important. De nouvelles approches thérapeutiques font désormais partie du traitement de première intention dans certains diagnostics (p.ex. le blinatumomab dans les leucémies).
Malgré tous ces progrès, les séquelles tardives du traitement jouent un rôle significatif dans la vie de nombre de patients ayant survécu à un cancer de l’enfant, appelés aussi survivants.
Séquelles tardives après un traitement oncologique chez l’enfant et l’adolescent
Les séquelles à long terme se traduisent par des troubles médicaux chroniques et surviennent à la suite du traitement oncologique antérieur. Ils peuvent survenir dès le diagnostic ou le traitement (p.ex. déficits neurologiques après une tumeur cérébrale, une amputation ou une perte d’audition) ou plus tard seulement. Les séquelles tardives peuvent potentiellement toucher n’importe quel système d’organes. La fréquence varie en fonction du type et de la sévérité des séquelles à long terme ainsi que de l’âge actuel des survivants, mais ils sont souvent mentionnés dans environ deux tiers des cas.6–8 On part du principe que le traitement oncologique accélère le processus de vieillissement physiologique des organes et que, par conséquent, les limitations fonctionnelles des organes peuvent survenir plus tôt. La radiothérapie comporte un risque supplémentaire de développement des tumeures secondaires. Les systèmes d’organes qui présentent un risque accru dépendent du diagnostic, du traitement, des complications pendant le traitement ainsi que d’éventuels antécédents. Ce risque doit être déterminé individuellement pour chaque survivant. Cela doit donner lieu à une consultation et un suivi personnalisés.
Suivi à long terme et recommandations
Dans les premières années suivant la fin du traitement, le suivi oncologique se concentre principalement sur la détection précoce des récidives. Parallèlement, des examens de dépistage sont réalisés pour détecter des séquelles à long terme potentielles. Plus le temps passe après la fin du traitement, plus l’accent est mis sur le dépistage précoce de ces séquelles dans le cadre du suivi à long terme. Les contrôles sont effectués sous forme d’examens de dépistage personnalisés, ciblés et adaptés au risque. Le suivi à long terme se déroule conformément aux directives internationales, les principales étant les recommandations de l’International Guideline Harmonization Group, les PanCare Guidelines (UE) et les Guidelines du Children’s Oncology Group (États-Unis).9–12
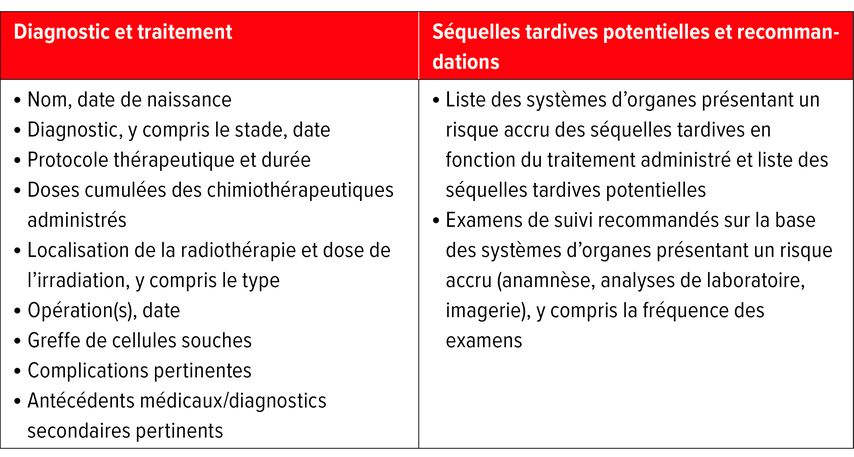
Les piliers pour la formulation des recommandations sur le suivi à long terme sont le diagnostic, y compris le stade, le traitement administré, les complications potentielle et les antécédents. Le Tableau 1 résume ces quatre piliers dans la colonne de gauche. La deuxième étape consiste à définir les systèmes d’organes pour lesquels des examens de dépistage sont recommandés. Ces informations sont intégrées dans le résumé du traitement personnalisé qui fournit une vue d’ensemble du diagnostic, du traitement administré, des séquelles tardives potentielles ainsi que de l’intervalle et de la modalité d’examen. Des contrôles cardiologiques réguliers sont par exemple recommandés après un traitement à base d’anthracyclines, la fréquence dépendant de la dose cumulée. La fonction rénale est contrôlée, entre autres, après un traitement par des alkylants, une chimiothérapie à base de platine, une radiothérapie impliquant les reins ou une néphrectomie. Le résumé du traitement est toujours remis aux survivants ainsi qu’aux médecins impliqués dans le suivi. Il aide les médecins n’ayant pas ou peu d’expérience dans le suivi à long terme à mettre en relation les troubles ou les symptômes avec les antécédents oncologiques.
Il convient de mentionner ici que les directives internationales actuelles sont principalement axées sur les «anciens» chimiothérapeutiques connus. Pour les traitements et les médicaments plus récents (p.ex. blinatumomab, brentuximab vedotin, dabrafenib), il n’existe encore que peu ou pas de données à long terme chez les enfants et les adolescents. C’est aussi pour cette raison que les directives internationales sont régulièrement mises à jour. Parallèlement, les résumés du traitement déjà rédigés et remis aux survivants doivent aussi être fréquemment vérifiés et, le cas échéant, mis à jour.
Modèles de suivi à long terme
La littérature décrit principalement cinq modèles de suivi à long terme (Tab.2).13–17
Ils ont tous les objectifs suivants:
-
surveiller la survenue des séquelles à long terme potentielles liés au traitement (dépistage),
-
informer les patients, les survivants, les médecins et les autres professionnels de santé (éducation et autonomisation), et
-
garantir un traitement approprié en cas de survenue des séquelles à long terme.
Les modèles conservant un lien avec l’oncologie pédiatrique ou les experts en suivi à long terme ont l’avantage de pouvoir vérifier et mettre à jour les résumés du traitement à intervalles réguliers.
Situation en Suisse
En Suisse, les enfants et les adolescents (<18 ans) sont traités dans l’une des neuf cliniques d’oncologie pédiatrique regroupées depuis 50 ans au sein du Groupe d’Oncologie Pédiatrique Suisse (SPOG, www.spog.ch ). Le suivi se déroule dans l’une des cliniques appartenant au SPOG jusqu’à l’âge de 18 ans, voire plus longtemps dans certaines cliniques. Les survivants adultes passent ensuite à différents modèles de suivi à long terme en fonction de la situation locale: principalement un modèle avec consultation de suivi à long terme spécifique (modèle 1, Tab.2) ou un modèle chez le médecin de famille (modèle 5), plus rarement un modèle spécifique à la maladie (modèle 3). Le modèle 3 se déroule différemment selon les cliniques. Si l’on prend l’exemple de la neuro-oncologie, il peut s’agir d’une consultation de suivi en neuro-oncologie intégrée dans le modèle 1. Outre l’accent mis sur la neurologie, les autres systèmes d’organes présentant un risque accru des séquelles à long terme sont également pris en compte. Les patients passent parfois à des consultations neurologiques ou neurochirurgicales; d’autres systèmes d’organes ne sont souvent pas pris en considération dans ce modèle. Nombre de survivants optent pour le modèle 1, même si cela peut signifier que les contrôles ont lieu plus loin de chez eux. La coordination de différentes disciplines la même (demi-)journée, la consultation d’experts en suivi à long terme ainsi que la convocation écrite pour les visites (souvent tous les 1 à 2 ans) sont des avantages souvent cités. Ces avantages contribuent au respect des contrôles à l’âge adulte.17
En cas de transfert au médecin de famille (modèle 5), il est chargé d’orienter les patients vers d’autres spécialistes (p.ex. cardiologie) en fonction des examens de dépistage nécessaires. Dans ce contexte, il est important que le résumé du traitement soit également remis aux autres médecins impliqués dans le suivi par le médecin de famille ou le survivant.
Si un survivant se présente pour la première fois chez un interniste, un médecin de famille ou un spécialiste et qu’il n’est pas certain que ses antécédents oncologiques aient une influence sur la raison de la consultation, il vaut la peine de demander au survivant un résumé du traitement. Si aucun résumé n’existe et si cette information est pertinente pour la suite du suivi ou si le survivant en a besoin, il convient de l’orienter vers une consultation de suivi oncologique spécialisée. Ce type de consultation est actuellement principalement rattaché à des centres d’oncologie pédiatrique, certains proposant une consultation unique (p.ex. Hôpital universitaire pédiatrique de Zurich) et d’autres un suivi à plus long terme (p.ex. Hôpital pédiatrique de Suisse orientale). Les liens correspondants sont disponibles sur le site Cancer de l’Enfant en Suisse ( https://www.kinderkrebs-infoplattform.ch/de/survivors/angebote-fachstelle/nachsorgesprechstunden ).
Conclusion
Le nombre de patients ayant survécu à un cancer de l’enfant est en augmentation, même en médecine adulte. Les médecins doivent avoir connaissance des besoins spécifiques de ces patients. En cas d’incertitude, ils peuvent demander aux patients s’ils disposent d’un résumé du traitement. Si aucun résumé n’existe, ils peuvent le réclamer auprès de la clinique qui les a traités ou s’adresser à une consultation de suivi oncologique spécialisée.
Littérature:
1 Gibson TM et al.: Temporal patterns in the risk of chronic health conditions in survivors of childhood cancer diagnosed 1970-99: a report from the Childhood Cancer Survivor Study cohort. Lancet Oncol 2018; 19: 1590-601 2 Botta L et al.: Long-term survival and cure fraction estimates for childhood cancer in Europe (EUROCARE-6): results from a population-based study. Lancet Oncol 2022; 23: 1525-36 3 Howlader N et al. (eds): SEER Cancer Statistics Review, 1975-2018. National Cancer Institute. Bethesda, MD,https://seer.cancer.gov/csr/1975_2018/, based on November 2020 SEER data submission, posted to the SEER web site, April 2021; https://seer.cancer.gov/archive/csr/1975_2018/index.html, zuletzt aufgerufen am 10.3.2026 4 Kinderkrebsregister: Jahresbericht. https://www.kinderkrebsregister.ch/statistiken-und-berichte/jahresberichte/ ; zuletzt aufgerufen am 6.3.2026 5 Mauz-Körholz C et al.: Response-adapted omission of radiotherapy in children and adolescents with early-stage classical Hodgkin lymphoma and an adequate response to vincristine, etoposide, prednisone, and doxorubicin (EuroNet-PHL-C1): a titration study. Lancet Oncol 2023; 24: 252-61 6 Bhakta N et al.: The cumulative burden of surviving childhood cancer: an initial report from the St Jude Lifetime Cohort Study (SJLIFE). Lancet 2017; 390: 2569-82 7 Oeffinger KC et al.: Chronic health conditions in adult survivors of childhood cancer. N Engl J Med 2006; 355: 1572-82 8 Hudson MM et al.: Clinical ascertainment of health outcomes among adults treated for childhood cancer. JAMA 2013; 309: 2371-81 9 International Guideline Harmonization Group for Late Effects of Childhood Cancer: http://www.ighg.org/ ; zuletzt aufgerufen am 6.3.2026 10 Kremer LC et al.: A worldwide collaboration to harmonize guidelines for the long-term follow-up of childhood and young adult cancer survivors: a report from the International Late Effects of Childhood Cancer Guideline Harmonization Group. Pediatr Blood Cancer 2013; 60: 543-9 11 PanCare: www.pancare.eu ; zuletzt aufgerufen am 6.3.2026 12 Long-Term Follow-Up Guidelines Version 6.0: http://www.survivorshipguidelines.org/pdf/2023/COG_LTFU_Guidelines_Only_v6.pdf ; zuletzt aufgerufen am 6.3.2026 13 Friedman DL et al.: Models of care for survivors of childhood cancer. Pediatr Blood Cancer 2006; 46: 159-68 14 Singer S, Gianinazzi ME, Hohn A, Kuehni CE, Michel G: General practitioner involvement in follow-up of childhood cancer survivors: a systematic review. Pediatr Blood Cancer 2013; 60: 1565-73 15 Eshelman-Kent D et al.: Cancer survivorship practices, services, and delivery: a report from the Children’s Oncology Group (COG) nursing discipline, adolescent/young adult, and late effects committees. J Cancer Surviv 2011; 5: 345-57 16 Dixon SB et al.: Factors influencing risk-based care of the childhood cancer survivor in the 21st century. CA Cancer J Clin 2018; 68: 133-52 17 Otth M et al.: Transition from pediatric to adult follow-up care in childhood cancer survivors – a systematic review. J Cancer Surviv 2021; 15: 151-62
Das könnte Sie auch interessieren:
L’obésité et ses conséquences sur les reins
L’obésité est devenue l’un des principaux problèmes de santé dans le monde. Elle a des conséquences directes et indirectes sur les reins. Outre le risque de glomérulopathie et l’ ...
Traitement ostéoanabolique: quels médicaments, quand et pendant combien de temps?
Actuellement, trois médicaments ostéoanaboliques sont autorisés en Suisse dans le traitement de l’ostéoporose sévère. Le Pr Dr méd. Christian Meier de l’Hôpital universitaire de Bâle a ...
Une perte de poids précoce peut favoriser la rémission du diabète de type 2
De nouveaux concepts physiopathologiques remettent en question la compréhension actuelle du diabète de type 2 (DT2). L’accent n’est plus mis sur l’augmentation de la glycémie, mais sur ...