Examens diagnostiques néphrologiques de base
Auteur:
Dr méd. Cédric Jäger EMBA (UniL)
Abteilung für Nephrologie
Medizinische Universitätsklinik
Kantonsspital Baselland, Standort Bruderholz
E-mail: cedric.jaeger@ksbl.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Bien que l’insuffisance rénale chronique (IRC) soit l’une des maladies les plus fréquentes,1 sa mortalité a augmenté ces dernières années par rapport aux maladies cancéreuses ou à la BPCO.2 L’apparition de nouveaux traitements néphroprotecteurs tels que les inhibiteurs du SGLT2 et les analogues du GLP-1 rend le dépistage précoce de l’IRC plus important que jamais. Cet article traite des possibilités d’examens diagnostiques néphrologiques de base dans le cadre de la médecine de premier recours.
Keypoints
-
Un dépistage de l’insuffisance rénale chronique (IRC) est recommandé chez tous les patients souffrant de maladies cardiovasculaires, de diabète ou présentant un risque accru d’IRC.
-
Le dépistage comprend la détermination de la fonction rénale au moyen de la créatinine et du DFGe (CKD-EPI), mais aussi l’albuminurie au moyen du rapport albuminurie/créatininurie dans l’urine (RAC).
-
Les examens diagnostiques de base approfondis englobent, selon la problématique, le sédiment urinaire, un examen complet de la protéinurie, la détermination des indices urinaires et l’échographie.
Quand faut-il dépister les néphropathies?
Un dépistage généralisé des néphropathies sous forme d’examen de routine réalisé dans l’ensemble de la population n’est pas recommandé. Cependant, la présence de certaines comorbidités augmente considérablement la probabilité pré-test d’une IRC, de sorte que les patients qui remplissent au moins l’un des trois critères suivants doivent être dépistés:
-
présence d’une hypertension artérielle ou d’autres maladies cardiovasculaires,
-
d’un diabète ou
-
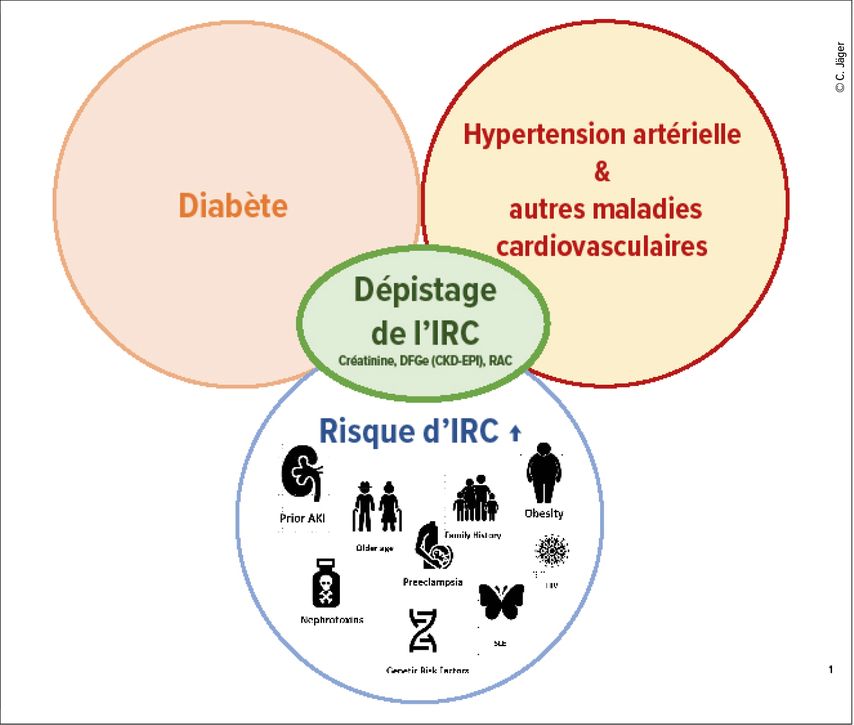
de comorbidités associées à une néphropathie (Fig. 1).3
Fig. 1: Un dépistage de l’insuffisance rénale chronique (IRC) doit être effectué en présence de diabète ou de maladies cardiovasculaires et en cas de comorbidités définies présentant un risque accru d’IRC (adapté d’après Shlipak et al.)3
La fonction rénale
Le rein est le principal régulateur de l’homéostasie de l’organisme. En dépit de variations considérables des apports et des facteurs environnementaux, le rein maintient l’équilibre de la composition de l’organisme de manière étroitement contrôlée. Lorsque nous déterminons la fonction rénale dans la pratique clinique quotidienne, nous mesurons sa fonction excrétoire. Celle-ci englobe la filtration glomérulaire du plasma et la réabsorption ou la sécrétion tubulaire sélective d’eau ou d’électrolytes. Dans la pratique clinique quotidienne, le débit de filtration glomérulaire (DFG) s’est imposé comme substitut de la fonction excrétoire. Le DFG est défini par le produit du taux de filtration de chacun des néphrons multiplié par leur nombre. Pour standardiser la fonction rénale en fonction de variations telles que la taille des reins, le DFG est normalisé pour 1,73m2 de surface corporelle, ce qui correspond à la surface corporelle moyenne d’hommes et de femmes jeunes. Le DFGnormal est d’environ 120–130ml/min/1,73m2 chez les jeunes adultes en bonne santé et diminue constamment avec l’âge.4 Malgré de nombreuses limitations, la créatinine – un produit final du catabolisme musculaire – reste le meilleur marqueur de substitution pour estimer le DFG. Elle est filtrée librement et n’est que peu absorbée ou sécrétée au niveau tubulaire. Les variations d’origine extrarénale telles que l’âge, le sexe ou la composition corporelle constituent des limitations. De plus, la créatinine réagit lentement aux modifications aiguës du DFG et est toujours retardée de quelques jours. Différentes formules (Cockcroft-Gault, MDRD, CKD-EPI) utilisent différents paramètres pour estimer le DFG à partir de la créatinine sérique. La formule la plus précise est l’équation CKD-EPI qui inclut la créatinine, l’âge, le sexe et l’ethnie. Elle a été validée dans une grande cohorte5 et est aujourd’hui considérée comme la norme. L’année dernière, une nouvelle version de la formule CKD-EPI, qui ne tient plus compte de l’ethnie, a été publiée.6 On ne sait pas encore si elle s’imposera.
La cystatine C est une alternative à la créatinine et est présente dans la plupart des cellules de l’organisme. Bien qu’elle soit théoriquement moins dépendante de facteurs extrarénaux, il n’a pas été prouvé jusqu’à présent que l’estimation du DFGe est bien meilleure lorsqu’on utilise la cystatine C plutôt que la créatinine. Cependant, elle est désormais acceptée comme marqueur de la fonction rénale et a été intégrée dans les directives.3,6 La plupart des néphrologues ne la déterminent toutefois que dans certaines problématiques. Il faut également tenir compte du fait qu’en Suisse, sa détermination est cinq fois plus chère que celle de la créatinine qui, elle, reste abordable.
Protéinurie
La prévalence de la protéinurie dans la population globale est d’environ 8% et augmente avec l’âge.7 La protéinurie est un marqueur important de nombreuses néphropathies et joue un rôle dans leur dépistage, leur diagnostic et leur surveillance. Elle est souvent le premier signe d’une maladie glomérulaire et peut survenir avant une chute du DFGe. Outre son importance pour les examens diagnostiques, la protéinurie est également un prédicteur de risque de progression des néphropathies et un signe de mortalité cardiovasculaire accrue. On distingue la protéinurie glomérulaire, la protéinurie tubulaire et la protéinurie par débordement.
L’excrétion normale de protéines est d’environ 150mg par jour. La plus grande partie est constituée de protéines non spécifiques comme la protéine de Tamm-Horsfall. Dans le cadre des examens diagnostiques de la protéinurie, on différencie les protéines de haut poids moléculaire (albumine) et les protéines de faible poids moléculaire (α1-microglobuline, protéine de liaison au rétinol). L’albumine est le principal marqueur de la protéinurie dite glomérulaire. Dans le rein sain, elle est peu filtrée par la membrane basale glomérulaire et sa présence dans l’urine est donc toujours le signe d’une lésion glomérulaire structurelle. Par le passé, on parlait de microalbuminurie pour désigner une albuminurie comprise entre 30 et 300mg/j, tandis qu’une valeur d’albuminurie >300mg/j était appelée une macroalbuminurie. Ces désignations portant à confusion, elles ne doivent plus être utilisées étant donné qu’il s’agit dans tous les cas d’une albuminurie.
On parle de protéinurie tubulaire lorsque des protéines de faible poids moléculaire (α1-microglobuline, protéine de liaison au rétinol) sont détectées dans l’urine. Ces protéines sont filtrées librement, mais elles sont généralement réabsorbées par le système tubulaire et ne sont pratiquement plus mesurables dans un rein sain. Elles indiquent un trouble de la réabsorption tubulaire tel qu’il peut se produire en cas d’insuffisance rénale aiguë prérénale associée à une nécrose tubulaire ou en cas de néphrite tubulo-interstitielle.
Une protéinurie par débordement, le troisième type de protéinurie, survient lorsque de grandes quantités de protéines plasmatiques (p.ex. chaînes légères en présence d’un myélome multiple ou myoglobine en cas de rhabdomyolyse) dépassent la capacité de résorption du système tubulaire.
Détermination quantitative de la protéinurie
Le recueil d’urine de 24 heures est la méthode de référence permettant une détermination quantitative de la protéinurie. En raison de sa complexité et des erreurs de collecte fréquentes, elle est cependant actuellement rarement utilisée.
La bandelette urinaire mesure l’albumine de manière semi-quantitative. Elle est toutefois peu sensible et n’est pas en mesure de détecter de petites quantités d’albumine, ce qui en fait un outil de dépistage pas toujours adapté. De plus, la bandelette ne permet pas de détecter la protéinurie tubulaire ou la protéinurie par débordement.
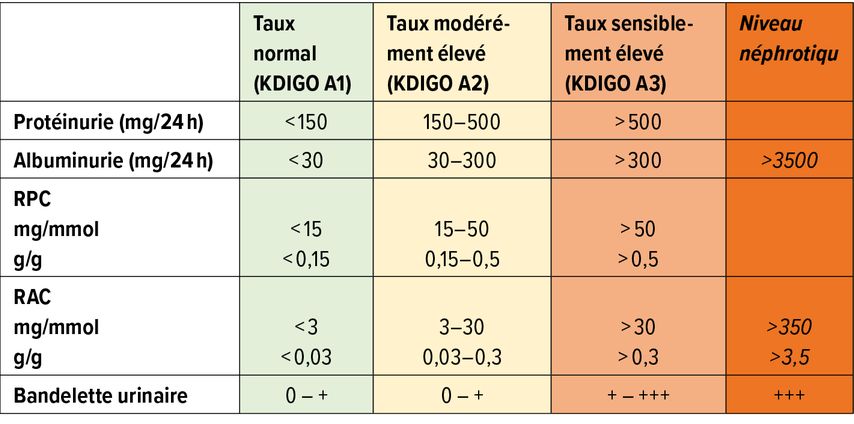
Les rapports urinaires constituent le meilleur outil pour quantifier facilement la protéinurie. Il s’agit de mesurer la concentration de protéines dans un spot urinaire et de l’exprimer par rapport à la concentration de créatinine. Dans l’idéal, la détermination est effectuée sur la première ou la deuxième urine du matin. Dans la pratique clinique, tout spot urinaire est toutefois acceptable. Les unités utilisées sont le mg/mmol ou le g/g. En raison de l’excrétion constante de créatinine de 100–200µmol/kg de PC, la protéinurie quotidienne peut être facilement estimée. Ainsi, une personne de 70kg excrète environ 10mmol de créatinine par jour (150µmol x 70kg). Si on utilise un rapport exprimé en mg/mmol, il suffit donc de multiplier par 10 pour obtenir une estimation de la protéinurie par jour. En mg/g, le résultat correspond directement à la protéinurie quotidienne, en effet 1g de créatinine correspond à environ 10mmol de créatinine (8,8mmol) (Tab. 1). Plusieurs études ont montré que la protéinurie quotidienne estimée à partir des rapports est bien corrélée avec le recueil des urines sur 24 heures et rend obsolète la collecte fastidieuse.8
Dans la pratique clinique, il est recommandé de déterminer le rapport albuminurie/créatininurie dans l’urine (RAC) lors de l’examen de dépistage. Ce test est standardisé dans la plupart des laboratoires et constitue à la fois un marqueur d’atteinte glomérulaire et un facteur de risque cardiovasculaire pertinent. Il a été démontré à plusieurs reprises que même des quantités infimes d’albumine dans l’urine (<300mg/j) sont associées à une mortalité cardiovasculaire nettement plus élevée.9 Toutefois, l’albuminurie doit plutôt être considérée comme un marqueur de substitution de risque cardiovasculaire accru que comme un lien de causalité.
S’il s’agit de clarifier l’étiologie d’une insuffisance rénale avérée, la valeur diagnostique du RAC est limitée dans la mesure où ce paramètre ne détecte ni les protéines (tubulaires) de faible poids moléculaire ni une protéinurie par débordement. Dans ces cas, il est recommandé de déterminer un profil protéique complet (protéines totales, albumine, α1-microglobuline, protéines de liaison au rétinol). Si ce n’est pas possible, le rapport protéines/créatinine urinaire (RPC) et le RAC peuvent être déterminés ensemble. S’il existe un écart important entre les deux valeurs, ceci indique la présence de protéines autres que l’albumine (p.ex. protéinurie tubulaire). Si l’écart est supérieur à une valeur estimée de 1g/j, il faut songer, sur la base d’un diagnostic différentiel, à une protéinurie par débordement.
Hématurie
L’hématurie désigne la détection d’érythrocytes dans l’urine. La bandelette urinaire n’est pas appropriée pour la détection étant donné qu’elle ne mesure pas les érythrocytes, mais l’hémoglobine. Des résultats faux positifs sont obtenus par exemple en présence de myoglobine. Mais des substances oxydantes telles que les désinfectants ou le sperme peuvent également entraîner des résultats faux positifs. Il est donc recommandé de procéder à un sédiment urinaire. Pour ce faire, il faut centrifuger 10ml d’urine, décanter le surnageant et examiner le centrifugat au microscope. La microhématurie est définie comme la détection de plus de 2 (à 5) érythrocytes par champ de vision à un grossissement de 400x. Il est important de faire la distinction entre les érythrocytes dits glomérulaires (formes annulaires, acanthocytes) et les érythrocytes non glomérulaires. Les érythrocytes glomérulaires déformés sont toujours d’origine rénale et sont l’expression d’une glomérulopathie. Si une microhématurie glomérulaire est mise en évidence, il est recommandé, en particulier en cas de survenue simultanée d’une insuffisance rénale et/ou d’une protéinurie, d’adresser le patient à un néphrologue pour effectuer des examens complémentaires et, le cas échéant, de réaliser une biopsie rénale.
Indices urinaires
Le dosage du sodium, de l’urée et de la créatinine urinaires, mais aussi du sodium, de l’urée et de la créatinine sériques permet de calculer les indices urinaires FENa (excrétion fractionnelle de sodium) et FEUrea (excrétion fractionnelle d’urée). Certains laboratoires les calculent directement; dans le cas contraire, les formules figurent dans de nombreuses applications médicales. Elles font partie intégrante de l’évaluation d’une insuffisance rénale aiguë. Une FENa <1% ou une FEUrea <35% sont le signe d’une insuffisance rénale prérénale. Contrairement à la FENa, la FEUrea n’est pas faussée par la prise de diurétiques. Ces indices sont très spécifiques des causes prérénales, mais des indices normaux ne les excluent pas.
Échographie
L’échographie a son importance pour les problématiques de modifications structurelles (p.ex. kystes rénaux, taille des reins) ou de modifications d’origine post-rénale. Un rein sain mesure entre 8,5 et 13cm. Des différences de taille peuvent par exemple suggérer des problèmes de perfusion chroniques. Une congestion du bassinet indique un obstacle à l’écoulement et doit faire l’objet d’un examen urologique urgent, en particulier en présence d’insuffisance rénale.
Quand faut-il faire appel à un néphrologue?
Adresser le patient à un néphrologue n’est pas nécessaire à chaque fois qu’une insuffisance rénale, une protéinurie ou une hématurie glomérulaire sont détectées.
Ceci est toutefois recommandé dans les situations suivantes:
-
Pour clarifier l’étiologie en cas de
- détérioration rapide du DFGe
>5ml/min/1,73m2 en un an
- (augmentation de la) protéinurie
(RAC >50 à 100mg/mmol)
- microhématurie glomérulaire
associée la détection simultanée
d’une albuminurie et/ou d’une
insuffisance rénale -
En présence d’un DFGe de 30 à 45ml/min/1,73m2 en cas d’insuffisance rénale chronique progressive
- pour évaluer et traiter les complica-tions secondaires
- pour planifier la suite de la prise en charge commune -
En cas de DFGe de 15 à 25ml/min/1,73m2 pour planifier et préparer un traitement de substitution rénale
Résumé
L’insuffisance rénale chronique est une maladie fréquente associée à une morbidité et une mortalité élevées. Les nouvelles possibilités de traitement rénoprotecteur rendent le dépistage précoce essentiel. L’examen de dépistage comprend la détermination de la fonction rénale et de l’albuminurie. Malgré certaines limites, la créatinine sérique reste la meilleure méthode pour déterminer la fonction rénale, ce qui permet d’estimer le DFGe à l’aide de la formule CKD-EPI. Le RAC à partir d’un spot urinaire est la meilleure méthode pour déterminer l’albuminurie quantitative qui est bien corrélée à l’albuminurie quotidienne. Les examens diagnostiques approfondis comprennent la détermination de l’hématurie au moyen du sédiment urinaire, la détermination du profil de protéines urinaires en cas de troubles de la fonction rénale et des indices urinaires en présence d’insuffisance rénale aiguë, mais aussi l’échographie, principalement pour mettre en évidence des anomalies morphologiques ou pour détecter des causes post-rénales.
Littérature:
1 Tomonaga Y et al.: The prevalence of chronic kidney disease in a primary care setting: a Swiss cross-sectional study. PLoS One 2013; 8: e67848 2 Institute for Health Metrics and Evaluation: Findings from the global burden of disease study 2017. 2018. www.healthdata.org 3 Shlipak MG et al.: The case for early identification and intervention of chronic kidney disease: conclusions from a Kidney Disease: Improving Global Outcomes (KDIGO) Controversies Conference. Kidney Int 2021; 99: 34-47 4 Wetzels JFM et al.: Age- and gender-specific reference values of estimated GFR in Caucasians: the Nijmegen Biomedical Study. Kidney Int 2007; 72: 632-7 5 Inker LA et al.: Estimating glomerular filtration rate from serum creatinine and cystatin C. N Engl J Med 2012; 367: 20-9 6 Inker LA et al.: New Creatinine- and cystatin C-based equations to estimate GFR without race. N Engl J Med 2021; 385: 1737-49 7 Garg AX et al.: Albuminuria and renal insufficiency prevalence guides population screening: results from the NHANES III. Kidney Int 2002; 61: 2165-75 8 Price CP et al.: Use of protein:creatinine ratio measurements on random urine samples for prediction of significant proteinuria: a systematic review. Clin Chem 2005; 51: 1577-86 9 Chronic Kidney Disease Prognosis Consortium; Matsushita K et al.: Association of estimated glomerular filtration rate and albuminuria with all-cause and cardiovascular mortality in general population cohorts: a collaborative meta-analysis. Lancet 2010; 375: 2073-81 10 Skorecki K et al. (eds.): Brenner and Rector‘s The Kidney. 10th ed. Philadelphia: Elsevier; 2016
Das könnte Sie auch interessieren:
Les conjugués anticorps-médicament ont le vent en poupe
Actuellement, de nombreux conjugués anticorps-médicament sont en cours d’évaluation dans le cancer du poumon. Qu’ils soient utilisés seuls ou en combinaison avec d’autres thérapies ...
Effets sur la santé ainsi que risques liés au travail posté et de nuit
Le travail posté et de nuit entraîne un risque accru de multiples problèmes de santé en raison de la perte de sommeil et de la désynchronisation circadienne. Il s’agit notamment de ...
Les défis des interfaces interdisciplinaires
Face à un éventail croissant d’options ciblées et immunothérapeutiques, les tests moléculaires sont de plus en plus au centre de l’attention dans les tumeurs gastro-intestinales. Des ...