Réduction, voire arrêt des corticoïdes grâce à la biothérapie?
Compte-rendu:
Reno Barth
Journaliste médical
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Les corticoïdes oraux constituent le traitement de référence des exacerbations de l’asthme et sont également utilisés pour celles de la BPCO. Cette norme s’appuie toutefois sur des études anciennes menées sur un nombre de patient·es très limité au regard des critères actuels. À l’avenir, les médicaments biologiques pourraient également remplacer les corticoïdes dans les situations aiguës et réduire ainsi la toxicité du traitement.
Les exacerbations sont des aggravations aiguës d’une maladie chronique qui entraînent un recours accru aux ressources médicales. Dans le cas de l’asthme bronchique, cela signifie qu’un facteur déclenchant, comme une infection banale, renforce les symptômes au point d’entraîner des modifications pertinentes de la physiologie, de la fonction pulmonaire et de l’inflammation. «Les exacerbations sont aujourd’hui traitées de manière largement uniforme par des corticoïdes oraux et/ou des antibiotiques», explique la Pre Mona Bafadhel du King’s College de Londres. Cependant, l’utilisation de corticoïdes systémiques pose justement un problème considérable chez les patient·es qui connaissent des exacerbations fréquentes. «Aucun nouveau traitement n’a été développé pour les exacerbations depuis 50 ans. L’exposition des patient·es aux corticoïdes est élevée, le succès thérapeutique est de courte durée et les échecs thérapeutiques sont fréquents», a déclaré M. Bafadhel. Une semaine de traitement à une dose moyenne de corticoïdes suffit à augmenter considérablement le risque de septicémie, de thrombose veineuse et de fracture.1
Petites études sur les corticoïdes datant des années 1990
Alors pourquoi n’a-t-on pas réussi à développer de meilleurs traitements pour les exacerbations? M. Bafadhel attribue notamment cela à des définitions floues des exacerbations, largement basées sur les symptômes, aussi bien pour l’asthme que pour la BPCO. Les preuves sont limitées et une proportion importante de patient·es qui présentent des exacerbations fréquentes sont exclu·es des études cliniques. Cela concerne par exemple les fumeur·ses souffrant d’asthme, les patient·es n’ayant jamais fumé souffrant·es de BPCO et les patient·es souffrant à la fois d’asthme et de BPCO. De plus, les preuves disponibles sont anciennes. La plupart des études sur les corticoïdes dans les exacerbations de l’asthme datent des années 1990, c’est-à-dire d’une époque où les corticoïdes n’étaient pas utilisés par voie orale, mais par voie intraveineuse dans cette indication. Un total d’environ 500 patient·es ont été examiné·es dans le cadre de ces travaux, et toutes les études ne se sont pas révélées positives. Les corticoïdes systémiques pour la prévention de nouvelles crises d’asthme n’ont été étudiés que dans quatre études, dont une seule (celle portant sur la méthylprednisolone par voie intramusculaire) s’est terminée par un résultat positif, mais qui a donné lieu à une méta-analyse positive.2
Dans le cas de la BPCO, les preuves sur l’utilisation des corticoïdes pendant les exacerbations aiguës sont certes plus récentes, mais encore plus limitées. La plupart des études disponibles n’ont montré aucun avantage significatif, mais la méta-analyse donne un résultat tout juste significatif en faveur des corticoïdes.3 Moins de 500 patient·es ont également été étudié·es dans l’indication des exacerbations de la BPCO. Quoi qu’il en soit, les corticoïdes se sont avérés être associés à une mortalité accrue chez les patient·es souffrant de BPCO, en fonction de la dose.4
Les revues Cochrane concluent à la pertinence de l’utilisation des corticoïdes dans les exacerbations de l’asthme ou de la BPCO en l’absence d’alternatives, mais reconnaissent la nécessité de poursuivre les recherches.2,3
M. Bafadhel a néanmoins recommandé de considérer ces conclusions avec prudence.
Différents mécanismes peuvent être à l’origine des exacerbations
Il pourrait être pertinent de différencier les différents endotypes d’exacerbations. Ainsi, 30 à 50% des exacerbations de BPCO se caractérisent par un nombre élevé d’éosinophiles dans le sang, mais les exacerbations dominées par des bactéries ou des virus jouent également un rôle. Cela peut être démontré dans la pratique clinique quotidienne dans le sens d’un traitement personnalisé. L’orientation du traitement en fonction du nombre d’éosinophiles a fait l’objet de plusieurs études qui ont mis en évidence la non-infériorité clinique de cette stratégie, selon M. Bafadhel. De cette manière, il a été possible de réduire l’exposition aux corticoïdes, mais pas d’éliminer complètement les corticoïdes oraux.5–7 Aucune étude de ce type n’a été réalisée à ce jour dans l’indication de l’asthme.
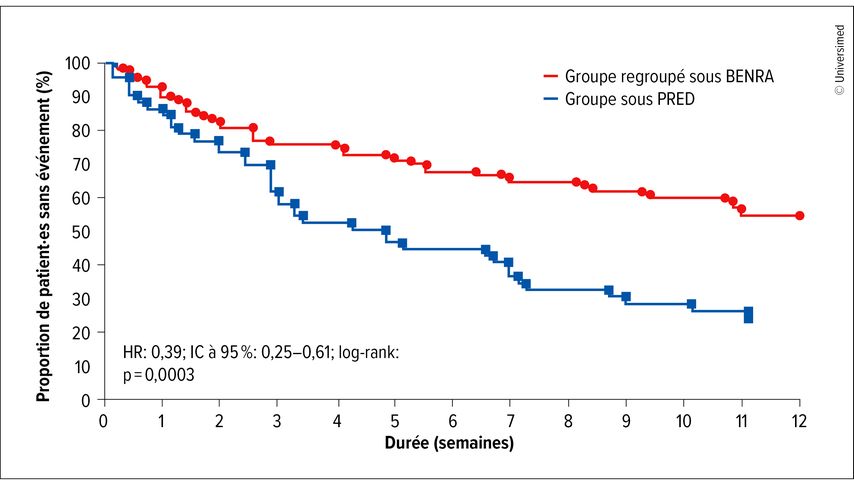
Les médicaments biologiques ciblant l’interleukine 5 pourraient constituer une alternative aux corticoïdes et ont fait leurs preuves depuis des années dans la gestion à long terme de l’asthme. Les données relatives aux situations aiguës font toutefois largement défaut. Il y a maintenant dix ans, une petite étude de preuve de concept a été menée sur le benralizumab dans les exacerbations de l’asthme en tant que traitement complémentaire aux corticoïdes oraux. L’étude n’a pas atteint son critère d’évaluation primaire, à savoir la prévention d’autres exacerbations dans les 12 semaines.8 L’étude ABRA, dans laquelle ont été inclus·es des patient·es souffrant d’asthme, de BPCO ou d’asthme et de BPCO au cours d’une exacerbation aiguë avec un nombre élevé d’éosinophiles, s’est révélée très fructueuse. Les critères d’évaluation primaires étaient la présence de symptômes au jour 28 et l’échec thérapeutique au jour 90. Les patient·es ont reçu soit de la prednisolone orale pendant cinq jours plus du benralizumab, soit de la prednisolone orale pendant cinq jours plus un placebo, soit un placebo plus du benralizumab. L’étude ABRA a atteint ces critères d’évaluation (Fig.1). En outre, aucune différence n’a été constatée entre le benralizumab en monothérapie et le benralizumab plus prednisolone. Ce résultat est resté constant dans tous les sous-groupes.9 L’utilisation du benralizumab a également réduit l’exposition cumulée aux corticoïdes sur 90 jours. Enfin, M. Bafadhel a aussi souligné les avantages en termes de coûts de la biothérapie qui n’ont pas encore été publiés: «la prednisolone est certes bon marché, mais elle ne fonctionne pas très bien. Et l’échec thérapeutique engendre des coûts considérables».
Fig.1: Étude ABRA: Courbe de Kaplan-Meier du délai écoulé jusqu’au premier échec thérapeutique dans le groupe de traitement sous prednisolone (prednisolone en monothérapie; PRED) et dans le groupe de traitement regroupé sous benralizumab (benralizumab en monothérapie et benralizumab plus prednisolone; BENRA) (modifiée selon Ramakrishnan S et al. 2025)9
Traitement d’entretien: réduction des besoins en corticoïdes sous tézépélumab
Dans le domaine du traitement d’entretien, la réduction des corticoïdes oraux est également un objectif thérapeutique important qui peut être atteint grâce aux médicaments biologiques. C’est ce qu’a montré récemment une analyse post-hoc de l’étude de phase IIIb WAYFINDER, présentée dans le cadre du congrès 2025 de l’ERS, qui a examiné la réduction des besoins en corticoïdes oraux sous tézépélumab en relation avec l’allergie et le nombre d’éosinophiles dans le sang.10
Dans l’étude WAYFINDER, les patient·es ont reçu 210mg de tézépélumab toutes les quatre semaines pendant une durée allant jusqu’à 52 semaines. Les critères d’évaluation coprimaires étaient les proportions de patient·es qui réduisaient leur dose d’entretien de corticoïdes oraux à ≤5mg/j ou les arrêtaient sans perdre le contrôle de leur asthme. Pour l’analyse actuelle, ces critères ont été évalués chez des patient·es avec ou sans allergie (FEIA+) et sur la base du nombre d’éosinophiles dans le sang à la référence (BEC; <300 et ≥300 cellules/μl). Une réduction et un arrêt de la dose d’entretien de corticoïdes oraux ont été observés dans tous les sous-groupes après 52 semaines. La population de patient·es la plus importante ayant atteint les critères d’évaluation coprimaires était celle des patient·es qui présentaient à la fois un asthme allergique et un BEC ≥300 cellules/μl. Les auteur·rices concluent de ces données que le traitement par le tézépélumab permet de réduire ou d’arrêter les corticoïdes oraux dans différents phénotypes d’asthme sans perdre le contrôle de l’asthme, la plus grande efficacité ayant été observée chez les patient·es souffrant à la fois d’asthme allergique et d’asthme éosinophile.
Source:
Congrès 2025 de l’ERS, du 27 septembre au 1er octobre 2025, à Amsterdam
Littérature:
1 Waljee AK et al.: Short term use of oral corticosteroids and related harms among adults in the United States: population based cohort study. BMJ 2017; 357: j1415 2 Rowe BW et al.: Corticosteroids for preventing relapse following acute exacerbations of asthma. Cochrane Database Syst Rev 2007; 3: CD000195 3 Walters JA et al.: Systemic corticosteroids for acute exacerbations of chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2009; 1: CD001288 4 Tse G et al.: A long-term study of adverse outcomes associated with oral corticosteroid use in COPD. Int J Chron Obstruct Pulmon Dis 2023; 18: 2565-80 5 Bafadhel M et al.: Blood eosinophils to direct corticosteroid treatment of exacerbations of chronic obstructive pulmonary disease: a randomized placebo-controlled trial. Am J Respir Crit Care Med 2012; 186: 48-55 6 Sivapalan P et al.: Eosinophil-guided corticosteroid therapy in patients admitted to hospital with COPD exacerbation (CORTICO-COP): a multicentre, randomised, controlled, open-label, non-inferiority trial. Lancet Respir Med 2019; 7: 699-709 7 Ramakrishnan S et al.: Blood eosinophil-guided oral prednisolone for COPD exacerbations in primary care in the UK (STARR2): a non-inferiority, multicentre, double-blind, placebo-controlled, randomised controlled trial. Lancet Respir Med 2024; 12: 67-77 8 Nowak RM et al.: A randomized trial of benralizumab, an antiinterleukin 5 receptor α monoclonal antibody, after acute asthma. Am J Emerg Med 2015; 33: 14-20 9 Ramakrishnan S et al.: Treating eosinophilic exacerbations of asthma and COPD with benralizumab (ABRA): a double-blind, double-dummy, active placebo-controlled randomised trial. Lancet Respir Med 2025; 13: 59-68 10 Brussele G et al.: OCS reduction with tezepelumab in OCS-dependent patients with severe allergic, eosinophilic asthma in WAYFINDER. ERS 2025; Poster #2485
Das könnte Sie auch interessieren:
Traitements pharmacologiques innovants dans la pneumopathie interstitielle diffuse
Plusieurs principes actifs sont actuellement en cours de développement dans le traitement de la fibrose pulmonaire idiopathique (FPI) et de la fibrose pulmonaire progressive (FPP), en ...
BPCO: identification de patients non diagnostiqués
De nombreuses personnes atteintes de BPCO et/ou d’asthme n’ont jamais été diagnostiquées et ne sont donc pas traitées. Plusieurs études publiées ces derniers mois se penchent sur ce ...
Diarrhée chronique: déroulement de l’examen
La diarrhée chronique est le symptôme de différentes maladies. Le Pr Alain Schoepfer a expliqué comment rechercher au mieux le facteur déclenchant dans son exposé lors du congrès annuel ...