Prise en charge chirurgicale – mise à jour
Auteurs:
Prof. Dre méd. Isabelle Schmitt-Opitz
Raphael Werner
Klinik für Thoraxchirurgie
Universitätsspital Zürich
Rämistrasse 100
8091 Zürich
E-mail: isabelle.schmitt-opitz@usz.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Le mésothéliome pleural malin (MPM) est un néoplasme rare mais extrêmement agressif de la plèvre viscérale et pariétale. Dans plus de 80 % de tous les cas de MPM, une exposition à l’amiante est considérée comme la cause. Cependant, il existe généralement une période de latence de 30 à 50 ans entre l’exposition et l’apparition de la maladie. Bien que l’incidence du MPM soit en recul dans la plupart des pays européens depuis l’interdiction de l’amiante dans les années 1990, il y a toujours menace d’augmentation significative du nombre de cas dans les pays du tiers monde en raison de l’utilisation continue de l’amiante.
Le traitement du MPM est complexe et nécessite une approche multidisciplinaire accompagnée d’une discussion de chaque cas individuel au sein d’un tumor board spécialisé dans l’oncologie thoracique. Alors qu’une chimiothérapie et/ou immunothérapie systémique est principalement recommandée pour les patients présentant des stades avancés, selon les lignes directrices actuelles et notre expérience, un traitement multimodal avec une chimiothérapie néoadjuvante à base de platine suivie d’une résection macroscopique complète permet d’obtenir une survie globale plus longue et une période sans récidive plus longue chez les patients présentant une maladie résécable. Le présent article vise à fournir une vue d’ensemble de la prise en charge chirurgicale du MPM sur la base des lignes directrices les plus récentes de l’American Society of Clinical Oncology (ASCO), de l’European Respiratory Society (ERS)/European Society of Thoracic Surgeons (ESTS)/European Association for Cardio-Thoracic Surgery (EACTS)/European Society for Radiotherapy and Oncology (ESTRO) Task Force et de l’European Society of Medical Oncology (ESMO).1-3
Diagnostic et stadification
Le soupçon initial de MPM est le plus souvent établi après le bilan cytologFique d’un épanchement ponctionné. Cependant, un diagnostic cytologique n’est pas suffisant pour planifier un traitement antinéoplasique adéquat et doit toujours être confirmé au niveau histologique par une biopsie pleurale thoracoscopique avant tout traitement. De quoi permettre de déterminer le sous-type histologique (épithélioïde, sarcomatoïde ou biphasique) et de réaliser un profilage moléculaire éventuel, et compléter la stadification clinique par une évaluation de la profondeur d’infiltration et de l’étendue intrathoracique du résultat observé. Une biopsie pleurale doit donc toujours s’étendre à la graisse sous-pleurale et être réalisée à partir de trois localisations différentes ou plus. Pour réduire le risque d’implantation de cellules tumorales dans la paroi thoracique, seuls 1–2 sites d’entrée thoracoscopiques doivent être utilisés. De préférence, ils sont placés dans l’espace intercostal de la résection macroscopique complète prévue au cours de l’évolution ultérieure.
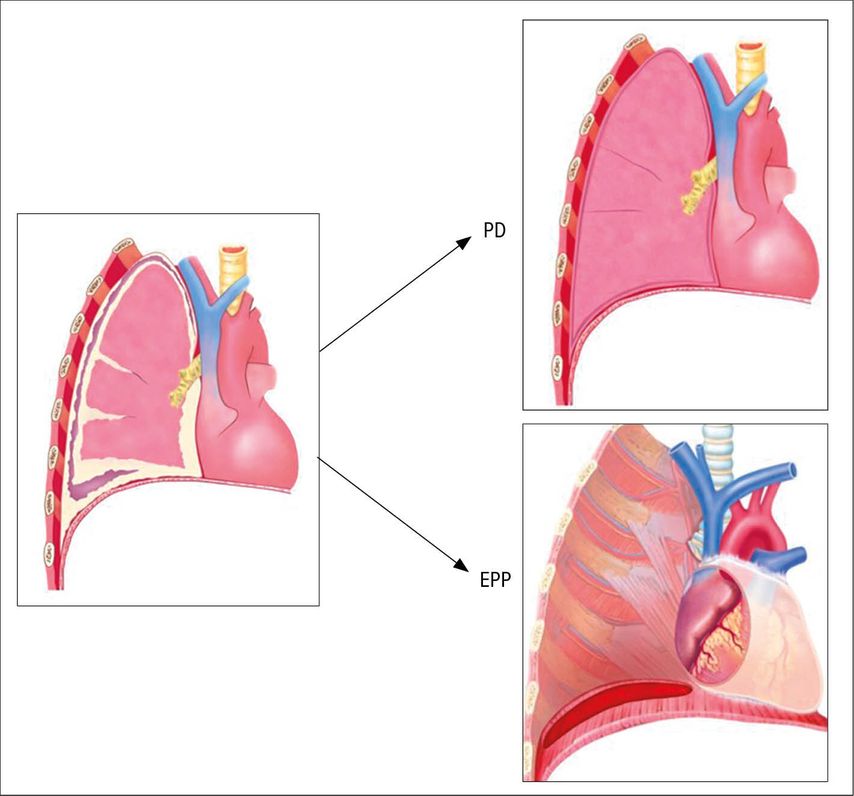
Fig. 1: Résection macroscopique complète (RMC) d’un mésothéliome pleural malin par pleurectomie et décortication (PD) ou pneumonectomie extrapleurale (PEP)
La stadification est réalisée par tomographie par émission de positons (TEP-CT) et est complétée par une médiastinoscopie ou une échographie endobronchique (EBUS) si l’on soupçonne une atteinte des ganglions lymphatiques médiastinaux, par une thoracoscopie controlatérale si l’on soupçonne une atteinte pleurale controlatérale, ou par une laparoscopie si l’on soupçonne une atteinte péritonéale. Une imagerie par résonance magnétique (IRM) du thorax peut également fournir des informations précieuses pour la stadification concernant une infiltration dans le diaphragme, la paroi thoracique, le péricarde ou le médiastin.
Résection macroscopique complète
Après une chimiothérapie néoadjuvante avec des cytostatiques contenant du platine et des antagonistes de l’acide folique, on procède à une nouvelle stadification par TEP-TDM ainsi qu’à une réévaluation de l’opérabilité. Une atteinte des ganglions lymphatiques péritonéaux, controlatéraux ou supraclaviculaires est considérée comme une contre-indication à la résection chirurgicale. Même chez les patients présentant un mésothéliome pleural sarcomatoïde confirmé histologiquement, aucune résection chirurgicale ne doit être pratiquée en dehors d’essais cliniques, compte tenu de la croissance agressive. En raison de la situation anatomique, à proximité des structures médiastinales, des distances de sécurité suffisantes ne peuvent être maintenues pendant une résection du MPM. Une résection radicale signifie donc dans ce cas une résection macroscopique complète dans le but d’une cytoréduction maximale, mais avec le risque d’une tumeur résiduelle microscopique. Une résection macroscopique complète peut être obtenue par pneumonectomie extrapleurale (PEP) ou pleuro-décortication élargie (PDE) préservant le parenchyme pulmonaire. Alors que la PEP implique une résection en bloc du poumon affecté avec la plèvre viscérale et pariétale ainsi que le diaphragme et le péricarde, la PDE ne fait que détacher et enlever la plèvre pariétale et viscérale ainsi que le diaphragme et le péricarde affectés, et le poumon est préservé. En l’absence de signes d’atteinte péricardique ou diaphragmatique, une pleuro-décortication (PD) isolée peut être choisie. Dans toutes les résections chirurgicales, une lymphadénectomie médiastinale systématique doit en outre être effectuée. Une PDE ou une PD préserve le parenchyme pulmonaire et les réserves fonctionnelles et permet au patient d’avoir une meilleure qualité de vie. De plus, étant donné que la PEP est associée à une morbidité et une mortalité péri-opératoires accrues, une PD(E) doit être pratiquée autant que possible. Une PEP doit exclusivement être envisagée dans des cas sélectionnés présentant une infiltration étendue du parenchyme pulmonaire et des réserves cardiopulmonaires suffisantes, et ne doit être réalisée que dans des centres expérimentés.
Interventions palliatives
Chez les patients pour lesquels une cytoréduction maximale par résection macroscopique complète n’est pas envisageable, la récurrence d’un épanchement pleural symptomatique peut être prévenue dans le cadre d’une approche palliative. Lorsque le poumon est dilaté, on procède à une pleurodèse par insufflation de talc par voie thoracoscopique; lorsque le poumon est piégé de façon chronique, on utilise un système de cathéter tunnelisé par voie sous-cutanée, qui peut également être utilisé pour drainer régulièrement l’épanchement à domicile.
Bilan
Chez des patients sélectionnés présentant un MPM localement limité et de bonnes réserves fonctionnelles, un concept de traitement multimodal avec chimiothérapie et résection macroscopique complète est recommandé. Les approches épargnant le parenchyme telles que la PD(E) devraient être privilégiées. Le traitement dans l’ensemble complexe doit être réalisé dans un centre spécialisé et évalué par un tumor board interdisciplinaire spécialisé dans l’oncologie thoracique. Les interventions palliatives telles que la pleurodèse par insufflation de talc par voie thoracoscopique ou l’insertion d’un système de cathéter tunnelisé sous-cutané peuvent contribuer au soulagement des troubles aux stades avancés.
Littérature:
1 Kindler HL et al.: Treatment of malignant pleural mesothelioma: American Society of Clinical Oncology Clinical Practice Guideline. J Clin Oncol 2018; 36: 1343-73 2 Opitz I et al.: ERS/ESTS/EACTS/ESTRO guidelines for the management of malignant pleural mesothelioma. Eur J Cardiothorac Surg 2020; 58: 1-24 3 Baas P et al.: Malignant pleural mesothelioma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2015; 26 Suppl 5: v31-9
Das könnte Sie auch interessieren:
BPCO: identification de patients non diagnostiqués
De nombreuses personnes atteintes de BPCO et/ou d’asthme n’ont jamais été diagnostiquées et ne sont donc pas traitées. Plusieurs études publiées ces derniers mois se penchent sur ce ...
Diarrhée chronique: déroulement de l’examen
La diarrhée chronique est le symptôme de différentes maladies. Le Pr Alain Schoepfer a expliqué comment rechercher au mieux le facteur déclenchant dans son exposé lors du congrès annuel ...
Réduction, voire arrêt des corticoïdes grâce à la biothérapie?
Les corticoïdes oraux constituent le traitement de référence des exacerbations de l’asthme et sont également utilisés pour celles de la BPCO. Cette norme s’appuie toutefois sur des ...