_Emanuel_Zitt.jpg)
Meilleure fiabilité du pronostic et
Compte-rendu:
Dre méd. Sabina Ludin
Rédactrice en chef
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
La néphropathie membraneuse est l’une des glomérulopathies les plus fréquentes. Dans le monde, l’incidence globale est d’environ 1/100000, la néphropathie membraneuse primaire représentant environ 80% des cas.1 Le rapport hommes/femmes est de 2:1. Au cours des deux dernières années, deux études intéressantes sur la néphropathie membraneuse ont été publiées. Elles ont été présentées par le Prof. Dr méd. Thomas Fehr, directeur médical, médecin-chef et chef du service de médecine interne à l’Hôpital cantonal des Grisons à Coire, lors de l’Update Refresher Médecine interne.
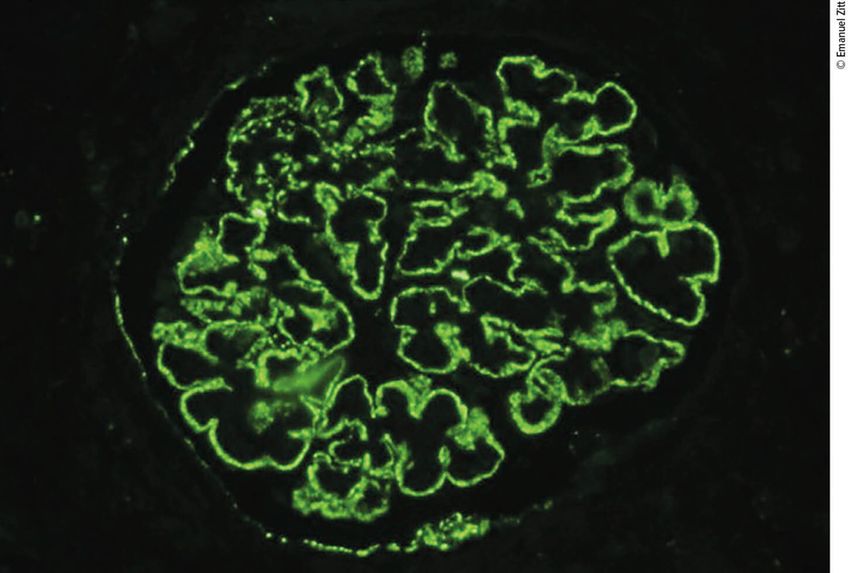
La néphropathie membraneuse primaire est une maladie auto-immune qui touche seulement les reins. Le principal auto-anticorps est dirigé contre un antigène podocytaire, le récepteur de la phospholipase A2 de type M (PLA2R) (Fig. 1). Les causes de la néphropathie membraneuse secondaire comprennent les tumeurs, les infections telles que l’hépatite B, le paludisme ou la syphilis, ainsi que les maladies systémiques telles que le lupus érythémateux et la polyarthrite rhumatoïde. D’un point de vue histologique, on observe un épaississement de la membrane basale avec des dépôts sous-épithéliaux de complexes immuns.
Fig. 1: Détection par microscopie à immunofluorescence de dépôts granulaires diffus de PLA2R dans la néphropathie membraneuse primaire associée à la PLA2R (avec l’aimable autorisation de: Zitt E: Nephrologie Universum Innere Medizin 2017; [4]: 30-1)
La néphropathie membraneuse appartient au groupe des glomérulonéphrites et se présente typiquement, sur le plan clinique, avec un syndrome néphrotique accompagné d’une protéinurie sévère. Une rémission spontanée survient chez un tiers des patients, un tiers des affections connaît une évolution progressive lente et un tiers connaît une évolution progressive rapide.
Meilleure fiabilité du pronostic avec la détermination combinée des Ac
Les patients atteints de néphropathie membraneuse peuvent présenter des auto-anticorps contre les antigènes podocytaires membraneux (PLA2R) et intracellulaires. Le groupe italien dédié à l’étude de la néphropathie membraneuse s’est penché sur la question de savoir s’il existe une corrélation entre la configuration de ces deux types d’auto-anticorps (Ac) et l’évolution clinique.2 Les auteurs ont trouvé des Acanti-PLA2R1 chez 64% des patients étudiés et, indépendamment de cela, des Ac contre les antigènes intracellulaires chez 65%.
Sur la base du profil sérologique, les patients ont été divisés en quatre groupes:
-
anti-PLA2R1+/intracellulaire+ (41%),
-
anti-PLA2R1+/intracellulaire– (22%),
-
anti-PLA2R1–/intracellulaire+ (22%) et
-
anti-PLA2R1–/intracellulaire– (11%).
L’analyse a montré que les patients chez qui aucun auto-anticorps n’a été détecté présentaient les meilleurs paramètres de protéinurie et de fonction rénale au moment de la pose du diagnostic et le plus faible risque de développer une insuffisance rénale dans les 12 mois. Les patients présentant des titres élevés d’Ac anti-PLA2R1 et chez qui on avait détecté des anticorps contre des antigènes intracellulaires avaient le risque le plus élevé d’évolution progressive rapide (odds ratio: 5,5; IC à 95%: 1,2–24; p=0,01).
«L’analyse sérologique combinée des auto-anticorps dirigés contre les antigènes des podocytes membranaires et intracellulaires permet d’identifier les patients dont le pronostic est mauvais», a résumé T. Fehr.
Traitement de la néphropathie membraneuse
Chez les patients présentant une faible protéinurie et une bonne fonction rénale, le traitement consiste dans l’administration d’un inhibiteur de l’ECA. En présence d’une protéinurie modérée et d’une fonction rénale stable, on débute le traitement également avec un inhibiteur de l’ECA. S’il n’y a pas d’effet après 6 mois, une immunosuppression est indiquée. En cas de syndrome néphrotique sévère et de déclin subaigu ou aigu de la fonction rénale, un traitement immunosuppresseur doit être démarré. Selon le protocole Cattran, qui s’est imposé au cours des 10 à 15 dernières années, le traitement standard consiste en l’administration de ciclosporine et de corticostéroïdes. Dans l’ancien protocole de Ponticelli, le traitement se compose de cyclophosphamide et corticostéroïdes. Les alternatives sont l’ACTH, l’aphérèse lipidique et le rituximab.
«Des séries de cas ont présenté à plusieurs reprises une bonne efficacité du rituximab, mais jusqu’à présent, il n’y avait pas de données contrôlées à ce sujet. Nous avons dû attendre que Cattran ait analysé son protocole contre le rituximab de façon randomisée dans le cadre de l’essai MENTOR»,3 a déclaré T. Fehr.
Étude MENTOR: rémission plus longue sous rituximab
L’étude a inclus 130 patients présentant une néphropathie membraneuse, une protéinurie dans la fourchette néphrotique (≥5g/24h), une fonction rénale relativement bonne (DFGe ≥40 ml/min/1,73m2) et au moins trois mois de traitement par un inhibiteur du SRAA.3 Tous les patients ont reçu le meilleur traitement d’appoint possible, notamment un inhibiteur du SRAA, une prise en charge de la pression artérielle et des mesures diététiques avec restriction du sel et des protéines. Ils ont été randomisés en deux groupes de traitement, selon un rapport de 1:1, et ont reçu en plus soit 1000mg de rituximab le jour 1 et le jour 15, soit 3,5mg/kgpc/j de ciclosporine. Un suivi intermédiaire a été effectué au bout de 6 mois. Si une diminution de la protéinurie d’au moins 25% était observée à cette date-là, mais qu’une rémission complète n’était pas encore atteinte, un deuxième cycle de rituximab a été effectué dans le groupe rituximab et le traitement a été poursuivi sans changement dans le groupe ciclosporine pendant 6 mois supplémentaires. En cas de rémission complète après 6 mois, le 2e cycle de rituximab a été supprimé et la ciclosporine a été progressivement abandonnée dans l’autre groupe et arrêtée après 2 mois. Une réduction de la protéinurie de <25% après 6 mois a été considérée comme un échec thérapeutique et le traitement a été arrêté.
Le critère d’évaluation primaire était la rémission complète (RC) ou partielle (RP) à 24 mois (RC: protéinurie <0,3g/24h et albumine sérique ≥3,5g/dl; RP: réduction de la protéinurie de ≥50% et protéinurie 0,3–3,5g/24h).
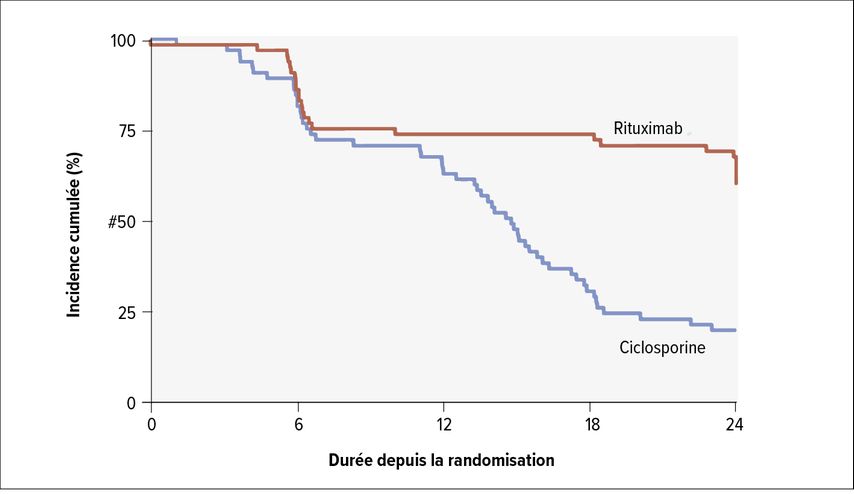
Après 12 mois, 60% des patients du groupe rituximab avaient obtenu une rémission complète ou partielle, contre 52% dans le groupe ciclosporine. Ainsi, le rituximab a satisfait aux critères de non-infériorité à 12 mois (p=0,004). Après 24 mois, 60% des patients du groupe rituximab étaient toujours en rémission complète ou partielle, contre seulement 20% dans le groupe ciclosporine. Ainsi, le rituximab satisfait aux critères de supériorité à 24 mois (p<0,001).
Comme critère d’évaluation secondaire, la durée jusqu’à l’échec du traitement a également été examinée; ceci est défini comme l’absence de RP/RC à 6 mois, la récidive (augmentation de la protéinurie à >3,5g/j) ou l’arrêt du traitement en raison d’effets secondaires. L’analyse a montré que 24 mois après le début de l’étude, 40% des patients dans le groupe rituximab et 80% dans le groupe ciclosporine ont connu un échec de traitement (HR: 0,34; IC à 95%: 0,21–0,54) (Fig. 2). Jusqu’à 12 mois, les courbes des deux bras de traitement sont quasi congruentes. Par la suite, c’est-à-dire après l’arrêt de la ciclosporine, l’activité de la maladie augmente à nouveau dans ce groupe, alors qu’une stabilisation a été obtenue dans le groupe rituximab jusqu’à 24 mois après l’entrée dans l’étude. «C’est très impressionnant. D’autant plus que le rituximab a été testé par rapport à la meilleure thérapie à ce jour», a indiqué T. Fehr. «Nous savons, par d’autres maladies auto-immunes, qu’il est possible d’administrer à nouveau du rituximab après cela ou d’instaurer un traitement d’entretien avec une administration tous les 12 mois pour maintenir la rémission. Cela pourrait être une bonne option dans la néphropathie membraneuse également.»
Source:
FomF Update Refresher Médecine interne, 1er au 5 décembre 2020
Littérature:
1 www.orpha.net 2 Ghiggeri GM et al.; Italian Study Group for Membranous Nephropathy: Multi-autoantibody signature and clinical outcome in membranous nephropathy. Clin J Am Soc Nephrol 2020; 15: 1762-76 3 Fervenza FC et al.; MENTOR Investigators: Rituximab or cyclosporine in the treatment of membranous nephropathy. N Engl J Med 2019; 381: 36-46
Das könnte Sie auch interessieren:
BPCO: identification de patients non diagnostiqués
De nombreuses personnes atteintes de BPCO et/ou d’asthme n’ont jamais été diagnostiquées et ne sont donc pas traitées. Plusieurs études publiées ces derniers mois se penchent sur ce ...
Diarrhée chronique: déroulement de l’examen
La diarrhée chronique est le symptôme de différentes maladies. Le Pr Alain Schoepfer a expliqué comment rechercher au mieux le facteur déclenchant dans son exposé lors du congrès annuel ...
Réduction, voire arrêt des corticoïdes grâce à la biothérapie?
Les corticoïdes oraux constituent le traitement de référence des exacerbations de l’asthme et sont également utilisés pour celles de la BPCO. Cette norme s’appuie toutefois sur des ...