Weitere DGU-Highlights zu Fortschritten in Therapie, Diagnostik und Digitalisierung
Autor:innen:
Dr. Heidemarie Ofner
Dr. Katharina Oberneder
Priv.-Doz. Dr. David DʼAndrea, FEBU
Universitätsklinik für Urologie
Medizinische Universität Wien
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Der 77. Kongress der Deutschen Gesellschaft für Urologie in Hamburg stand unter dem Motto „Urologie verbindet“. Vier Tage lang diskutierten Expert:innen aus Klinik und Forschung die neuesten Entwicklungen der Urologie. Im Zentrum des DGU-Kongresses standen translational-onkologische Themen, die künstliche Intelligenz in Diagnostik und Therapieplanung sowie Fragen der Nachhaltigkeit. Neben Leitlinien-Updates und großen Phase-III-Studien wurde die Bedeutung internationaler Kooperation und Forschung verdeutlicht, um die Versorgung von Patient:innen zu verbessern.
Keypoints
-
Enfortumab Vedotin + Pembrolizumab zeigt auch bei älteren oder komorbiden Patient:innen mit metastasiertem Urothelkarzinom eine hohe Wirksamkeit und ist damit eine vielversprechende Therapieoption in der klinischen Routine.
-
Innovative Bildgebung wie FAPI-PET/CT und Liquid-Biopsy-Verfahren verbessern die Genauigkeit der Diagnostik und das Verständnis tumorbiologischer Prozesse.
-
Die aktualisierten S3-Leitlinien zum Prostatakarzinom markieren einen Paradigmenwechsel hin zu risikoadaptierter, evidenzbasierter Früherkennung.
DGU-Highlights zum Urothelkarzinom
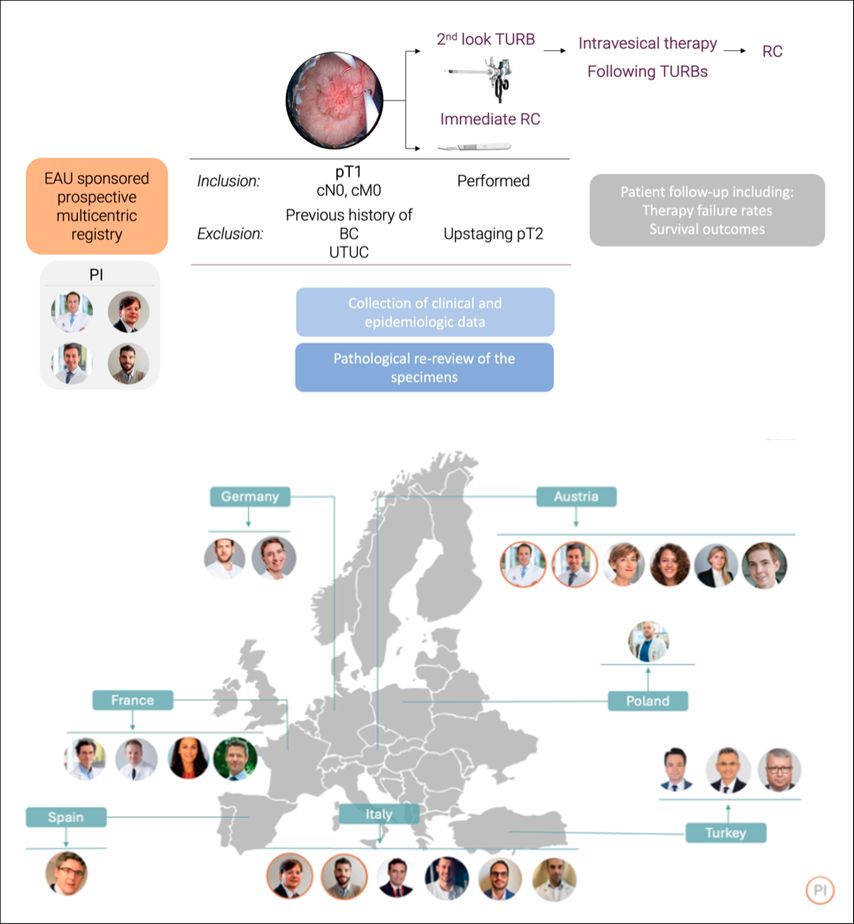
Das von der Europäischen Urologischen Gesellschaft (EAU) geförderte Projekt ROGUE-1 ist ein prospektives, multizentrisches Register für Patient:innen mit primärem pT1-High-Grade-Urothelkarzinom (Abb. 1). Ziel sind die europaweite Standardisierung und Verbesserung der Versorgung durch die Verknüpfung klinischer, pathologischer und verlaufsbezogener Daten.
Auf dem DGU-Kongress wurden zwei Analysen des Registers vorgestellt: In der ersten zeigte sich, dass eine strukturierte chirurgische Checkliste mit einer signifikant geringeren Rate an Residualtumoren beim Second-Look-Eingriff assoziiert war (24% Residualtumoren insgesamt; vollständige Resektion OR: 0,26; p=0,026).1 In der zweiten Analyse wurde geprüft, ob Residualtumoren die BCG-Wirksamkeit beeinflussen – im kurzen Follow-up ergab sich hierfür kein signifikanter Zusammenhang. Die Ergebnisse betonen den Wert standardisierter chirurgischer Abläufe und prospektiver Qualitätssicherung für eine optimierte Therapieplanung und Behandlung.1
Auch im Bereich der systemischen Therapie gab es spannende Einblicke in die sich rasch wandelnde Therapielandschaft, die zunehmend durch neue Antikörper-Wirkstoff-Konjugate und Immuntherapien geprägt ist. J. Bedke et al. präsentierten Daten der prospektiven EV-103-Studie, Kohorte H, zur neoadjuvanten Enfortumab- Vedotin(EV)-Monotherapie bei Cisplatin-ungeeigneten Patient:innen mit muskelinvasivem Urothelkarzinom.2 Nach drei Zyklen EV vor radikaler Zystektomie erreichten 37,5% der Behandelten eine pathologische Komplettremission (pCR), was sich in einem deutlich verbesserten ereignisfreien Überleben (EFS) widerspiegelte (3-Jahres-EFS 72,9% bei pCR vs. 46,4% ohne pCR). Diese Daten unterstreichen, dass EV auch als Monotherapie in der neoadjuvanten Situation eine potenzielle Option für Cisplatin-ungeeignete Patient:innen darstellen könnte.
Die Real-World-Studie GUARDIANS untersuchte eine vulnerable Patient:innenkohorte mit terminaler Niereninsuffizienz, reduziertem Leistungsstatus und/oder einem Alter ≥80 Jahre mit metastasiertem Urothelkarzinom.3 Diese in klinischen Studien oft unterrepräsentierte Kohorte zeigte bei einer Therapie mit Enfortumab Vedotin und Pembrolizumab (EV+P) eine objektive Ansprechrate von 54% und eine Krankheitskontrollrate von 74%. Diese Ergebnisse zeigen, dass EV+P in der klinischen Routine trotz hohen Alters oder reduzierter Nierenfunktion eine hochwirksame, wenngleich eng zu überwachende Option darstellen kann.
Auch in der Diagnostik wurden auf dem DGU neue Erkenntnisse vorgestellt. L. Unterrainer et al. verglichen die beiden PET/CT-Tracer [18F]F-FAPI-74 und [68Ga]Ga-FAPI-46 im prätherapeutischen Lymphknoten-Staging des Harnblasenkarzinoms mit der konventionellen CT.4 Beide FAPI-PET/CT-Verfahren zeigten eine deutlich höhere Sensitivität (bis zu 100% bei [18F]F-FAPI-74 vs. 30% in der CT) bei vergleichbarer Spezifität. Damit könnten FAPI-basierte PET/CT-Verfahren künftig die Genauigkeit des präoperativen Stagings wesentlich verbessern und insbesondere bei grenzwertigen Befunden einen klinischen Mehrwert bieten.
Beim Upper Tract Urothelial Carcinoma (UTUC) rückten nichtinvasive Biomarker in den Fokus. Die von S. Brönimann et al. präsentierte Studie „Non-invasive Tumor Genomic Profiling (Urine vs Plasma) in Patients with UTUC“ wurde mit dem 2. Vortragspreis (experimentell) ausgezeichnet.5 In der genomischen Analyse von 41 Patient:innen mittels UroAmp-Assay klassifizierten Urinproben über 90% der Fälle korrekt, während Plasma-Proben deutlich weniger sensitiv waren. Besonders die häufigeren TP53-Mutationen bei muskelinvasiven Stadien unterstreichen das Potenzial des Urin-basierten Genom-Profilings als nichtinvasives Diagnose- und Prognoseinstrument in der Urothelkarzinomdiagnostik.
DGU-Highlights zum Prostatakarzinom
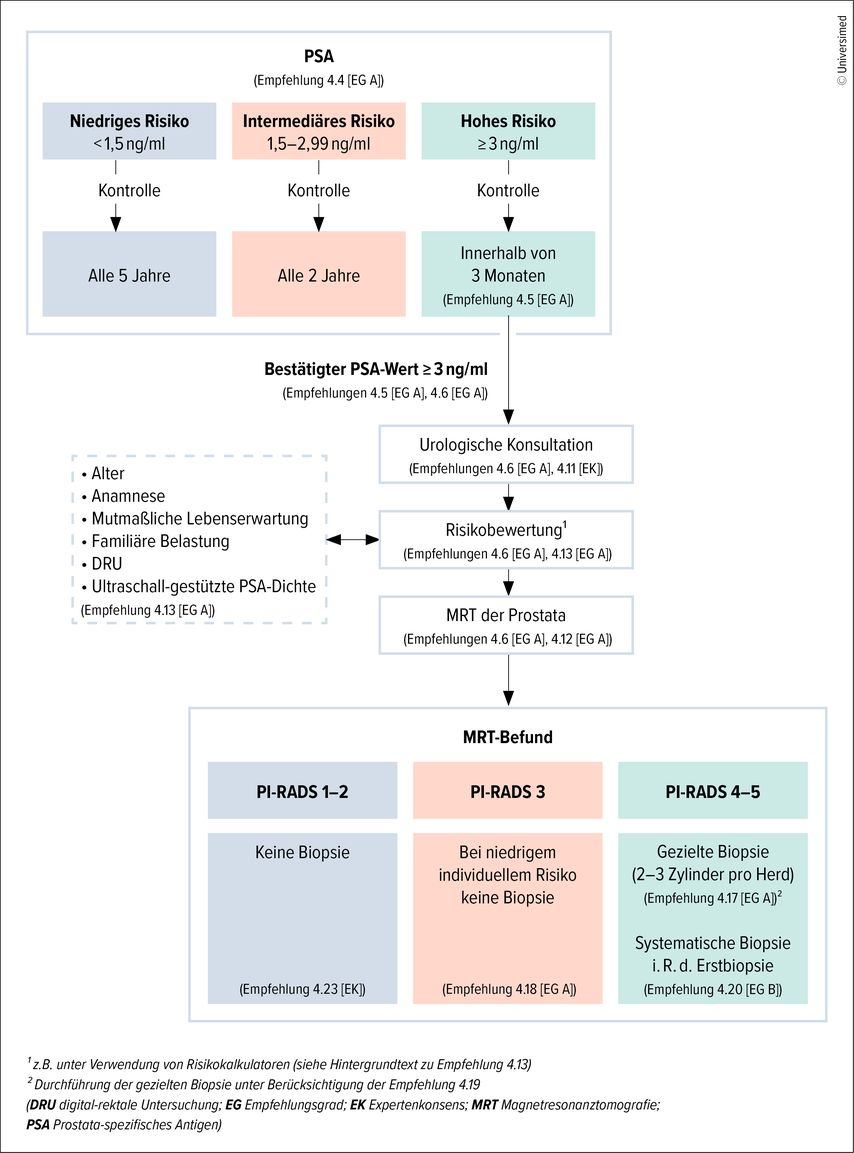
Ein zentrales Thema des DGU-Kongresses 2025 in Hamburg waren die Änderungen der S3-Leitlinie zum Prostatakarzinom, insbesondere im Bereich der Früherkennung. Erstmals wird darin eine negative Empfehlung für die digital-rektale Untersuchung (DRU) ausgesprochen – diese soll nicht mehr routinemäßig zur Krebsfrüherkennung eingesetzt werden, da sie anderen Tests, wie zum Beispiel der PSA-Testung, hinsichtlich Sensitivität und Spezifität deutlich unterlegen ist. Stattdessen empfiehlt die Leitlinie nun ein risikoadaptiertes, PSA-basiertes Screening für Männer ab 45 Jahren. Je nach PSA-Wert wird das Untersuchungsintervall individuell angepasst, wobei ab einem Wert von 3ng/ml eine weiterführende Abklärung empfohlen wird (Abb. 2). Die DRU bleibt Teil der individuellen Risikoabschätzung und kann in Einzelfällen ergänzend eingesetzt werden. Zudem wird die Rolle der multiparametrischen MRT (mpMRT) der Prostata deutlich gestärkt: Diese soll definitiv vor einer Biopsie durchgeführt werden, um nicht notwendige Eingriffe und damit potenzielle Überdiagnostik zu vermeiden; bei einem PI-RADS-1–2-Befund wird ausdrücklich von einer Biopsie abgeraten. Insgesamt unterstreichen die Neuerungen der S3-Leitlinie 2025 den Wandel hin zu einer personalisierten, evidenzbasierten und patientenzentrierten Prostatakrebsversorgung.6
Abb. 2: Algorithmus zur Früherkennung und Diagnostik des Prostatakarzinoms mit Verweis auf ausgewählte Empfehlungen (Leitlinienprogramm Onkologie, Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF, 2025)6
Im Bereich des lokalisierten Prostatakarzinoms präsentierten L. Graf et al. im Abstract „Biochemische Spätrezidive und Mortalität bei Patienten mit 10 Jahren rezidivfreiem Überleben nach radikaler Prostatektomie“ eine Analyse aus der Datenbank „Familiäres Prostatakarzinom“. Eingeschlossen waren Patienten, die zwischen 1986 und 2014 eine radikale Prostatektomie (RP) erhielten. Nach einem medianen Follow-up von 16,6 Jahren traten bei 504 von 4339 Patienten späte biochemische Rezidive auf (nach 10 Jahren). Von den 104 Todesfällen während des Beobachtungszeitraums waren jedoch nur 13 krebsspezifisch. Diese Ergebnisse zeigen, dass auch nach über zehn Jahren nach der initialen RPE noch ein Rezidivrisiko besteht, die tumorspezifische Mortalität jedoch hierbei sehr gering bleibt.7
In der Sitzung zur Systemtherapie des metastasierten hormonsensitiven Prostatakarzinoms (mHSPC) wurden unter anderem die Ergebnisse der Phase-III-Studie ARANOTE diskutiert. Die Studie untersuchte die Wirksamkeit und Sicherheit von Darolutamid in Kombination mit Androgendeprivationstherapie (ADT) im Vergleich zu ADT allein. In der Gesamtpopulation zeigte sich ein deutlicher Vorteil für Darolutamid + ADT, mit einer 46-prozentigen Reduktion des Risikos für radiologisches Fortschreiten oder Tod (HR: 0,54; 95% CI: 0,41–0,71; p<0,0001). Eine Subgruppenanalyse bestätigte diesen Vorteil sowohl bei Patienten mit hoher als auch mit niedriger Tumorlast nach CHAARTED- Kriterien. Eine weitere Subanalyse zeigte, dass eine ausgesprochen tiefe PSA-Therapieantwort (<0,02ng/ml) unter der Kombinationstherapie fünfmal häufiger erreicht wurde als unter ADT allein. Diese tiefen PSA-Therapieantworten korrelierten zudem mit einem signifikant verlängerten progressionsfreien Überleben und einer verzögerten Zeit bis zur Kastrationsresistenz und unterstreichen die Wirksamkeit der Kombinationstherapie weiter.8
Digitale Urologie
Auch die digitale Urologie nahm in Hamburg einen zentralen Platz ein. Im Rahmen der CONCORDIA-Studie untersuchten Rinderknecht et al., ob große Sprachmodelle (LLMs) wie ChatGPT-4 oder Claude 3,5 die Therapieempfehlungen multidisziplinärer Tumorboards abbilden können.9 Die Ergebnisse zeigen, dass weiterer Bedarf an Validierung und kontextueller Anpassung besteht, bevor eine Integration in die klinische Versorgung erfolgen kann.
Im Rahmen des KITTU-Projekts wurde ein erklärbares, KI-gestütztes System entwickelt, das auf Basis umfangreicher Patient:innendaten personalisierte Therapieempfehlungen für uroonkologische Erkrankungen erstellt.10 Das Projekt stellt einen wichtigen Meilenstein auf dem Weg zu einer standardisierten und transparenten Nutzung künstlicher Intelligenz in der klinischen Entscheidungsfindung dar.
Ausblick
Der DGU-Kongress 2025 zeigte eindrucksvoll, wie klinische Forschung und Standardisierung, molekulare Präzision und digitale Innovation die Uroonkologie gemeinsam voranbringen.
Während klinische Studien wie GUARDIANS und EV-103 neue Therapieoptionen etablieren und innovative Verfahren wie FAPI-Imaging und Liquid Biopsy präzisere Diagnosen ermöglichen, markieren die aktualisierten S3-Leitlinien zum Prostatakarzinom den Wandel hin zu einer risikoadaptierten, evidenzbasierten Versorgung.
Zugleich eröffnen KI-gestützte Systeme neue Perspektiven für eine standardisierte und personalisierte Entscheidungsfindung.
Literatur:
1 Oberneder K et al.: Association of surgical checklist with residual disease at second-look TURB and residual disease with response to BCG therapy: preliminary results from the ROGUE-1 multicenter register. DGU 2025, Abstract 635 + 641 2 Bedke J: EV-103 Study Cohort H: Neoadjuvant treatment with enfortumab vedotin (EV) monotherapy in cisplatin (cis)-ineligible patients with muscle-invasive bladder cancer (MIBC): 3-year efficacy results. Vortrag V18-01, 77. Kongress der Deutschen Gesellschaft für Urologie (DGU), Hamburg, 17.–20. September 2025 3 Darr C: Enfortumab vedotin + pembrolizumab in metastatic urothelial carcinoma – health insurance approval process in a German multicenter real-world cohort (GUARDIANS). Vortrag V18-08, 77. Kongress der Deutschen Gesellschaft für Urologie (DGU), Hamburg, 17.–20. September 2025 4 Unterrainer LM et al.: 68Ga-FAPI and 18F-FAPI PET/CT for detection of nodal metastases prior radical cystectomy in high-risk urothelial carcinoma patients. Eur J Nucl Med Mol Imaging 2025; 52(11): 3963-74 5 Brönimann S et al.: “Urine-and plasma-based tumor genomic profiling in patients with upper tract urothelial carcinoma”, DGU 2025, Abstract V05-05 6 Leitlinienprogramm-Onkologie (Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF): S3-Leitlinie Prostatakarzinom, Langversion 8.1, 2025, AWMF-Registernummer 043-022OL, www.leitlinienprogramm-onkologie.de/leitlinien/prostatakarzinom/ 7 Graf L et al.: Biochemische Spätrezidive und Mortalität bei Patienten mit 10 Jahren rezidivfreiem Überleben nach radikaler Prostatektomie, Technische Universität München, School of Medicine and Health, Klinik und Poliklinik für Urologie, Universitätsklinikum rechts der Isar der Technischen Universität München, München 8 Saad F et al.: Darolutamide in combination with androgen-deprivation therapy in patients with metastatic hormone-sensitive prostate cancer from the phase III ARANOTE trial. J Clin Oncol 2024; 42(36): 4271-81 9 Rinderknecht E: „Können multidisziplinäre uro-onkologische Tumorboards in ihren Therapieempfehlungen durch Large Language Models ersetzt werden? Ergebnisse der prospektiven, bizentrischen CONCORDIA-Studie“. Vortrag V13-01, 77. Kongress der Deutsche Gesellschaft für Urologie (DGU), Hamburg, 17.–20. Sept. 2025; 10 Duwe G et al.: Development of an artificial intelligence-generated, explainable treatment recommendation system for urothelial carcinoma and renal cell carcinoma to support multidisciplinary cancer conferences. Eur J Cancer 2025; 220: 115367
Das könnte Sie auch interessieren:
Frischer Wind in Hamburg – Highlights vom DGU 2025
Vom 17. bis 20.9.2025 fand in Hamburg der 77. Kongress der Deutschen Gesellschaft für Urologie (DGU) statt. Der Kongresspräsident Prof. Dr. Bernd Wullich betont in seinen Grußworten, ...
Active Surveillance beim Low-Risk-PCa: was uns Studien wirklich lehren
Active Surveillance (AS) bei Prostatakarzinom gewinnt unter den Ärzt:innen zunehmend an Akzeptanz. Patienten wünschen sich vermehrt Informationen dazu, um qualifiziert entscheiden zu ...
Klassifikationssysteme für intraoperative Komplikationen in der Urologie
Intraoperative Komplikationen gehören zum chirurgischen Alltag, deren systematische Erfassung ist jedoch in der Urologie nach wie vor lückenhaft. Vorhandene Klassifikationssysteme werden ...