Aktuelle Therapie des metastasierten Urothelkarzinoms
Autoren:
PD Dr. Daniela Colleselli
Dr. David Oswald
Dr. Birgit Kloss
Abteilung für Urologie
Landeskrankenhaus Salzburg
E-Mail: D.Colleselli@salk.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Nach jahrzehntelangem Stillstand hat in den letzten Jahren vor allem durch Einführung der PD-L1-Inhibitoren eine kontinuierliche Entwicklung in der Therapie und Prognose des metastasierten Urothelkarzinoms begonnen. Erstmals etablierten sich Alternativen zur konventionellen Chemotherapie, und auch in den Studien zur Zweit- und Drittlinientherapie konnten noch bemerkenswerte Ansprechraten erzielt werden.
Keypoints
-
Der aktuelle Erstlinienstandard für alle platintauglichen Patienten mit metastasiertem Urothelkarzinom ist die cisplatin- oder carboplatinhaltige Chemotherapie gefolgt von einer Avelumab-Erhaltungstherapie.
-
Die Checkpoint-Inhibitor-Monotherapie sollte in der Erstlinientherapie nur bei platinuntauglichen Patienten verabreicht werden. In der Zweitlinientherapie verfügt Pembrolizumab über die solideste Datenlage. Ebenfalls in dieser Indikation zugelassen sind die PD-L1-Inhibitoren Atezolizumab und Nivolumab.
-
Mit dem Antikörper-Wirkstoff-Konjugat Enfortumab Vedotin lassen sich selbst in der Drittlinie noch Ansprechraten von 44% erzielen.
-
Kombinationstherapien in verschiedensten Konstellationen sind derzeit Gegenstand der klinischen Forschung mit teils bemerkenswerten Ergebnissen in allen Therapielinien. Hier wird wahrscheinlich neben der Individualisierung der Therapie je nach molekularem Marker auch die Zukunft in der Therapie des Urothelkarzinoms liegen.
Erstlinienchemotherapie
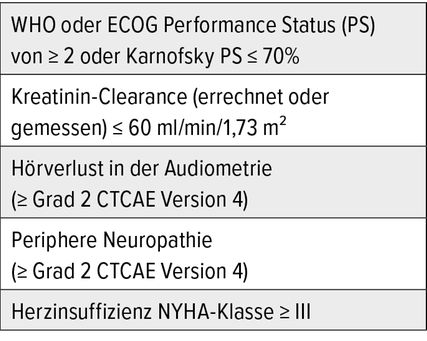
Seit den späten 1980er-Jahren ist die cisplatinhaltige Chemotherapie der Therapiestandard in der Erstlinientherapie des metastasierten Urothelkarzinoms. Die Kombinationstherapien Methrotrexat/Vinblastin/Adriamycin/Cisplatin (MVAC) bzw. Gemcitabin/Cisplatin (GC) verlängerten in einer randomisierten Phase-III-Studie das mediane Gesamtüberleben (OS) auf 14,8 bzw. 13,8 Monate.1 Das Ansprechen betrug 46% für MVAC (12% CR, 34% PR) und 49% für GC (12% CR, 37% PR). Eine Überlegenheit eines der beiden Regime zeigte sich nicht, jedoch kam es unter GC zu einer geringeren Anzahl an lebensbedrohlichen Toxizitäten wie Neutropenien oder Septitiden, weshalb sich die Kombination aus GC durchsetzen konnte. Allerdings erfüllen nach Anwendung von konsensbasierten Ausschlusskriterien2 nur ca. 30–50% aller Patienten die Voraussetzungen für den Erhalt einer cisplatinhaltigen Chemotherapie (Tab. 1).
Tab. 1: Ausschlusskriterien zur Anwendung einer cisplatinhaltigen Chemotherapie bei Urothelkarzinompatienten2
Die erste publizierte randomisierte Phase-II/III-Studie zur Chemotherapie (EORTC 30986) von cisplatinuntauglichen Patienten mit fortgeschrittenem Urothelkarzinom verglich Gemcitabin/Carboplatin (GCa) mit Methotrexat/Carboplatin/Vinblastin (M-CAVI) bei 237 Patienten.3 Die beiden Regime unterschieden sich nicht signifikant in ihrer Wirksamkeit (M-CAVI: medianes OS 8,1 Monate, 21% ORR; GCa: medianes OS 9,3 Monate, 36,1% ORR; ORR = objektive Ansprechrate). Aufgrund seiner geringen Toxizität kann GCa als Chemotherapiestandard bei cisplatinuntauglichen Patienten angesehen werden.
Cisplatintaugliche Patienten sollten eine cisplatinhaltige Therapie erhalten, da Carboplatin in diesem Kollektiv keine gleichwertige Alternative darstellt.
Checkpoint-Inhibitor-Monotherapie
Derzeit verfügen drei „Programmed death ligand-1“(PD-L1)-Inhibitoren über eine EMA-Zulassung in der Monotherapie des metastasierten Urothelkarzinoms.
Atezolizumab und Pembrolizumab erhielten 2017 zunächst eine uneingeschränkte FDA- und EMA-Zulassung in der Erstlinie bei cisplatinuntauglichen Patienten auf Basis der Phase-II-Studien IMvigor210 und KEYNOTE-052.4,5 Atezolizumab bzw. Pembrolizumab zeigten in einer Population von 119 bzw. 370 cisplatinuntauglichen Patienten eine ORR von 23% (CR-Rate von 9%) bzw. von 27% ORR (CR-Rate von 7%; CR = „complete response“).
Im Mai und Juni 2018 kam es jedoch durch die FDA und EMA zu einer Warnung bzw. Zulassungseinschränkung in der Erstlinientherapie auf Patienten mit einem positiven PD-L1-Status. Ausschlaggebend hierfür waren Zwischenauswertungen aus den Phase-III-Studien IMvigor130 und KEYNOTE-361, welche bei Patienten mit einem niedrigen PD-L1-Status ein kürzeres OS für die Therapie mit Atezolizumab oder Pembrolizumab im Vergleich zu den klassischen platinhaltigen Kombinationschemotherapien ergaben.6,7 Die Kriterien für die PD-L1-Positivität wurden jeweils mit einem IC (Anzahl tumorinfiltrierender Immunzellen) ≥5% bei Atezolizumab und einem CPS („combined positive score“) ≥10 bei Pembrolizumab definiert.
In der Zweitlinientherapie sind aktuell die PD-L1-Inhibitoren Pembrolizumab, Nivolumab und Atezolizumab als Monotherapie beim metastasierten Urothelkarzinom durch die EMA zugelassen, wobei Pembrolizumab aufgrund der vorliegenden Studien die solideste Datenlage vorweist.
In der randomisierten Phase-III-Studie KEYNOTE-045 wurden 542 Patienten bei Progress nach platinhaltiger Chemotherapie entweder mit Pembrolizumab oder einer Chemotherapie der Wahl (Vinflunin, Paclitaxel oder Docetaxel) behandelt.8 Dabei zeigte sich ein OS von 10,3 Monaten vs. 7,5 Monate (95% CI: 6,1–8,3). Der Überlensvorteil konnte unabhängig vom PD-L1-Status nachgewiesen werden.
Die Zulassung von Atezolizumab basiert auf den Ergebnissen der einarmigen Phase-II-Studie IMvigor210, in der eine ORR von 15% (95% CI: 11–19) erzielt wurde.4 Da die ORR in der Kohorte IC2/3 mit 26% (95% CI: 18–36) einen höheren Wert erzielte, sollte die Verlängerung des OS in dieser Gruppe auch der primäre Endpunkt in einer konfirmativen Phase-III-Studie (IMvigor211) sein, welcher jedoch überraschenderweise nicht erreicht werden konnte.9 Das mediane OS für die IC2/3-Population betrug in dieser Studie 11,1 Monate (95% CI: 8,6–15,5) im Atezolizumab-Arm und 10,6 Monate im Standardchemotherapie-Arm (95% CI: 8,4–12,2). In der gesamten Intention-to-treat-Gruppe konnte jedoch ein statistisch signifikanter Überlebensvorteil zugunsten der Atezolizumab-Therapie erzielt werden mit einem medianen OS von 8,6 Monaten (95% CI: 7,8–9,6) vs. 8,0 Monate (95% CI: 7,2–8,6) in der Chemotherapiegruppe.
Im Rahmen der Phase-II-Studie CheckMate 275 wurde bei 270 Patienten mit Nivolumab eine ORR von 19,6% und von 8,7 Monaten erreicht.10 Publizierte Phase-III-Daten zu Nivolumab in der Zweitlinie liegen bislang nicht vor.
Switch Maintenance
Durch die Etablierung der PD-L1-Inhibitoren in der Therapie des metastasierten Urothelkarzinoms wurden mehrere Ansätze verfolgt, diese auch in Kombination mit der Standardchemotherapie in der Erstlinientherapie anzuwenden. Dabei wurden u.a. die Kombinationen von Atezolizumab (IMvigor130) bzw. Pembrolizumab (KEYNOTE-361) mit einer platinhaltigen Chemotherapie gegenüber der alleinigen Chemotherapie verglichen.6,7 Obwohl in der Studie IMvigor130 ein Vorteil im progressionsfreien Überleben (PFS) für die Kombinationstherapie gezeigt werden konnte (8,2 Monate vs. 6,3 Monate), ergab sich kein Vorteil hinsichtlich des OS. Dieser konnte ebensowenig bei der Kombination von Chemotherapie und Pembrolizumab gezeigt werden, weshalb sich die Kombination aus Chemotherapie und Immuntherapie in der Erstlinienchemotherapie nicht etablieren konnte.
Ein neuer Ansatz wurde hingegen in der JAVELIN-Bladder-100-Studie angewandt.11 Im Rahmen der Studie erhielten platintaugliche Patienten vier bis sechs Zyklen einer Chemotherapie entweder mit Cisplatin oder mit Carboplatin. Patienten mit einem klinischen Benefit unter dieser Therapie, definiert als komplette Remission, partielle Remission oder „stable disease“, wurden im Anschluss an die Chemotherapie randomisiert und erhielten entweder eine Erhaltungstherapie mit dem PD-L1-Inhibitor Avelumab oder Best Supportive Care (BSC). Dabei zeigte sich ein signifikanter Überlebensvorteil für den Avelumab-Arm. Das mediane OS betrug 21,4 Monate (95% CI: 18,9–26,1) versus 14,3 Monate (95% CI: 12,9–17,9). Nach einem Jahr waren 71,3% der Patienten (95% CI: 66,0–76,0%) im Avelumab-Arm am Leben gegenüber 58,4% (95% CI: 52,7–63,7%) der Patienten, die nur BSC erhielten. Der Überlebensvorteil konnte in einer Reihe von Subgruppen bestätigt werden. Der positive Effekt war sowohl bei mit Cisplatin als auch mit Carboplatin behandelten Patienten (HR: 0,69 für GC versus 0,66 für GCa) nachweisbar. Vor allem Patienten mit PR oder SD konnten von der sogenannten Switch Maintainance mit Avelumab profitieren. Im Jahr 2021 erfolgte auch die EMA-Zulassung für die Erhaltungstherapie mit Avelumab nach platinhaltiger Chemotherapie, sodass diese gemäß NCCN- und EAU-Leitlinien auch als aktuelle Standardtherapie beim metastasierten Urothelkarzinom in der Erstlinie für alle platintauglichen Patienten empfohlen wird.
Antikörper-Wirkstoff-Konjugate
Als „First in class“-Antikörper-Wirkstoff-Konjugat hat Enfortumab Vedotin bereits die FDA-Zulassung in der Drittlinientherapie nach platinhaltiger Chemotherapie und Immuntherapie erhalten. Der Antikörper Enfortumab bindet an das Oberflächenprotein Nektin-4, welches bei Urothelkarzinomen hoch exprimiert wird. Es kommt zur Aufnahme des Antikörper-Wirkstoff-Konjugats in die Tumorzelle, wo Vedotin (Monomethylauristatin E) als Hemmstoff der Mikrotubuli zu einem Zellzyklus-Arrest und anschließender Apoptose führt.
Im Rahmen der Studie EV-201, einer Phase-II-Studie, zeigten sich bei progredienten Patienten mit Urothelkarzinom, welche bereits eine Chemotherapie und eine Immuntherapie erhalten hatten, ein bemerkenswertes objektives Ansprechen von 44% und eine CR von 12%.12 Ähnliche Ergebnisse ließen sich auch in den vordefinierten Subgruppen von Patienten mit Lebermetastasen (ORR 38%) oder fehlendem Ansprechen auf vorhergehende Immuntherapie (ORR 41%) erzielen. Die häufigsten Nebenwirkungen waren Fatigue (50%), periphere Neuropathie (50%), Alopezie (49%) und Hautausschläge (48%). Auf Basis dieser Daten wird auch die Zulassung in Europa für diesen Herbst dringlich erwartet.
Ebenfalls interessante Daten lieferte die Kombinationsstudie aus Enfortumab Vedotin in Kombination mit Pembrolizumab in der Erstlinientherapie von cisplatinuntauglichen Patienten.13 Hierbei zeigte sich bei 45 behandelten Patienten eine vielversprechende ORR von 73,3% mit einer CR von 15,6%. Eine randomisierte Phase-III-Studie (NCT04223856) zur Bestätigung dieser Ergebnisse ist derzeit im Laufen.
Mit Sacituzumab Govitecan erhielt ein weiteres Antikörper-Wirkstoff-Konjugat eine FDA-Zulassung in der Drittlinientherapie des metastasierten Urothelkarzinoms.14 Im Rahmen der TROPHY-U-01-Studie wurde bei platin- und immuntherapievortherapierten Patienten eine ORR von 27% erzielt. Auch hier erfolgte bereits die FDA- Zulassung, wobei sich die konfirmatorische Phase-III-Studie (NCT04527991) ebenfalls in der Rekrutierungsphase befindet.
FGFR-Inhibitoren
Alterationen im „fibroblast growth factor receptor“ (FGFR) kommen bei 10 bis 20% aller MIBC-Patienten vor und dort vor allem beim sogenannten luminalen Typ, welcher ein schlechteres Ansprechen auf Chemo- und Immuntherapien aufweist. Der orale Pan-FGFR-Inhibitor Erdafitinib erzielte in der einarmigen, offenen Phase-II-Studie bei Patienten mit bestimmten FGFR-2/3-Alterationen, die eine Progression nach platinhaltiger Therapie erlitten hatten, eine ORR von 40%, wovon 3% eine CR erreichten.15 Bei den 22 Patienten, die zuvor eine Immuntherapie mit einem PD-L1-Inhibitor erhalten hatten, kam es zu einer ORR von 59%. Das mediane progressionsfreie Intervall betrug 5,5 Monate und das mediane OS 13,8 Monate. Nebenwirkungen Grad 3 oder höher traten bei 46% der Patienten auf. 13% aller Studienteilnehmer mussten die Therapie aufgrund von Nebenwirkungen beenden, unter anderem wegen schwerer ophthalmologischer Nebenwirkungen. Eine Phase-III-Studie (NCT03390504), die Erdafitinib in der Zweitlinientherapie bei Urothelkarzinomen mit FGFR-Alterationen mit Docetaxel, Vinflunin oder Pembrolizumab vergleicht, ist bereits angelaufen.
Des Weiteren rekrutieren derzeit mehrere Studien, welche die Kombination aus FGRF-Inhibitoren und PD-L1-Inhibitoren beim metastasierten Urothelkarzinom untersuchen.
Literatur:
1 Van der Maase H et al.: Long-term survival results of a randomized trial comparing gemcitabine plus cisplatin, with methotrexate, vinblastine, doxorubicin, plus cisplatin in patients with bladder cancer. Clin Oncol 2005; 23: 4602-8 2 Galsky MD et al.: A consensus definition of patients with metastatic urothelial carcinoma who are unfit for cisplatin-based chemotherapy. Lancet Oncol 2011; 12: 211-4 3 De Santis M et al.: Randomized phase II/III trial assessing gemcitabine/ carboplatin and methotrexate/carboplatin/vinblastine in patients with advanced urothelial cancer „unfit“ for cisplatin-based chemotherapy: phase II--results of EORTC study 30986. J Clin Oncol 2009 27: 5634-9 4 Balar AV et al.: Atezolizumab as first-line treatment in cisplatin-ineligible patients with locally advanced and metastatic urothelial carcinoma: a single-arm, multicentre, phase 2 trial. Lancet 2017; 389: 67-76 5 Balar AV et al.: First-line pembrolizumab in cisplatin-ineligible patients with locally advanced and unresectable or metastatic urothelial cancer (KEYNOTE-052): a multicentre, single-arm, phase 2 study. Lancet Oncol 2017; 18(11): 1483-92 6 Galsky MD et al.: Atezolizumab with or without chemotherapy in metastatic urothelial cancer (IMvigor130): a multicentre, randomised, placebo-controlled phase 3 trial Lancet 2020; 395: 1547-57 7 Alva A et al.: LBA23 - Pembrolizumab (P) combined with chemotherapy (C) vs C alone as first-line (1L) therapy for advanced urothelial carcinoma (UC): KEYNOTE-361. Ann Oncol 2020; (Suppl 4): S1142-S1215 8 Bellmunt J et al.: Pembrolizumab as second-line therapy for advanced urothelial carcinoma. N Engl J Med 2017; 376: 1015-26 9 Powles T et al.: Atezolizumab versus chemotherapy in patients with platinum-treated locally advanced or metastatic urothelial carcinoma (IMvigor211): a multicentre, open-label, phase 3 randomised controlled trial. Lancet 2018; 391: 748-57 10 Sharma P et al.: Nivolumab in metastatic urothelial carcinoma after platinum therapy (CheckMate 275): a multicentre, single-arm, phase 2 trial. Lancet Oncol 2017; 18: 312-22 11 Powles T et al.: Avelumab maintenance therapy for advanced or metastatic urothelial carcinoma. N Engl J Med 2020; 383: 1218-30 12 Rosenberg JE et al.: Pivotal trial of enfortumab vedotin in urothelial carcinoma after platinum and anti-programmed death 1/programmed death ligand 1 therapy. J Clin Oncol 2019; 37: 2592-2600 13 Rosenberg JE et al.: Study EV-103: preliminary durability results of enfortumab vedotin plus pembrolizumab for locally advanced or metastatic urothelial carcinoma. J Clin Oncol 2020; 38(Suppl 6); abstr 441. doi: 10.1200/JCO.2020.38.6_suppl.441 14 Tagawa ST et al.: TROPHY-U-01: a phase II open-label study of sacituzumab govitecan in patients with metastatic urothelial carcinoma progressing after platinum-based chemotherapy and checkpoint inhibitors. J Clin Oncol 2021; 39: 2474-85 15 Loriot Y et al.: Erdafitinib in locally advanced or metastatic urothelial carcinoma. N Engl J Med 2019; 381: 338-48
Das könnte Sie auch interessieren:
Erstes „Da Vinci Single Port“-OP-System in Österreich
Seit März 2025 werden an der Klinik Oberwart robotisch assistierte Eingriffe mit dem „Da Vinci Single Port“(SP)-Operationssystem durchgeführt. Prim. Dr. Gottfried Pfleger berichtet über ...
PCNL-Indikationen in Zeiten von flexibler Ureterorenoskopie mit Absaugung?
In der Behandlung von Nierensteinen, die größer als 2cm sind, spielt die perkutane Nephrolithotomie (PCNL) weiterhin eine wichtige Rolle. Die flexible Ureterorenoskopie (URS) mit ...
Heutiger Stellenwert der ESWL: Renaissance in Sicht?
Die ESWL (extrakorporale Stoßwellenlithotrypsie) ist eine Technik zur urologischen Steintherapie, die in den 80er-Jahren des vorigen Jahrhunderts in den klinischen Alltag Einzug gehalten ...
.jpg)

