Respiratorisches Synzytial-Virus (RSV) – Neues aus der Prävention
Autorin:
Prof. Dr. Martina Prelog, MSc
Pädiatrische Rheumatologie/Spezielle Immunologie
Universitäts-Kinderklinik
Würzburg
E-Mail: martina.prelog@uni-wuerzburg.de
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Dank neuer Entwicklungen im Bereich der passiven wie auch aktiven Immunisierung gegen RSV stehen in der Praxis erfolgversprechende Konzepte zur Verfügung, um besonders vulnerable Gruppen wie Frühgeborene, immunologisch eingeschränkte Säuglinge und ältere Menschen vor RSV-assoziierten Komplikationen zu schützen.
Keypoints
-
Die RSV-Infektion induziert neutralisierende Antikörper.
-
Neutralisierende Antikörper gegen das Pre-Fusions(F)-Protein sind als passive Immunisierung mit Langzeitwirksamkeitfür Säuglinge zugelassen.
-
Neutralisierende Antikörper durch Protein-, Vektor-basierte- oder mRNA-Impfstoffe befinden sich in klinischen Zulassungsstudien.
-
Konzepte der aktiven Impfung: maternale Impfung, Säug-lingsimpfung und Impfung von Älteren
Einleitung
Beim respiratorischen Synzytialvirus (RSV) handelt es sich um ein einzelsträngiges, unsegmentiertes RNA-Virus aus der Familie der Pneumoviridae (Genus Orthopneumovirus), das über Tröpfcheninfektion und Oberflächen von Mensch zu Mensch übertragen wird. Innerhalb von durchschnittlich fünf bis sechs Tagen kommt es zu einer Erkrankung des oberen und/oder unteren Atemtraktes mit Erkältungssymptomatik, wie Schnupfen und Husten. Die bronchiale Obstruktion kann zur respiratorischen Insuffizienz mit Tachydyspnoe, Hypoxämien bis zu Apnoen führen.
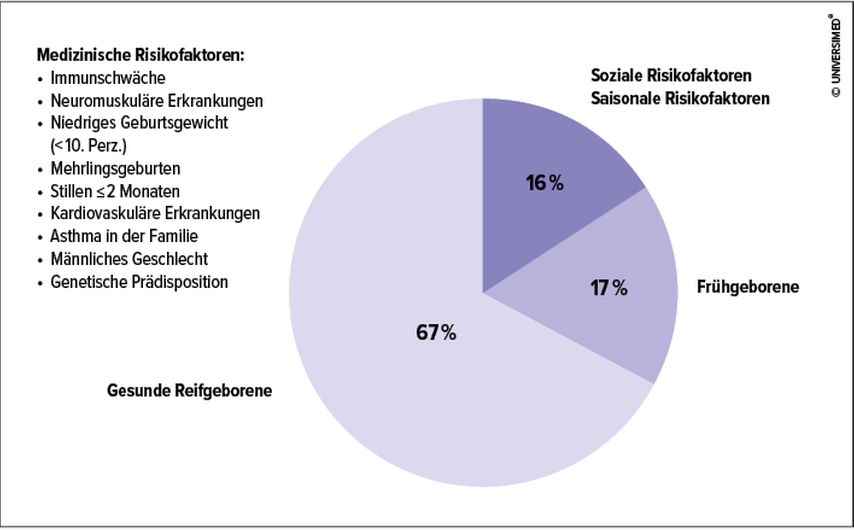
Von schweren Verläufen mit einer Erkrankung der unteren Atemwege sind vor allem junge Säuglinge und ältere Menschen betroffen. Besonders gefährdet sind Risikopopulationen, wie Frühgeborene, untergewichtige und vorerkrankte Säuglinge. Bis zu einem Alter von zwei Jahren haben über 90% aller Kinder einmal Kontakt zu RSV gehabt. Die hohe Krankheitslast in der Bevölkerung auch bei gesunden Säuglingen (Abb. 1) und die Gefahr von Komplikationen haben den Ruf nach einer Primärprävention in den letzten Jahren laut werden lassen. Derzeit stehen uns sowohl passive als auch aktive Immunisierungsstrategien zur Verfügung, die in der folgenden Übersicht besprochen werden.
Abb. 1: Gesundheitsassoziierte Parameter von aufgrund von RSV hospitalisierten Kindern ≤2 Jahren (modifiziert nach Ariola CS et al.: J Pediatric Infect Dis Soc 2020; 9(5): 587-95)
Pathogenese und Immunologie
Weltweit wird die Inzidenz von RSV-assoziierten Atemwegserkrankungen auf 48,5 Fälle und 5,6 schwere Fälle pro 1000 Kinder unter zwölf Monaten geschätzt, wobei die Letalität in Übersichtsarbeiten aus mehreren Primärstudien auf durchschnittlich 0,3% der Kinder ohne bekanntes Risiko, auf 1,2% bei Frühgeborenen, 4,1% bei vorbestehender bronchopulmonaler Dysplasie und auf 5,2% bei Kindern mit angeborenen Herzvitien geschätzt wird.
Das RSV ist von einer doppelschichtigen Lipidhülle umgeben, in die Glykoproteine integriert sind. Dazu gehören das Fusions-(F)- und das Adhäsions(G)-Protein. Es werden zwei Gruppen von RSV unterschieden, A und B, die in der Antigenstruktur des G-Proteins unterschiedlich sind.
RSV A ist bei uns dominant. Typisch ist die saisonale Häufung auf der Nordhalbkugel in den Wintermonaten mit Erkrankungsgipfel im Januar und Februar. Die SARS-CoV-2-Pandemie und die damit verbundenen Maßnahmen zur Eindämmung werden für eine aktuelle Verschiebung der Erkrankungshäufigkeiten verantwortlich gemacht.
Das RSV repliziert sich in den zilientragenden Schleimhautepithelzellen der Atemwege, wobei das F-Protein mit der namensgebenden Synzytienbildung assoziiert ist. Durch das Einwandern von unspezifischen und spezifischen Abwehrzellen kommt es zu einer inflammatorischen Reaktion, die durch eine Aktivierung von Granulozyten, Monozyten und Lymphozyten gekennzeichnet ist. Es kommt zu einer Induktion der T-Helfer-Zell-Typ-2(Th2)-Immunantwort, die auch bei Asthma bekannt ist. Inflammatorische Zytokine und Entzündungsmediatoren führen zu einer erhöhten mikrovaskulären Permeabilität, zu Ödem und Schwellung des peribronchialen Gewebes und zusammen mit abgelösten Epithelzellen und Zelldetritus durch die lytische Virusreplikation zu einer vermehrten Schleimbildung und Obstruktion. Zusätzlich kommt es zu einer Freilegung von nozizeptiven Nervenendigungen, die den Hustenreiz triggert. Die Erkrankung verläuft üblicherweise selbstlimitierend und nach mehreren Wochen kommt es zur Regeneration des Epithels. RSV induziert eine adaptive Immunantwort mit der Bildung von spezifischen T-Zellen und neutralisierenden Antikörpern. Reinfektionen sind trotzdem häufig, verlaufen aber meist milde.
Primärprävention durch passive und aktive Immunisierung
Allgemeine Hygienemaßnahmen helfen, das Risiko für eine RSV-Infektion zu minimieren, können es aber nicht ganz verhindern. Eine kausale antivirale Therapie steht nicht zur Verfügung.
Passive Immunisierung
Eine passive Immunisierung mit monoklonalen Antikörpern gegen das F-Protein des RSV ist zugelassen und wird monatlich während der RSV-Saison i.m. verabreicht, wobei die Schutzwirkung zwar nach der ersten Verabreichung schon eintritt, aber erst nach der zweiten Dosis das Wirkmaximum erreicht. Diese Prophylaxe ist jedoch besonderen Risikopopulationen wie Frühgeborenen oder kranken und immunkompromittierten Säuglingen vorbehalten.
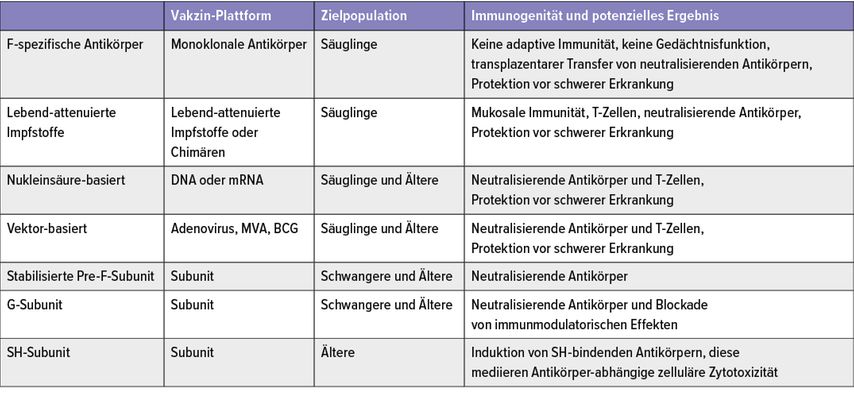
Gerade die jetzige Phase der abklingenden Pandemie hat gezeigt, dass das massive und verfrühte Zurückkehren der RSV-Infektion in allen Altersklassen nach Beendigung der Pandemie-assoziierten transmissionsverhindernden Maßnahmen ein bevölkerungsrelevantes Gesundheitsproblem darstellt. In dieser Situation machen die Strategien zur Verbesserung der passiven Immunprophylaxe und zur Entwicklung von aktiven Immunisierungen gegen RSV Hoffnung, dass in Kürze effektive RSV-Impfungen zur Verfügung stehen. Verschiedene Strategien zielen auf die aktive Impfung von Schwangeren, Neugeborenen und jungen Säuglingen sowie älteren Personengruppen ab (Tab. 1).
Tab. 1: Bisher erfolgreiche Impfstoffentwicklungskonzepte (modifiziert nachRuckwardt TJ et al.: Immunity 2019; 51: 429-42)
Im November 2022 zugelassen wurde ein monoklonaler Antikörper (Nirsevimab) gegen das Pre-F-Protein mit monatelanger Langzeitwirksamkeit und hoher Effektivität von 74,5% gegen RSV-assoziierte Infektionen der unteren Atemwege mit Notwendigkeit des Arztbesuchs und einer Effektivität von 62,1% gegen Hospitalisierungen bei früh- und reifgeborenen Kindern. Man macht sich mit diesen neutralisierenden Antikörpern die Besonderheit der Konformationsänderung des viralen Pre-F-Proteins zu Post-F-Protein zunutze, das für die Fusion mit der Zellmembran verantwortlich ist. Die biologische Wirksamkeit des viralen F-Proteins wird dadurch gehemmt („neutralisiert“), dass das F-Protein in der Präfusionskonformation blockiert wird. Dadurch ist es freien Virionen nicht mehr möglich, in die Zellen einzudringen, und die Ausbreitung des zellassoziierten Virus durch Zellfusion wird verhindert.
Aktive Immunisierung
Als aktive Immunisierungen sind derzeit Impfkonzepte als maternale Impfung in Erprobung. Für die maternale Impfung ist vor allem das dritte Schwangerschaftstrimenon geeignet, da hier physiologischerweise der aktive transplazentare Transfer von spezifischen IgG-Antikörpern auf den Fetus stattfindet. Derzeit liegen die Auswertungen einer Phase-IIb-Studie vor, die die Effektivität und Immunogenität einer Impfung gegen das Pre-F-Protein untersucht. Dabei zeigte sich eine Impfstoffeffektivität gegen RSV-assoziierte Infektionen von 84,7% und gegen schwere Infektionen von 91,5% bei den Säuglingen der in der Schwangerschaft geimpften Mütter. Der transplazentare Transfer von neutralisierenden Antikörpern auf die Kinder konnte nachgewiesen werden.
In einer Human-Challenge-Studie, bei der Erwachsene kontrollierten Infektionsbedingungen mit RSV ausgesetzt wurden, konnte das Konzept einer Erwachsenen-Impfung untersucht werden. Vorher geimpfte und danach kontrolliert infizierte Personen zeigten keine PCR-bestätigte symptomatische Infektion mit RSV im Vergleich zu Placebo (100% Effektivität).
Eine hohe Effektivität konnte auch eine Zulassungsstudie für einen mRNA-basierten Impfstoff, der codierende RNA-Sequenzen für Präfusionskonformation-stabilisiertes Glykoprotein F enthält, zeigen. Dieser Impfstoff ist in die gleichen Lipidnanopartikel verpackt wie ein Covid-19-mRNA-Impfstoff und führte zu einer Wirksamkeit von 83,7% bei Erwachsenen ab 60 Jahren bei einer guten Verträglichkeit.
Der Erfolg anderer Konzepte, wie Vektor-basierter Impfstoffe oder von „Scaffolds“ zur Verhinderung der Konformationsänderung des F-Proteins, wird sich zeigen.
Fazit
Mit den genannten Innovationen im Bereich der passiven wie auch aktiven Immunisierung gegen RSV stehen uns erfolgversprechende Konzepte zur Verfügung, um Risikogruppen wie Frühgeborene oder immunologisch eingeschränkte Säuglinge und ältere Menschen vor RSV-assoziierten Komplikationen, wie Bronchiolitis und Pneumonie, zu schützen. Das Verständnis der biologischen und immunologischen Vorgänge bei der viralen Attacke gegen die Epithelzellen der Atemwege macht es möglich, spezifische neutralisierende Antikörper zu entwickeln beziehungsweise durch eine aktive Immunisierung vom körpereigenen Immunsystem produzieren zu lassen und somit erfolgreich RSV-assoziierte Arztkonsultationen und Hospitalisationen zu vermeiden. Dabei stehen uns die Möglichkeiten der maternalen Impfung, der Impfung von Säuglingen und alten Menschen zur Verfügung.
Literatur:
bei der Verfasserin
Das könnte Sie auch interessieren:
Long-Covid-Rehabilitation 2025 – von der klinischen Erfahrung zur Evidenz
Seit 2020 hat sich die Rehabilitation bei Covid-19 und Long Covid von ersten Erfahrungsberichten hin zu einer evidenzbasierten Maßnahme entwickelt. Aktuelle Studien belegen, dass ...
Asthma bronchiale: Herausforderungen bei Kindern und Jugendlichen
Asthma bronchiale ist eine chronische Krankheit, die im Kindesalter andere Herausforderungen mit sich bringt als bei Erwachsenen. Die physikalische Untersuchung sowie die Therapie sind ...