Antikörpertherapie bei COPD
Bericht:
Reno Barth
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Mit Dupilumab und Mepolizumab sind mittlerweile zwei Biologika in der Indikation COPD zur Reduktion des Exazerbationsrisikos zugelassen. Einige weitere Biologika wurden und werden in dieser Indikation in klinischen Studien untersucht. Die dabei beobachteten, zum Teil widersprüchlichen Ergebnisse werden allerdings nur teilweise verstanden. In Zukunft könnten mit Antikörpern auch neue Therapieziele und Komorbiditäten anvisiert werden.
Bis vor relativ kurzer Zeit spielten Biologika im Management der COPD keine Rolle. Das hat sich mit der Zulassung des Anti-IL-4/IL-13-Antikörpers Dupilumab (EMA-Zulassung seit 2024) und des Anti-IL-5-Antikörpers Mepolizumab (derzeit nur von der FDA zugelassen) in dieser Indikation geändert. Allerdings sind Biologika aktuell vor allem eine Option für Patienten mit einem eosinophilen Phänotyp und häufigen Exazerbationen trotz maximaler inhalativer Therapie. Das Forschungsinteresse richtete sich initial vor allem auf die Gruppe der gegen IL-5 oder den IL-5-Rezeptor gerichteten Antikörper wie Mepolizumab oder Benralizumab, erläuterte Prof. Dr. Gerard J. Criner von der Lewis Katz School of Medicine an der Temple University in Philadelphia, der auch darauf hinwies, dass die ersten Biologikastudien in der Indikation COPD ein unklares Bild ergaben. Dies änderte sich mit den Phase-III-Studien BOREAS mit Dupilumab1 und MATINEE mit Mepolizumab2, die beide signifikante Reduktionen des Exazerbationsrisikos in den behandelten Patientenpopulationen zeigten.
Patientenselektion liefert Informationen für klinischen Alltag
Hinsichtlich dieses genannten primären Endpunkts sind die Ergebnisse der beiden Studien einander recht ähnlich, so Criner, bei den sekundären Endpunkten zeigen sich allerdings interessante Unterschiede. Während sich nämlich in BOREAS (Dupilumab) die Lungenfunktion und die Lebensqualität der Patienten signifikant verbesserten, war dies in MATINEE mit Mepolizumab nach einem Jahr nicht der Fall. Mögliche Erklärungen, die auch für Empfehlungen im klinischen Alltag relevant sein können, liefert ein Blick auf die Patientenselektion, so Criner. Beispielsweise litten alle Patienten in den Dupilumab-Studien unter chronischer Bronchitis, während dies in Mepolizumab-Studien keine Voraussetzung für den Einschluss war.
Die MATINEE-Population umfasste COPD-Patienten mit GOLD-Grad 2–4, während in BOREAS nur GOLD-2- und -3-Patienten eingeschlossen waren. In MATINEE konnte man mit jedem Dyspnoe-Grad aufgenommen werden, in BOREAS nur mit Dyspnoe-Grad 2–4. Die Lebensqualität bei Einschluss war in BOREAS etwas besser als in MATINEE. Auch Subgruppenanalysen deuten auf unterschiedliches Ansprechen in unterschiedlichen Patientenpopulationen hin. So war mit Mepolizumab die Reduktion der Exazerbationsrate bei Patienten in GOLD 3 oder 4 ausgeprägter als in GOLD 2. Dafür verbesserte sich mit Mepolizumab die Lebensqualität vor allem in GOLD 2. Relevant ist auch die Laufzeit der Studien, denn im zweiten Behandlungsjahr von MATINEE trat auch eine Verbesserung der Lungenfunktion im Vergleich zu Placebo ein. Dies zeige, so Criner, dass Biologikatherapien unter Umständen mehr Zeit benötigen, um ihre volle Wirkung zu entfalten.
Als Beispiel für die Komplexität der Situation nannte Criner die mit Benralizumab durchgeführte Phase-III-Studie RESOLUTE, die laut Informationen des Herstellers den primären Endpunkt verfehlte, obwohl die Studienpopulation auf Basis zweier vorhergegangener Studien selektiert worden war.3 Voraussetzungen für den Einschluss waren häufige Exazerbationen und eine Eosinophilenzahl im Blut von mindestens 300 Zellen/μl unter maximaler inhalativer Therapie.
Alarmine als Ziel für Interventionen
Typ-2-Inflammation ist jedoch nicht das einzige potenzielle Ziel für die Biologikatherapie bei COPD. Untersucht werden auch Strategien, bei den Alarminen, den Zytokinen des Epithels, anzusetzen. Antikörper gegen „thymic stromal lymphopoietin“ (TSLP) bieten die Option, sowohl den T2- als auch den T1/T17-Signalweg zu blockieren. Ebenso bietet IL-33 einen möglichen Angriffspunkt. Sowohl für IL-33 als auch für TSLP konnten Assoziationen mit erhöhtem Exazerbationsrisiko nachgewiesen werden.4 Die klinischen Konsequenzen sind noch unklar.
Der Anti-IL-33-Antikörper Itepekimab bewirkte in der Phase-II-Studie in einer COPD-Population keine Reduktion des Exazerbationsrisikos. Subgruppenanalysen zeigten jedoch, dass Itepekimab bei ehemaligen Rauchern, nicht jedoch bei aktuellen Rauchern oder Nichtrauchern, sehr wohl wirksam war.5 Auf Basis dieser Daten wurden zwei Phase-III-Studien durchgeführt, die die Lage noch undurchsichtiger machten. Während in AERIFY-1 der primäre Endpunkt nach 52 Wochen erreicht wurde, war das in AERIFY-2 nicht der Fall. Obwohl in der Frühphase der Studie alles auf einen Erfolg hingedeutet hatte. Die Hintergründe sind unklar, eine mögliche Erklärung liegt in einer insgesamt sehr niedrigen Ereignisrate, da die Studie während der Covidpandemie durchgeführt wurde.
Astegolimab ist ein monoklonaler Antikörper gegen den IL-33-Rezeptor ST2, der ebenfalls in der Indikation COPD untersucht wird. Die Phase-II-Daten aus der Studie ALIENTO, die eine Reduktion moderater oder schwerer Exazerbationen um 15,4% dokumentieren, wurden im Rahmen des Kongresses vorgestellt.6 In ARNASA, einer zweiten Phase-II-Studie, wurde eine numerische Reduktion von Exazerbationen in ähnlicher Größenordnung beobachtet, diese verfehlte jedoch die Signifikanz. Criner: „Die genauere Auswertung der Daten in den kommenden Wochen wird hoffentlich mehr Einsicht in diese Ergebnisse bringen.“
Auch für Tozorakimab, einen Antikörper gegen IL-33, liegen widersprüchliche Daten aus der Phase II vor. Diese waren jedoch ausreichend positiv, um die Initiation mehrerer Phase-III-Studien zu rechtfertigen. Auch mit dem gegen TSLP gerichteten Tezepelumab wurde in einer Phase-II-Studie der primäre Endpunkt Reduktion des Exazerbationsrisikos verfehlt. Hier zeigen jedoch Subgruppenanalysen bei Patienten mit höherer Eosinophilenzahl im Blut einen sehr deutlichen Behandlungseffekt.7
Neue Therapieziele: „mucus plugs“ und Komorbiditäten
Auch neue klinische Therapieziele bei COPD werden in Angriff genommen. Criner wies darauf hin, dass ungünstige Effekte von „mucus plugging“ (Mukusimpaktion) bei COPD ein häufiges Problem darstellen, das sich auf die Lungenfunktion, die Lebensqualität, das Exazerbationsrisiko und die Mortalität ungünstig auswirkt. Bei Asthmapatienten konnte für mehrere Biologika eine Reduktion des „mucus plugging“ gezeigt werden. Für die COPD fehlen entsprechende Daten bislang.
Ein weiteres relevantes Ziel ist die neutrophile Inflammation, die bislang durch die verfügbaren Therapien kaum beeinflusst werden kann. Criner wies auf eine Studie hin, die bei Patienten mit Bronchiektasie eine Reduktion des Exazerbationsrisikos durch Brensocatib zeigen, einen oralen Inhibitor der Dipeptidylpeptidase1.8 In die Studie waren auch Patienten mit COPD eingeschlossen. In dieser Subgruppe war Brensocatib ebenso wirksam wie in der Gesamtpopulation. Bislang wurde jedoch nicht untersucht, ob Brensocatib auch bei COPD-Patienten ohne Bronchiektasie Vorteile bringt.
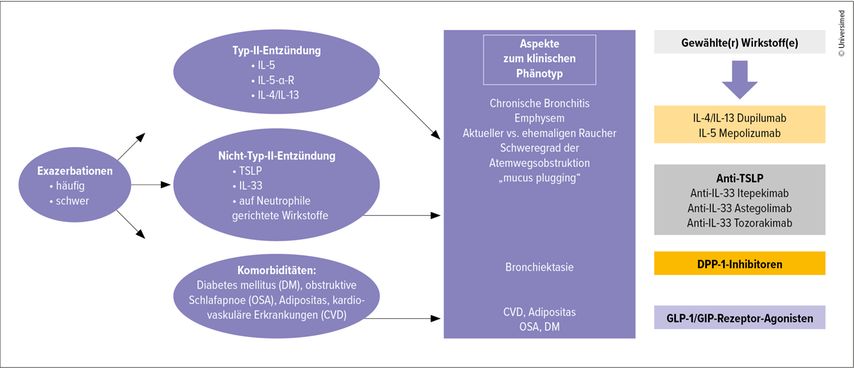
Nicht zuletzt eröffnen Biologika auch die Möglichkeit, verschiedene bei COPD häufige Komorbiditäten zu beeinflussen (Abb.1). Dies betrifft beispielsweise die Gruppe der GLP-1-Rezeptor-Agonisten (GLP-1-RA), die zur Behandlung von Typ-2-Diabetes und Adipositas eingesetzt werden. Retrospektive Studiendaten zu einer Population von Patienten mit COPD und komorbidem Typ-2-Diabetes zeigen, dass das Risiko für COPD-Exazerbationen mit den eingesetzten Antidiabetika korrelierte, wobei GLP-1-RA, gefolgt von SGLT2-Inhibitoren, mit dem niedrigsten Risiko assoziiert waren.9 Allerdings ist nicht klar, ob GLP-1-RA das Exazerbationsrisiko auch bei COPD-Patienten senken, die nicht unter komorbidem Diabetes leiden.
Abb. 1: Integration des klinischen Phänotyps mit endotypischen Faktoren (modifiziert nach Criner GJ 2025)
Quelle:
„Biologics in COPD: targeting the right pathways for the right treatments“, Vortrag von Prof. Dr. Gerard J. Criner, Philadelphia; ERS Congress, 30. September 2025
Literatur:
1 Bhatt SP et al.: Dupilumab for COPD with type 2 inflammation indicated by eosinophil counts. N Engl J Med 2023; 389(3): 205-14 2 Sciurba FC et al.: Mepolizumab to prevent exacerbations of copd with an eosinophilic phenotype. N Engl J Med 2025; 392(17): 1710-20 3 https://www.astrazeneca.com/media-centre/press-releases/2025/update-on-resolute-phase-iii-trial.html ; zuletzt aufgerufen am 8.10.2025 4 Joo H et al.: Association between plasma interleukin-33 level and acute exacerbation of chronic obstructive pulmonary disease. BMC Pulm Med 2021; 21(1): 86 5 Rabe KF et al.: Safety and efficacy of itepekimab in patients with moderate-to-severe COPD: a genetic association study and randomised, double-blind, phase 2a trial. Lancet Respir Med 2021; 9(11): 1288-98 6 Greening N et al.: Randomised, placebo-controlled trial of astegolimab for COPD with frequent exacerbations: ALIENTO. ERS 2025, Presentation #1116 7 Singh D et al.: Efficacy and safety of tezepelumab versus placebo in adults with moderate to very severe chronic obstructive pulmonary disease (COURSE): a randomised, placebo-controlled, phase 2a trial. Lancet Respir Med 2025; 13(1): 47-58 8 Chalmers JD et al.: Phase 3 trial of the DPP-1 inhibitor brensocatib in bronchiectasis. N Engl J Med 2025; 392(16): 1569-81 9 Foer D et al.: Association of GLP-1 receptor agonists with chronic obstructive pulmonary disease exacerbations among patients with type 2 diabetes. Am J Respir Crit Care Med 2023; 208(10): 1088-1100
Das könnte Sie auch interessieren:
Nichttuberkulöse Mykobakterien (NTM): Klinik, Diagnose und Therapie
Infektionen mit nichttuberkulösen Mykobakterien nehmen global signifikant zu. Die Unterscheidung von Kolonisation, transienter Infektion und NTM-Erkrankung kann klinisch sehr schwierig ...
Innovative Pharmakotherapien bei ILD
Derzeit befinden sich mehrere Wirkstoffe für die Behandlung von idiopathischer pulmonaler Fibrose (IPF) und progredienter pulmonaler Fibrose (PPF) in der Entwicklung, wobei verschiedene ...