Übersicht über Melasmabehandlungen
Autor:innen:
Firat Aslanel
FMH Facharzt für Dermatologie und Venerologie
Stv. ärztliche Leitung
Cand. med. Rosa Sonnentag
Hautwerk AG, Zürich
E-Mail: klinik@hautwerk.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Das Melasma bleibt eine der hartnäckigsten und am schwierigsten zu behandelnden Hyperpigmentierungen. Aufgrund der chronisch-rezidivierenden Natur stellt es für Betroffene und Behandelnde eine grosse Herausforderung dar. Moderne Therapiekonzepte setzen auf multimodale Ansätze, die topische, systemische und gerätebasierte Verfahren intelligent kombinieren. Dieser Artikel bietet einen aktuellen Überblick über die wirksamsten Strategien mit einem besonderen Fokus auf innovative Laser- und Lichttechnologien.
Keypoints
-
Multimodal statt Monotherapie: Die Kombination aus Photoprotektion, topischen Regimen, ggf. oraler Tranexamsäure und gezielten Geräteverfahren erzielt nachhaltigere Resultate.
-
Dermales Targeting-Denken: Melasma als Photoaging-Phänotyp behandeln – seneszente Fibroblasten, Gefässe und Entzündung modulieren.
-
Sicherheit vor Aggressivität: Bei dunkleren und asiatischen Hauttypen Low-fluence-Strategien (1064nm Nd:YAG «Nano-Toning») und tiefes RFMN bevorzugen; zu oberflächliche/energiereiche Protokolle erhöhen das PIH-Risiko.
-
Erhaltung ist Pflicht: getönter LSF50+ (mit Eisenoxiden), hydrochinonfreie Regime, Antioxidanzien und kontrollierte Auffrischungen zur Rezidivprophylaxe.
Das Melasma ist eine erworbene chronische Störung der Hautpigmentierung, die sich klinisch durch symmetrisch verteilte, meist scharf begrenzte bräunliche Makulae und Plaques manifestiert. Sie betrifft vor allem sonnenexponierte Hautareale, insbesondere das Gesicht.1,2
Eine erhöhte Prävalenz findet sich bei Personen mit Herkunft aus dem Nahen Osten, Ostasien, dem mediterran-afrikanischen Raum sowie aus Südamerika. Besonders häufig betroffen sind dabei Frauen im dritten bis vierten Lebensjahrzehnt sowie Personen mit dunkleren Hauttypen (Fitzpatrick III–IV). Das sichtbare Hautbild führt nicht selten zu emotionalem Leidensdruck, verminderter Lebensqualität und gesellschaftlicher Stigmatisierung.1–5
Therapeutisch gilt das Melasma als besonders herausfordernd. Oft ist es therapieresistent, erfordert häufig multimodale Behandlungsansätze und neigt auch nach erfolgreicher Behandlung zu Rezidiven. Angesichts dieser Schwierigkeiten ist eine strukturierte Übersicht über die derzeit verfügbaren und neuen Behandlungsoptionen von hoher Relevanz, um evidenzbasierte Versorgung sicherzustellen und die Versorgung der betroffenen Patienten zu verbessern.1–3
Pathogenese des Melasmas
Die Entstehung des Melasmas ist multifaktoriell und beruht auf einem Zusammenspiel genetischer, hormoneller und umweltbedingter Einflüsse. Besonders ultraviolette Strahlung und sichtbares Licht, insbesondere hochenergetisches blaues Licht (400–500nm), sowie hormonelle Faktoren (z.B. Schwangerschaft, orale Kontrazeptiva) und exogene Trigger gelten als Hauptauslöser.5,6
Histologisch zeigen sich Veränderungen in mehreren Hautkompartimenten. Aktivierte melanogene Signalwege steigern die Melaninproduktion, während UV-exponierte Fibroblasten «stem cell factor» (SCF) freisetzen, der über c-kit die Melanogenese anregt. Seneszente Fibroblasten exprimieren «pro-aging»-assoziierte Mediatoren und Wnt-Signalweg-Komponenten, eine reduzierte WIF-1-Expression und Aktivierung von β-Catenin verstärken diesen Effekt.
UV-induzierte Matrixmetalloproteinasen (MMP-2, MMP-9) und Mastzellmediatoren schädigen die Basalmembran, wodurch Melanozyten in tiefere Hautschichten absinken («pendulous melanocytes») und Pigment in der Dermis verbleibt. Mastzellen fördern zusätzlich über Histamin, Tryptase und «vascular endothelial growth factor» (VEGF) Angiogenese, Matrixabbau und solare Elastose.5–7
Melasma stellt somit keine rein epidermale Hyperpigmentierung dar, sondern eine epidermal-dermale Erkrankung mit Merkmalen des Photoagings. Diese Komplexität erklärt die häufige Therapieresistenz und hohe Rezidivneigung und unterstreicht die Notwendigkeit multimodaler Therapieansätze.
Therapieoptionen: aktueller Stand und Innovationen
Photoprotektion
Der konsequente tägliche Lichtschutz ist die Basis jeder Melasmatherapie. UV- und sichtbares Licht stimulieren kontinuierlich die Melanogenese, weshalb eine ganzjährige Anwendung von Breitspektrumpräparaten (LSF 50+) unabdingbar ist. Besonders getönte Formulierungen mit Eisenoxiden schützen zusätzlich vor sichtbarem Licht. Zink- und Titandioxid wirken als physikalische UV-Filter, Antioxidanzien (Vit. C, E) neutralisieren freie Radikale und depigmentierende Zusätze wie Niacinamid oder Süssholzextrakt verbessern den Effekt. Ohne adäquaten Lichtschutz sind alle depigmentierenden Massnahmen wenig wirksam und Rezidive häufig.1,5
Topische Standardtherapien
Hautaufheller wie Hydrochinon (2–4%) gelten als Goldstandard. Es hemmt die Tyrosinase und reduziert die Melanozytenaktivität, erfordert aber dermatologische Kontrollen. Azelainsäure (10–20%) und Kojisäure wirken schwächer, sind aber besser verträglich.4,8
Retinoide (v.a. Tretinoin) beschleunigen den epidermalen Zellumsatz, vermindern solare Elastose und verbessern die Penetration anderer Wirkstoffe.4,9
Die Kligman’sche Triple-Kombination (Hydrochinon + Retinoid + Kortikosteroid) bleibt die effektivste topische Formulierung. Sie sollte aber nur kurzfristig und unter Kontrolle eingesetzt werden, um Nebenwirkungen wie Atrophie und Teleangiektasien zu vermeiden.4,8,9
Neue topische Substanzen
Thiamidol (Isobutylamido-Thiazolyl-Resorcinol) hemmt die Tyrosinase hochselektiv und zeigt eine vergleichbare Wirksamkeit wie Hydrochinon bei besserer Verträglichkeit.10 Cysteamin wirkt antioxidativ sowie melaninhemmend und eignet sich bei Hydrochinon-Unverträglichkeit.2
Tranexamsäure wirkt über die Hemmung der Plasminogenaktivierung auch auf vaskuläre und entzündliche Komponenten. In topischer Form ist sie variabel wirksam, mittels laserassistierter Drug Delivery oder Microneedling jedoch mit erhöhter Penetration und Effektivität.2
Experimentelle Ansätze
Neue Strategien zielen auf alternative Signalwege: Methimazol hemmt Peroxi- dasen und zeigte in Studien deutliche Aufhellungen ohne systemische Effekte. Auch topisches Omeprazol reduziert die Tyrosinaseaktivität. Innovative siRNA-Konzepte, die den Transkriptionsfaktor MITF hemmen, befinden sich noch in frühen Entwicklungsphasen, zeigen aber erste Erfolg versprechende Resultate.1
Tranexamsäure
Tranexamsäure (TXA) gilt heute als wichtigste systemische Option beim Melasma. Sie hemmt die Plasminogenaktivierung und unterbricht plasminabhängige Signalwege zwischen Keratinozyten und Melanozyten. Dadurch werden UV-induzierte Entzündung, Mastzellaktivität und angiogene Faktoren reduziert. Zusätzlich stimuliert TXA die Autophagie in Keratinozyten und fördert so den Abbau von Melanosomen.3,11 Prospektive Studien zeigen signifikante Verbesserungen des modifizierten Melasma Area and Severity Index (mMASI; ≈50%) unter 250–500mg zweimal täglich über acht bis zwölf Wochen. Höhere Dosen beschleunigen den Wirkungseintritt, steigern aber nicht die Gesamtwirksamkeit.12,13 TXA ist in der Regel gut verträglich. Kopfschmerzen, Dysmenorrhö oder gastrointestinale Beschwerden sind selten. Bei sorgfältiger Patientenselektion bleibt das Thrombose-Risiko gering; bei thrombotischen Vorerkrankungen oder Risikofaktoren (z.B. Rauchen, orale Kontrazeptiva) sind regelmässige Gerinnungskontrollen und enge dermatologische Überwachung erforderlich, um seltene Komplikationen wie venöse Thromboembolien zu minimieren. Trotz Off-Label-Status gilt TXA gemäss internationalen Leitlinien als evidenzbasierte Erstlinienoption bei moderatem bis schwerem Melasma, jedoch nur unter dermatologischer Kontrolle und individueller Risikoabschätzung.14,15
Orale Antioxidanzien
Orale Antioxidanzien können oxidativen Stress und UV-induzierte Entzündung mindern. Pycnogenol (Pinus-pinaster-Extrakt) zeigte in Studien mMASI-Redukt- ionen von rund 50% und wirkt dabei antioxidativ, antiinflammatorisch sowie gefässstabilisierend. Polypodium leucotomos (PLE) zeigte dagegen uneinheitliche Ergebnisse; der Nutzen ist unklar. Insgesamt sind Antioxidanzien als adjuvante, nicht als primäre Therapie zu verstehen.2
Chemische Peelings
Chemische Peelings eignen sich zur adjuvanten Behandlung refraktärer Fälle. Sie entfernen pigmentierte Keratinozyten und verbessern die Penetration topischer Wirkstoffe.
-
Glykolsäure (GA, 20–70%) ist am besten untersucht und zeigt in Kombination mit Triple-Therapie oder Azelainsäure signifikante MASI-Verbesserungen.16,17,18
-
Salicylsäure (SA, 20–30%) und Milchsäure (LA) sind milder, zeigen ähnliche Wirksamkeit bei geringerer Irritation und postinflammatorischer Hyperpigmentierungsrate.19,20
-
Trichloressigsäure (TCA, 10–20%) ist effektiv, birgt aber höhere Nebenwirkungsrisiken.21,22
-
Tretinoin-Peelings (1–10%) induzieren rasch epidermale Regeneration und beschleunigen die Depigmentierung.23
Das Hauptrisiko aller Peelings bleibt die postinflammatorische Hyperpigmentierung (PIH), besonders bei dunklen Hauttypen.24 Oberflächliche, wiederholte Anwendungen mit präventivem Priming (z.B. 2% Hydrochinon) und konsequenter Photoprotektion sind entscheidend.1–3
Hauttyp-spezifische Strategien
Bei dunkleren und asiatischen Hauttypen besteht ein deutlich höheres Risiko für PIH und Rebound-Phänomene.25
-
Topisch: Zyklische Therapie mit aktiver (z.B. Triple-Kombination) und anschliessender hydrochinonfreier Erhaltungsphase reduziert Reizungen.25,26
-
Peelings: nur oberflächliche, milde Verfahren anwenden; tiefe Peelings vermeiden.24,25
-
Laser/Energie: Schonende Systeme mit tiefer Penetration und geringer Mela-ninabsorption sind zu bevorzugen. Der Low-fluence Q-switched Nd:YAG-Laser (1064nm, «Nano-Toning») ist dabei Methode der Wahl; er fragmentiert das Pigment subzellulär, ohne Melanozyten zu schädigen (Abb.1A+B).25,27 Beim Radiofrequenz-Mikroneedling (RFMN) sollten tiefere Nadeltiefen gewählt werden, um die Energie gezielt in die Dermis zu leiten und epidermale Reizung zu vermeiden.
-
Lichtschutz & Pflege: Breitspektrumfilter mit Schutz gegen sichtbares Licht (400–500nm) sowie barrierestärkende Pflege sind Pflicht.25
Ein behutsamer, multimodaler Ansatz, der Melanogenese hemmt und gleichzeitig die dermale Integrität bewahrt, bleibt entscheidend – ein «One size fits all»-Konzept existiert nicht.25,26
Schwerpunkt: Laser- und lichtbasierte Therapien – ein detaillierter Überblick
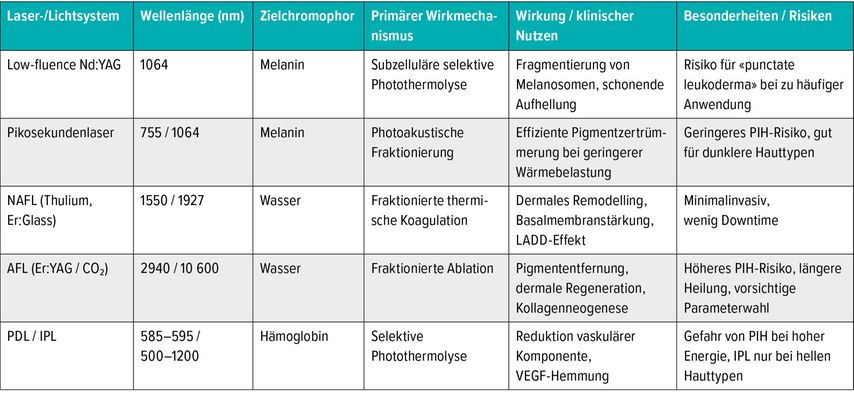
Laser- und Lichtsysteme wirken beim Melasma adjuvant, indem sie vorhandenes Pigment in Epidermis und Dermis reduzieren. Sie ersetzen jedoch nicht die Basistherapie, welche die Melaninsynthese hemmt. Laserbehandlungen sind nur im Rahmen eines multimodalen Gesamtkonzepts sinnvoll und ersetzen keine photoprotektiven oder topischen Massnahmen. Ihr Einsatz erfordert präzise Kenntnis der Pathophysiologie, um Nebenwirkungen wie PIH oder Hypopigmentierungen zu vermeiden (Tab.1).1,27
Low-fluence Nd:YAG-Laser
Der 1064-nm-Nd:YAG-Laser gilt als Standard für das «laser toning». Niedrige Fluenz und hohe Wiederholungsraten führen über subzelluläre Photothermolyse zur Fragmentierung der Melanosomen, ohne Melanozyten zu zerstören. Das Pigment wird anschliessend über Keratinozyten und Makrophagen abgebaut. Zu intensive Behandlungen können jedoch punktförmige Hypopigmentierungen verursachen.1,27
Pikosekundenlaser
Pikosekundenlaser erzeugen überwiegend photoakustische Effekte, die das Pigment schonend zerlegen. Die geringe Wärmeentwicklung reduziert PIH-Risiken und macht die Methode besonders für dunklere Hauttypen geeignet. Studien zeigen eine vergleichbare Wirksamkeit wie Nanosekundenlaser bei geringerer Nebenwirkungsrate.1,25,27
Nichtablative fraktionierte Laser (NAFL)
NAFL (1550/1927nm) erzeugen mikrothermische Koagulationszonen, fördern die Dermisremodellierung und eliminieren seneszente Fibroblasten. Sie verbessern die Basalmembran und ermöglichen durch «laser-assisted drug delivery» (LADD) eine bessere Wirkstoffpenetration, etwa für Tranexamsäure oder Vitamin C. Der 1927-nm-Thulium-Laser ist wegen seiner oberflächlichen Wirkung besonders geeignet (Abb.2A+B).1,25,27
Abb. 2: Ergebnis nach drei Behandlungen mit LADD von Tranexamsäure mittels Thulium-Laser im Abstand von jeweils vier Wochen
Ablative fraktionierte Laser (Er:YAG, CO₂)
Diese Systeme erzeugen mikroskopische Ablationskanäle zur Pigmententfernung und Regeneration. Der Er:YAG-Laser (2940 nm) arbeitet präzise mit geringer Wärmebelastung, der CO2-Laser (10600nm) wirkt tiefer, geht aber mit längerer Downtime einher. Aufgrund des PIH-Risikos ist Zurückhaltung geboten.1,6,25,27
Vaskuläre Laser und IPL
Da VEGF aus dilatierten Gefässen die Melanogenese stimuliert, kann die Gefässreduktion therapeutisch sinnvoll sein. «Pulsed dye laser» (PDL; 585/595nm) und «intense pulsed light» (IPL) zielen auf Hämoglobin, um diese Gefässe zu koagulieren. Zu hohe Energien erhöhen jedoch das Entzündungs- und PIH-Risiko. IPL ist wegen seiner unspezifischen Absorption v.a. für hellere Hauttypen geeignet.1,6,25,27
Radiofrequenz-Mikroneedling (RFMN)
RFMN wirkt nicht direkt auf Melanozyten, sondern stabilisiert die dermale Matrix. Durch Stärkung der Basalmembran, Reduktion seneszenter Fibroblasten und Koagulation pathologischer Mikrogefässe werden pigmentfördernde Reize reduziert. Der gepulste Modus (PW, ≈42–45°C) minimiert Entzündungen und PIH-Risiken, während die Energie gezielt in die Dermis abgegeben wird. Besonders bei dunklen Hauttypen sind tiefere Nadeltiefen entscheidend, um die Epidermis zu schonen. RFMN dient zunehmend der Rezidivprophylaxe nach konventioneller Therapie.28,29
Zukünftige Entwicklungen
Melasma bleibt aufgrund seiner Rezidivneigung herausfordernd. Zukünftige Strategien fokussieren auf dermale Trigger wie Fibroblastenseneszenz, vaskuläre Dysregulation und chronische Entzündung. RFMN hat sich hierbei als vielversprechender Ansatz erwiesen: Studien zeigen, dass fortgesetzte Behandlungen nach TXA-+-Kligman-Therapie Rezidive signifikant verzögern können. Weitere experimentelle Optionen wie intradermales BoNT-A oder «off-label « eingesetzte Medikamente (z.B. Rifampicin) könnten zukünftig ergänzend wirken.1
Fazit
Melasmabehandlung erfordert Geduld, Präzision und ein tiefes Verständnis der Hautbiologie. Kein einzelnes Verfahren führt zur Heilung – erst die Kombination topischer, systemischer und apparativer Methoden erzielt nachhaltige Resultate. Besonders bei dunklen und asiatischen Hauttypen ist höchste Vorsicht geboten, da selbst geringe Energieüberschüsse PIH auslösen können. Die Pathophysiologie ist noch nicht vollständig geklärt. Dies untermauert die Komplexität und wissenschaftliche Relevanz dieses Krankheitsbildes.
Literatur:
1 Jo JY et al.: Update on melasma treatments. Ann Dermatol 2024; 36(3): 125-34 2 Gan C, Rodrigues M: An update on new and existing treatments for the management of melasma. Am J Clin Dermatol 2024; 25(5): 717-33 3 Sarkar R et al.: Delphi consensus on melasma management by international experts and Pigmentary Disorders Society. J Eur Acad Dermatol Venereol 2025. Online ahead of print, https://onlinelibrary.wiley.com/doi/10.1111/jdv.70066 (zuletzt aufgreufen am 28.10.2025) 4 Mahajan VK et al.: Medical therapies for melasma. J Cosmet Dermatol 2022; 21(9): 3707-28 5 Galache TR et al.: Photobiomodulation for melasma treatment: integrative review and state of the art. Photodermatol Photoimmunol Photomed 2024; 40(1): e12935 6 Ali L, Al Niaimi F: Pathogenesis of melasma explained. Int J Dermatol 2025; 64(7): 1201-2 7 Zhang AD et al.: A scoping review on melasma treatments and their histopathologic correlates. Dermatopathology 2025;1 2(2): 13 8 Neagu N et al.: Melasma treatment: a systematic review. J Dermatolog Treat 2022; 33(4): 1816-37 9 McKesey J et al.: Melasma treatment: an evidence-based review. Am J Clin Dermatol 2020; 21(2): 173-225 10 Lima PB et al.: Efficacy and safety of topical isobutylamido thiazolyl resorcinol (Thiamidol) vs. 4% hydroquinone cream for facial melasma: an evaluator-blinded, randomized controlled trial. J Eur Acad Dermatol Venereol 2021; 35(9): 1881-7 11 Na JI et al.: Effect of tranexamic acid on melasma: a clinical trial with histological evaluation. J Eur Acad Dermatol Venereol 2013; 27(8): 1035-9 12 Del Rosario E et al.: Randomized, placebo-controlled, double-blind study of oral tranexamic acid in the treatment of moderate-to-severe melasma. J Am Acad Dermatol 2018; 78(2): 363-9 13 Zhu CY et al.: Analysis of the effect of different doses of oral tranexamic acid on melasma: a multicentre prospective study. Eur J Dermatol 2019; 29(1): 55-8 14 Kim HJ et al.: Efficacy and safety of tranexamic acid in melasma: a meta-analysis and systematic review. Acta Derm Venereol 2017; 97(7): 776-81 15 Sarkar R et al.: Prescribing practices of tranexamic acid for melasma: Delphi consensus from the Pigmentary Disorders Society. Indian J Dermatol Venereol Leprol 2023; 90(1): 41-5 16 Dayal S et al.: Combination of glycolic acid peel and topical 20% azelaic acid cream in melasma patients: efficacy and improvement in quality of life. J Cosmet Dermatol 2017; 16(1): 35-42 17 Sarkar R et al.: The combination of glycolic acid peels with a topical regimen in the treatment of melasma in dark-skinned patients: a comparative study. Dermatol Surg 2002; 28(9): 828-32 18 Hurley ME et al.: Efficacy of glycolic acid peels in the treatment of melasma. Arch Dermatol 2002; 138(12): 1578-82 19 Sharquie KE et al.: Lactic acid as a new therapeutic peeling agent in melasma. Dermatol Surg 2005; 31(2): 149-5420 Sarkar R et al.: Comparative evaluation of efficacy and tolerability of glycolic acid, salicylic mandelic acid, and phytic acid combination peels in melasma. Dermatol Surg 2016; 42(3): 384-91 21 Puri N. Comparative study of 15% TCA peel versus 35% glycolic acid peel for the treatment of melasma. Indian Dermatol Online J 2012; 3(2): 109-13 22 Atwa MA et al.: Combined chemical peels versus trichloroacetic acid (TCA) for treating melasma: a split-face study. J Dermatolog Treat 2022; 33(2): 959-64 23 Magalhães GM et al.: Double-blind randomized study of 5% and 10% retinoic acid peels in the treatment of melasma: clinical evaluation and impact on quality of life. Surg Cosmet Dermatol 2011; 3(1): 17-22 24 Draelos ZD: Cosmetic dermatology products and procedures. 3rd ed. Hoboken (NJ): Wiley-Blackwell, 2022. 25 Desai SR et al.: Best practices in the treatment of melasma with a focus on patients with skin of color. J Am Acad Dermatol 2024; 90(2): 269-79 26 Sarkar R et al.: Thiamidol in melasma in patients of skin of color: a preliminary report of efficacy and safety. Indian Dermatol Online J 2025; 16(5): 760-4 27 Kumar RD et al.: Melasma management: unveiling recent breakthroughs through literature analysis. Health Sci Rev 2025; 14: 100213 28 Kim JE et al.: Targeting the dermis for melasma maintenance treatment. Sci Rep 2024; 14(1): 949 29 Kwon HH et al.: Combined treatment of melasma involving low-fluence Q-switched Nd:YAG laser and fractional microneedling radiofrequency. J Dermatolog Treat 2019; 30(4): 352-6
Das könnte Sie auch interessieren:
Pre-pectoral breast reconstruction: PU versus ADM
In immediate pre-pectoral direct-to-implant breast reconstruction, the “interface” choice matters. In this cohort, polyurethane(PU)-coated implants used without acellular dermal matrices ...
Lebensqualität durch minimalinvasive funktionelle Gaumenrekonstruktion
Die funktionelle Rekonstruktion im Kopf-Hals-Bereich zählt zu den anspruchsvollsten Aufgaben moderner Chirurgie, da sie zentrale Lebensfunktionen unmittelbar betrifft. Wenn der weiche ...
Einblicke in die Geschichte des Botulinumtoxins
Die Geschichte der Entstehung des Botulinumtoxins ist bemerkenswert: Vom gefürchteten Lebensmittelgift entwickelte es sich zu einem etablierten, weltweit eingesetzten Arzneimittel mit ...