Zervikale vaskuläre Pathologien: Diagnostik und Management
Autor:innen:
Dipl.-Ing. Mag. Dr. Martina Wöß
Prim. Dr. Anton Kathrein
Krankenhaus Zams
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Vaskuläre Pathologien der Halswirbelsäule, insbesondere Dissektionen der A. carotis oder der A. vertebralis, sind potenziell lebensbedrohliche Zustände. Sie treten häufig infolge von stumpfen oder penetrierenden Traumata auf und sind klinisch oft schwer zu erkennen. Die frühzeitige multimodale Diagnostik und das adäquate interdisziplinäre Management sind von essenzieller Bedeutung für eine erfolgreiche Behandlung.
Keypoints
-
Zervikale Gefäßdissektionen entstehen häufig im Rahmen eines HWS-Traumas, kommen jedoch auch spontan vor.
-
Klinische Symptome sind meist unspezifisch und treten vielfach verzögert auf.
-
Die Therapie reicht von Antikoagulation bis zu interventionellen und chirurgischen Verfahren.
-
Die frühzeitige Diagnose ermöglicht in bis zu 90% der Fälle eine vollständige Remission.
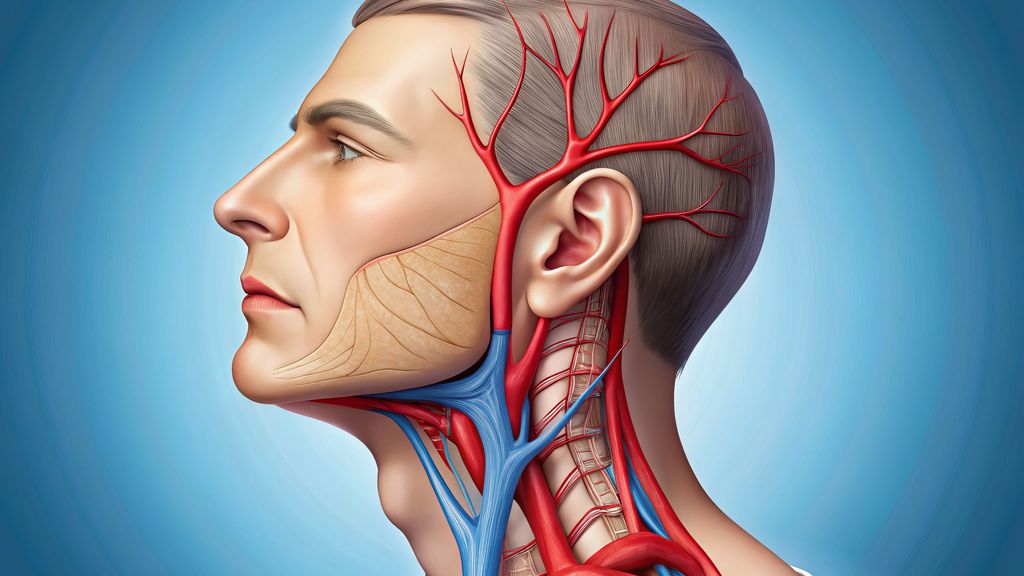
Anatomie, Pathogenese und klinische Relevanz
Anatomie
In der vorderen Halsregion liegt die A. carotis communis, diedem Aortenbogen (links) bzw. dem Truncus brachiocephalicus (rechts) entspringt. Sie teilt sich typischerweise auf Höhe des dritten bis vierten Halswirbels in die zwei wichtigsten Endäste für die Versorgung von Kopf und Hals. Bei dieser Gabelung befindet sich der Bulbus caroticus als Teil des sinuaortalen Systems. Etwas 2–3cm distal des Bulbus befindet sich die typische extrakranielle Lokalisation für Dissektionen. Die A. vertebralis entspringt in 90% der Fälle der Hinterwand der A. subclavia. Der Gefäßverlauf wird vom Ursprung der Arterie bis zur hinteren Schädelgrube unter anatomischen und klinischen Gesichtspunkten in vier Abschnitte unterteilt:
-
V1 Pars prevertebralis: Vom Abgang zieht die A. vertebralis auf dem M. longus colli im Trigonum scalenovertebrale nach kranial.
-
V2 Pars transversaria: Die A. vertebralis zieht auf der rechten Seite in etwa 95% der Fälle und auf der linken Seite in etwa 92% der Fälle zum Foramen transversarium des 6. Halswirbels. Mit dem Eintritt in das Foramen beginnt der zweite und wichtigste Verlaufsabschnitt. Die A. vertebralis ist die einzige Arterie des Körpers, welche in einem so langen osteofibrösen Kanal, auch „Querfortsatzkanal“ genannt, verläuft.
-
V3 Pars atlantica: Nach dem Austritt der A. vertebralis aus dem Foramen transversarium des Axis zieht diese von hier in bogenförmigem Verlauf zum Sulcus arteriae vertebralis des hinteren Atlasbogens (C1 Atlasschlinge). Bei jeglicher translatorischer oder rotatorischer Gewalteinwirkung auf die Halswirbelsäule – wie sie insbesondere bei B- und C-Verletzungen vorkommt – ist die Arteria vertebralis in den zuvor beschriebenen Abschnitten (V2 und V3) besonders verletzungsgefährdet. Dies liegt vor allem an ihrer exponierten Lage am hinteren Atlasbogen sowie an dem langen knöchernen Kanal, den sie in diesem Bereich durchläuft.
-
V4 Pars subarachnoidalis: Zwischen hinterem Atlasbogen und der Squama occipitalis durchbricht die A. vertebralis die Membrana atlantooccipitalis posterior, die Dura mater spinalis sowie die Arachnoidea mater und gelangt in den Subarachnoidalraum.1
Die A. vertebralis zeigt häufig Varianten in Ursprung und Verlauf. Insbesondere Schlängelungen (Tortuosity), Schlingenbildungen (Coiling), Knickbildungen (Kinking) oder asymmetrische Anlagen können die Anfälligkeit für Dissektionen erhöhen. Derartige Variationen müssen bei der radiologischen Diagnostik unbedingt beachtet werden, da diese zu Fehldiagnosen führen können. Auch präoperativ sollten Gefäßschleifen bekannt sein, um iatrogene Verletzungen zu vermeiden.2
Pathogenese
Bei einer Dissektion kommt es pathomorphologisch zu einem Einriss der Vasa vasorum mit daraus resultierendem intramuralem Wandhämatom. Dieses kann sich wie eine Wühlblutung nach kranial und kaudal ausbreiten. Dabei kann es sowohl initial als auch erst sekundär zu einer Ruptur der Intima mit Ausbildung einer Intimalefze und zweitem Lumen kommen. Sobald die Intima verletzt ist, wird das Gerinnungssystem aktiviert, Thromben lagern sich an und ein embolisches Geschehen in den hinteren Kreislauf mit zerebraler Ischämie oder hämorrhagischer Komplikation kann folgen. Bleibt es bei dem Wandhämatom ohne Intimaläsion, wirkt dieses raumfordernd nach innen mit Gefäßstenose und daraus resultierendenrFlussunregelmäßigkeit. Nach außen kann es zu einer aneurysmatischen Dilatation mit möglicher Bedrängung neuronaler Strukturen führen. Die Auslöser lassen sich in drei Hauptkategorien einteilen:
Spontane Dissektion:
-
Genetische Prädisposition bei Bindegewebserkrankungen (z.B. Ehlers-Danlos-, Marfan-Syndrom)
-
Degenerative Gefäßveränderungen durch Ablagerungen bei Hypercholesterinämie oder entzündliche Reaktionen
-
Arterielle Hypertonie, Nikotinabusus, Migräne (hohe intravasale Drücke)3
Traumatische Dissektion:
-
Verkehrsunfälle
-
Sport- oder Freizeitunfälle (z.B. Klettern, Snowboard, Fahrrad)
-
Stich- oder Schussverletzungen
Iatrogene Dissektion:
-
Chiropraktische Manipulationen (ca. 1/20000 pro Jahr)
-
Intraoperative Gefäßverletzungen (Pedikelschrauben, Unkoforaminotomie, …)
-
Interventionelle Maßnahmen (z.B. Katheter, Injektionen)4,5
Der Häufigkeitsgipfel der spontanen Dissektionen liegt bei 40–45 Jahren und ist in bis zu 25% Ursache der juvenilen Schlaganfälle. Die traumatisch bedingten Gefäßdissektionen entstehen durch direkte oder indirekte Gewalteinwirkung auf die Zervikalregion. Grundsätzlich unterscheidet man zwischen:
-
BCVI: Blunt Cerebrovascular Injury (stumpfes Trauma)
-
PCVI: Penetrating Cerebrovascular Injury (penetrierendes Trauma)
Die Mechanismen sind meist ein schnelles Dezelerationstrauma mit Hyperextension und Rotation. Dabei ist die A. vertebralis im engen Querfortsatzkanal stark gefährdet, insbesondere bei daraus resultierenden disko- und osteoligamentären Verletzungen sowie Gelenksverrenkungen. Ein massiver Distraktionsmechanismus kann zum Abriss der A. vertebralis führen. Stich- oder Schussverletzungen als direktes Trauma können sowohl in der vorderen, als auch der hinteren Zervikalregion zu Gefäßverletzungen führen.6
Klinische Bedeutung
Die klinische Präsentation zervikaler Dissektionen ist variabel, mild oder asymptomatisch und häufig verzögert. Strukturelle Zusatzverletzungen mit entsprechender Symptomatik sind vordergründig. Die klassische Trias aus plötzlichen Kopf- und/oder Nackenschmerzen unilateral und ipsilateral zur Seite der Dissektion, ipsilateralem Horner-Syndrom und Zeichen einer zerebralen Ischämie tritt bei den meisten Patienten nicht gleichzeitig auf. Leitbefunde sind ipsilaterale frontotemporale Cephalea bei Karotis-Dissektion und okzipitale Kopf- sowie Nackenschmerzen bei Vertebralis-Dissektion. Das gleichseitige Horner-Syndrom ist entweder postganglionär verursacht bei der Karotis-Dissektion oder zentral durch die Hirnstammischämie bei der Vertebralisverletzung. Zerebrale Ischämien treten bei mehr als 80% der Patienten auf und können sowohl hämodynamischer als auch embolischer Genese sein. Ist die A. carotis betroffen, treten die typischen Symptome eines Insults auf. Am häufigsten ist die dorsolaterale Medulla oblongata durch eine Läsion der A. vertebralis betroffen, sodass es zur klinischen Ausprägung eines kompletten oder inkompletten Wallenberg-Syndroms kommt. Dies bezeichnet einen Symptomenkomplex aus Schwindel, Ataxie, Hirnnervenausfällen und kontralateralen dissoziierten Sensibilitätsstörungen.
Diagnostik und Management
Die Diagnostik sollte multimodal und strukturiert erfolgen. Bei entsprechendem Trauma empfiehlt es sich, initial das Spiral-CT mit Angiografie (CTA) durchzuführen. Insbesondere bei Polytraumapatienten finden sich selbst bei unauffälligem neurologischem Status in 20–40% der Fälle vaskuläre Läsionen. Ein MRT mit MR-Angiografie (MRA) ist zur Zusatzdiagnostik ebenso empfohlen, hier können Intimalappen und luminale Thromben sehr gut verifiziert werden. Die Duplexsonografie ist zur Verlaufskontrolle und Zusatzdiagnostik empfehlenswert. Für interventionelle Eingriffe ist die digitale Subtraktionsangiografie (DSA) reserviert.7
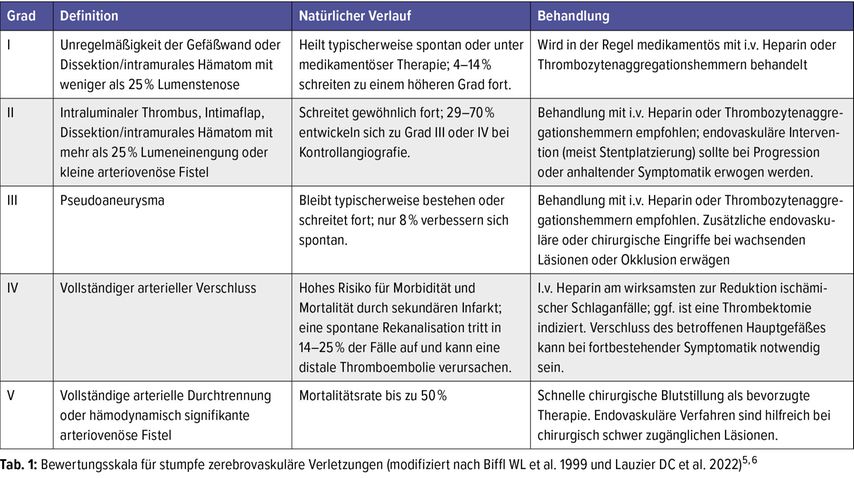
Zur Klassifikation von stumpfen zerebrovaskulären Verletzungen der HWS (Blunt Cerebrovascular Injury; BCVI) hat sich die Graduierungsskala nach Biffl et al.8 durchgesetzt. Hier wurden die Gefäßläsionen anhand der CTA oder DSA klassifiziert und das therapeutische Vorgehen von einer Arbeitsgruppe nach Lauzier DC et al.9 2022 abgeleitet (Tab.1).10
Tab. 1: Bewertungsskala für stumpfe zerebrovaskuläre Verletzungen (modifiziert nach Biffl WL et al. 1999 und Lauzier DC et al. 2022)5,6
Therapiemanagement
Gefäßläsionen Grad I–IV werden allseits medikamentös im Sinn einer Heparinisierung bzw. oralen Antikoagulation (AK)behandelt. Bei Grad II–IV kommen zusätzlich interventionell endovaskuläre Verfahren wie Stenting, Coil-Embolisierung oder Thrombektomie zur Anwendung. Bei einer Gefäßruptur ist die chirurgische Rekonstruktion angezeigt.
Die Therapieentscheidung erfolgt patientenindividuell und richtet sich neben der Graduierung an der Klinik und den möglichen Begleitverletzungen oder Vorerkrankungen. Therapieziele sind die Vermeidung sekundärer ischämischer Ereignisse, die Reperfusion des betroffenen Gefäßes und die Prävention neurologischer Defizite durch Schaffen stabiler Verhältnisse (Abb.1).
Abb. 1: Therapieziele sind die Vermeidung sekundärer ischämischer Ereignisse, die Reperfusion des betroffenen Gefäßes und die Prävention neurologischer Defizite durch Schaffen stabiler Verhältnisse
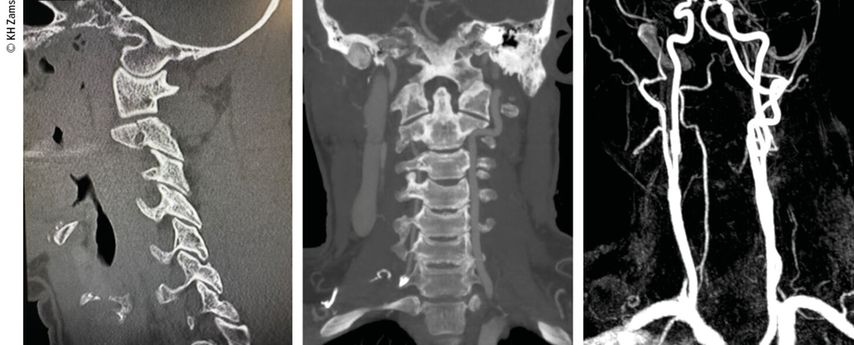
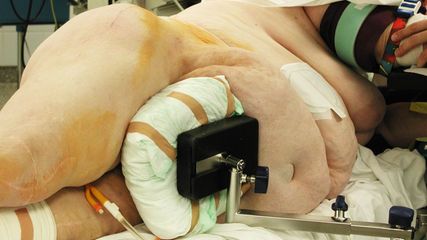
Der interdisziplinäre Ansatz ist entscheidend. Liegt beispielsweise eine instabile HWS-Verletzung mit Vertebralis-Dissektion vor, so ist die Wiederherstellung stabiler Verhältnisse für u.a. die A. vertebralis vordergründig (Abb.2–4). Dieser operative Eingriff erfolgt bereits unter therapeutischer Heparinisierung. Je nach Ausmaß der Gefäßverletzung wird dabei ein- oder zweizeitig die endovaskuläre/offene Therapie zur Gefäßreperfusion durchgeführt. Aktuelle interdisziplinäre Therapieempfehlungen:
Abb. 2: Fallbeispiel: Mann, 57a, Z.n. Fahrradsturz, stabile Fraktur des Proc. artic. C2 r. mit Dissektion der A. vertebralis r. mit asymptomatischem Substanzdefekt im hinteren Stromgebiet (cMRT), Heparintherapie initial, anschließend APT
Abb. 3: Mann, 30a, Z.n. Snowboardsturz, Rotations-/Subluxationsverletzung C5/6 mit Dissektion der A. vertebralis r.; Zervikobrachialgie mit sensiblem Defizit; OP unter Heparintherapie, APT für 3 Monate
Abb. 4: Mann, 28a, Z.n. Schisturz; instabile Teardrop-Verletzung mit Dissektion A. vertebralis l.; Zervikobrachialgie mit Dysästhesie C6, mehrere kleine embolische Infarkte vertebrobasilär mit Koordinationsstörung; OP + Heparintherapie initial, anschließend APT
Stabile HWS-Verletzung + Vertebralis-Dissektion:
-
Heparinisierung mit Perfusor, Ziel PTT 50–60 sek
-
Orale AK mit Sintrom, Ziel INR 2–3 für 3 Monate
Instabile HWS-Verletzung + Vertebralis-Dissektion:
-
Operative Stabilisierung unter therapeutischer Heparinisierung
-
Tamponade, Naht, Ligatur, Embolisation, Stenting
-
Orale AK mit Sintrom, Ziel INR 2–3 für 3 Monate, oder orale antithrombotische Therapie (APT; Thrombo ASS) für 3 Monate + Reassessment
Die Heparinisierung mit Perfusor erfolgt in der Regel für einige Tage und wird dann je nach klinischen Befunden auf eine orale antikoagulative Therapie (OAK) oder antithrombotische Therapie (APT) umgestellt. In der Literatur findet sich die Empfehlung zur radiologischen Verlaufskontrolle vor Umstellung auf die OAK. Dies sollte patientenindividuell, abhängig vom Risikoprofil und interdisziplinär entschieden werden.
Meist erfolgt die Rekanalisation innerhalb der ersten Woche, zumindest aber in den ersten drei Monaten. Danach empfiehlt sich die klinische und radiologische Reevaluierung. Bei noch nachweisbaren Wandunregelmäßigkeiten oder klinisch/neurologischen Symptomen wird die OAK-Therapie für weitere 3 Monate fortgesetzt. Bei nachweisbarer Persistenz der Gefäßveränderung ohne Dynamik wird die Umstellung auf eine AP-Dauertherapie als ausreichend erachtet.
Nach erfolgter zerebraler Gefäßdissektion sollten ruckartige Kopfbewegungen vermieden werden. Sportliche Betätigungen sollten erst nach 6–12 Monaten wieder aufgenommen, Ausdauersport frühestens nach 3 Monaten wieder begonnen werden.
Fazit
Die zervikale Gefäßdissektion stellt eine differenzialdiagnostisch und therapeutisch anspruchsvolle Entität dar. Besonders bei jungen Patienten mit Cephalea, neurologischer Symptomatik oder nach Trauma sollte frühzeitig an eine Dissektion gedacht werden. Eine gezielte Diagnostik mit multimodaler Bildgebung und eine abgestufte, interdisziplinäre Therapieplanung ermöglichen eine günstige Prognose. In bis zu 90% der Fälle ist bei frühzeitiger Behandlung eine vollständige Remission möglich.
Literatur:
1 Mohr JP, Grotta JC: Stroke, pathophysiology, diagnosis, and management. Elsevier Health Sciences. (2004) ISBN:0443066000 2 Schubert R et al.: Vascular anomalies and malformations. Radiopaedia.org 2025; doi: 10.53347/rID-17476 3 Schievink WI: Spontaneous dissection of the carotid and vertebral arteries. N Engl J Med 2001; 344(12): 898-906 4 Ernst E: Deaths after chiropractic: a review of published cases. Int J Clin Pract. 2010; 64(8): 1162-5 5 Smith W et al.: Spinal manipulative therapy is an independent risk factor for vertebral artery dissection. Neurology. 2003; 60(9): 1424-8 6 Kathrein A, Wöß M: Vaskuläre Pathologie HWS, Vortrag KH Zams, 2025 7 Rodallec M et al.: Craniocervical arterial dissection: spectrum of imaging findings and differential diagnosis. Radiographics 2008; 28(6): 1711-288 Biffl WL et al.: Blunt carotid arterial injuries: implications of a new grading scale. J Trauma 1999; 47(5): 845-53 9 Lauzier DC et al.: Neurointerventional management of cerebrovascular trauma. J NeuroIntervent Surg 2022; 14(7): 718-22 10 Park K et al.: Vertebral artery dissection: natural history, clinical features and therapeutic considerations. J Korean Neurosurg Soc 2008; 44(3): 109-15
Das könnte Sie auch interessieren:
Mehr kardiovaskuläre Ereignisse und Malignome?
Mit Tofacitinib, einem Strukturanalogon von ATP, wurde 2013 erstmals ein Januskinase-Inhibitor (JAKi) in der Schweiz zugelassen. Die Vertreter dieser Medikamentenklasse haben sich gut ...
Seltene Kleingefässvaskulitiden im Fokus
Bei Vaskulitiden der kleinen Gefässe liegt eine nekrotisierende Entzündung der Gefässwand von kleinen intraparenchymatösen Arterien, Arteriolen, Kapillaren und Venolen vor. Was gilt es ...
Elektive Hüft-TEP bei Adipositas Grad III
Übergewichtige Patient:innen leiden früher als normalgewichtige Personen an einer Hüft- oder Kniearthrose. Allerdings sieht die aktuelle S3-Leitlinie zur Behandlung der Coxarthrose in ...