Epiphysiolysis capitis femoris: Notfallversorgung
Autoren:
Prof. Dr. Catharina Chiari
MSc Dr.Madeleine Willegger, FEBOT
Doz. Dr. Alexander Kolb
Prof. Dr. Reinhard Windhager
Universitätsklinik für Orthopädie und Unfallchirurgie, Medizinische Universität Wien
Korrespondierende Autorin:
Prof. Dr. Catharina Chiari
Die Epiphysiolysis capitis femoris (ECF) oder „slipped capital femoral epiphysis“ (SCFE) wird häufig als „orthopädischer Notfall“ bezeichnet. Eine differenzierte Herangehensweise ist jedoch entscheidend, um die seltenen Fälle, die tatsächlich einer notfallmäßigen Akutversorgung bedürfen, von jenen, die einer zeitnah geplanten Operation zugeführt werden sollten, zu unterscheiden.
Die ECF ist durch das Abrutschen der proximalen Femurepiphyse vom Schenkelhals gekennzeichnet. Dabei reißt der perichondrale Ring, der beim Jugendlichen dünner ist als bei Kindern. Es entsteht eine typische Deformität, bei der die Epiphyse im Acetabulum verbleibt und der Schenkelhals eine anteriore und außenrotierte Translation erfährt. Das Ausmaß der posterioren Dislokation der Epiphyse ist variabel.
Der typische ECF-Patient ist männlich, adipös und zwischen 10 und 14 Jahre alt. Die klinische Präsentation variiert stark. Jene Patienten, die üblicherweise als Akutpatienten eingeliefert werden, sind plötzlich gehunfähig, haben starke Schmerzen und können die betroffene Extremität nicht belasten.
Für diese Patientengruppe hat Loder 1993 die Klassifikation der instabilen ECF etabliert.1 In dieser Arbeit wurde gezeigt, dass die Instabilität den entscheidenden prognostischen Faktor darstellt und instabile ECFs mit einem schlechteren Outcome einhergehen. Die instabile ECF wurde durch Gehunfähigkeit bzw. Nichtbelastbarkeit der Hüfte aufgrund von Schmerzen trotz Verwendung von Krücken unabhängig vom Zeitpunkt des Beschwerdebeginns definiert. Die Dauer der Symptome sagt nichts über die Stabilität der Epiphyse aus. Bei genauer Anamneseerhebung liegt der Beschwerdebeginn oft Wochen zurück. In sehr vielen Fällen erfolgt die Diagnosestellung stark verzögert.2 Grund ist der oft schleichende Beginn der Beschwerden. Die Schmerzen werden häufig in das Kniegelenk projiziert. Die Beweglichkeit der Hüfte ist eingeschränkt. Die Innenrotation ist aufgehoben; es entwickelt sich das typische Drehmann-Zeichen, bei dem das Bein bei Beugung des Hüftgelenks in Außenrotation und Abduktion ausweicht. Je nach Zeitverlauf sind die Patienten gehunfähig oder zeigen ein hinkendes Gangbild.
Die Klassifikation, die den Zeitfaktor beziehungsweise den Beginn der Symptome berücksichtigt, ist wie folgt:akut (Symptome <3 Wochen; ca. 10%), chronisch (schleichender Beginn, Symptome >3 Wochen; ca. 75%), akut auf chronisch (plötzliche Exazerbation der Symptome nach vorangegangenem chronischen Verlauf; ca. 15%).3
Das Ausmaß des Abrutsches wird nach Messung des Southwick-Winkels in der Lauenstein-Aufnahme in mild (<30°), moderat (30–60°) und schwer (>60°) eingeteilt.4,5
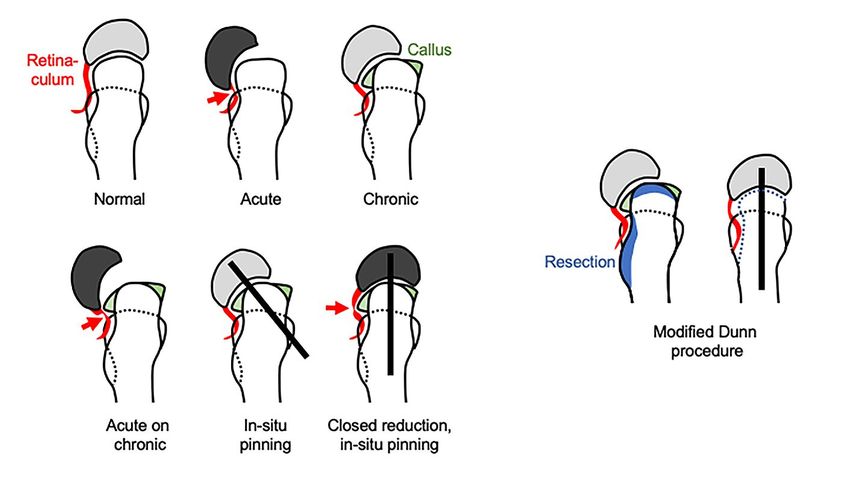
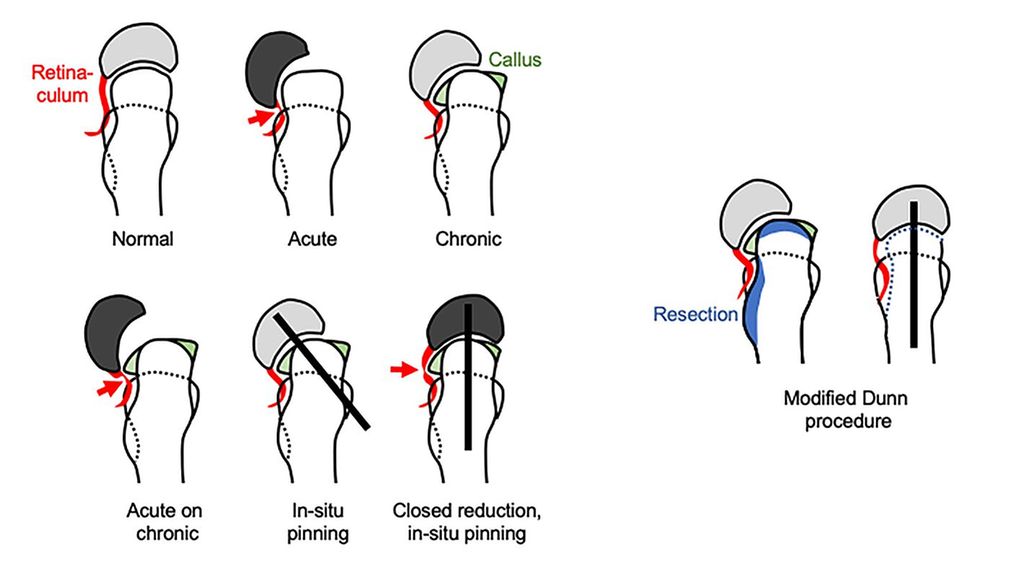
Abb. 1: Der Ramus profundus der A. circumflexa femoris medialis verläuft im posterioren Retinaculum entlang des Schenkelhalses. Er ist durch den Abrutsch selbst gefährdet abzuknicken, gefährlicher sind jedoch Repositionsmanöver. Das Gefäß wird vor allem in chronischen oder akut-auf-chronischen ECF durch Kallusapposition am Schenkelhals verdrängt und gedehnt. Somit ist die In-situ-Fixierung die sicherste Variante. Die Reposition sollte offen kontrolliert im Rahmen einer modifizierten Dunn-Osteotomie erfolgen, durch Schenkelhalsmodellierung kann die Epiphyse spannungsfrei reponiert werden (mit Genehmigung von Prof. Moritz Tannast)8
OP-Zeitpunkt und Operationsverfahren
Grundsätzlich stellt eine ECF immer eine OP-Indikation dar. Das primäre Behandlungsziel ist die Stabilisierung der Epiphyse und vor allem die Vermeidung der schwerwiegenden Komplikation der Chondrolyse und avaskulären Hüftkopfnekrose (AVN). Weiters gilt es, schwere Deformitäten zu verhindern, um Sekundärfolgen wie Impingementsituationen, Bewegungseinschränkungen und Sekundärarthrose vorzubeugen.
Vor diesem Hintergrund ist es zunächst wichtig, die Risikofaktoren für eine AVN zu definieren. Eine klare Evidenz ist bis heute nicht vorhanden, da zu diesem Thema fast ausschließlich retrospektive Studien vorliegen. Generell wurden akute und akut-auf-chronische Abrutschformen als besonders AVN-gefährdet angesehen. Seit der bereits oben erwähnten Studie von Loder ist jedoch der Faktor Stabilität in den Vordergrund gerückt. Die instabile ECF hat ein deutlich höheres Risiko für die AVN. Die Prävalenz der instabilen ECF wird mit 10–35% angegeben.6
Welche Rolle spielt nun das chirurgische Vorgehen? Hier sind Faktoren wie der Zeitpunkt der OP in Relation zum Symptombeginn, die Wahl des OP-Verfahrens sowie der Versuch einer geschlossenen Reposition zu berücksichtigen.
Die ECF wird häufig als „orthopädischer Notfall“ und als akute Indikation für eine OP innerhalb von 24 Stunden betrachtet. Mit dem heutigen Wissen um die Behandlungsergebnisse und die anatomischen Gegebenheiten, was vor allem die Gefäßversorgung der Epiphyse betrifft, ist dieses Vorgehen in den meisten Fällen nicht mehr gerechtfertigt. Der entscheidende Faktor für die Vermeidung der Hüftkopfnekrose ist der Erhalt der Blutversorgung der Epiphyse über den Ramus profundus der Ateria circumflexa femoris medialis. Dieser verläuft im posterioren Retinaculum entlang des Schenkelhalses.7 Das Gefäß läuft Gefahr, durch die Epiphysiolyse abzuknicken. Dies trifft vor allem auf die akute instabile ECF zu. Bei protrahierten Verläufen kommt es zur Kallusbildung zwischen Schenkelhals und Epiphyse, insbesondere posterior, wodurch der Gefäßverlauf zwar kompromittiert wird, sich das Gefäß aber adaptiert. In chronischen Situationen kommt es naturgemäß zu einer Verkürzung des Retinaculums. In Abbildung 1 aus einer Arbeit von Tannast et al. 2017 ist anschaulich dargestellt, dass eine geschlossene Reposition, die keine Kontrolle des Gefäßes erlaubt, ein extremes Risiko für die Durchblutung der Epiphyse darstellt.8 Theoretisch ist eine akute geschlossene Reposition daher nur bei einer instabilen akuten ECF ohne Kallusbildung Erfolg versprechend. Auch hier besteht aber das Risiko einer Gefäßverletzung durch das Repositionsmanöver selbst. Die Kallusformation ist nativradiologisch nicht sicher darstellbar. Auch die klinischen Zeichen der Instabilität korrelieren nicht mit dem Vorhandensein eines Kallus.9 Somit wäre es lediglich mittels MRT und radiärer Rekonstruktion des Schenkelhalses zur Darstellung der Kallusformation relativ sicher möglich, die wenigen Fälle, die sicher geschlossen reponiert werden können, herauszufiltern. Diese Untersuchungstechnik ist jedoch nur in wenigen Zentren in der Akutsituation verfügbar.
Somit gilt die generelle Empfehlung, keine geschlossenen Repositionsmanöver durchzuführen. Als schonungsvollere Option ist die Reposition über Traktion, bei der über einige Tage eine longitudinale innenrotierte Extensionsbehandlung erfolgt, beschrieben. Die Methode gilt zwar als sicher, ist aber wenig effektiv, da die Repositionsrate nur um die 30% liegt. Nach der Extension erfolgt die In-situ-Fixierung.10 Parsch et al. propagieren die vorsichtige offene Reposition über einen Watson-Jones-Zugang. Hier wird das Vorhandensein eines (blutigen) Gelenksergusses als wesentliches Kriterium für die Diagnose der Instabilität definiert. Der Erguss wird mittels Ultraschall festgestellt. Die Reposition erfolgt unter taktiler Kontrolle mit der Fingerspitze, während der Assistent ein vorsichtiges Repositionsmanöver durchführt. Die Stabilisierung der Reposition wird mit Bohrdrähten durchgeführt. Die Hämatomentlastung wird als zusätzlicher Faktor für die Reduktion des AVN-Risikos angesehen. Die Ergebnisse zeigen eine sehr niedrige AVN-Rate von 4,7% bei einer Repositionsrate von 95%.11 Für die erfolgreiche Anwendung dieser Methode sind jedoch entsprechende Erfahrung und ein geschultes Team notwendig.
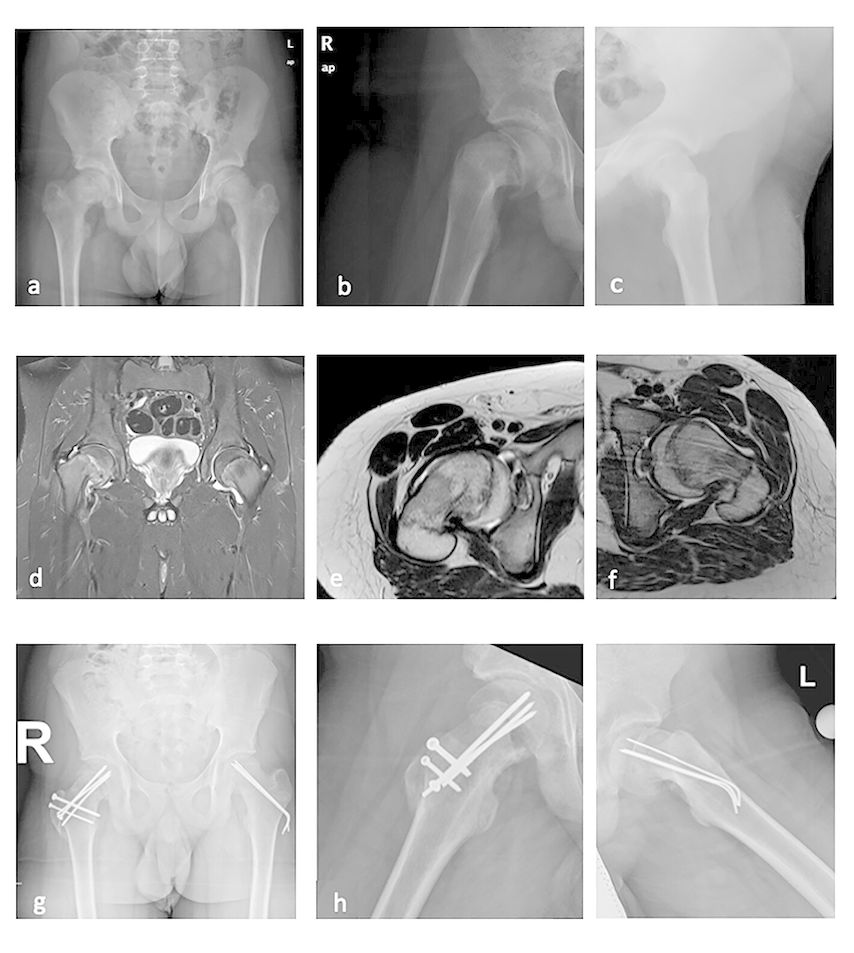
Abb. 2: Fallbeispiel: Adipöser 14-jähriger Patient mit beidseitiger ECF. Der Patient wurde akut wegen Gehunfähigkeit eingeliefert. Davor seit Wochen geringe Schmerzen, zunehmende Bewegungseinschränkung. Rechts (a, b, e) hochgradiger Abrutsch, akut auf chronisch (Kallusbildung vorhanden, die Epiphyse intraoperativ instabil). Links (a, c, f) mittelgradige ECF, chronisch, stabil. Klinisch keine Schmerzen, aber Bewegungseinschränkung. Rechts erfolgte die modifizierte Dunn-Osteotomie (g, h), links In-situ-Fixierung trotz erheblicher Restdeformität (g, i), da eine beidseitige Dunn-Osteotomie zu riskant gewesen wäre. Eine sekundäre Korrektur wird gegebenenfalls arthroskopisch erfolgen
Somit ist die In-situ-Fixierung ohne Reposition der Epiphyse der sicherste und effektivste Eingriff, um eine stabile Situation herbeizuführen. Carney et al. zeigten in einer der größten Langzeitstudien zur ECF, dass das In-situ-Pinning die niedrigste AVN-Rate aufwies, auch bei hochgradigem Abrutsch.12 Es sind verschiedenste Techniken beschrieben. Die am weitesten verbreiteten sind die Verwendung einer einzelnen Schraube, die eine definitive Epiphysiodese herbeiführt, und die Verwendung von mehreren Kirschner-Drähten, die ein Weiterwachsen ermöglichen, jedoch in einigen Fällen gewechselt werden müssen, wenn die Drähte durch das Wachstum zu kurz werden.13 Die prophylaktische Fixierung der Gegenseite wird vor allem in den USA kontrovers diskutiert, ist aber weiterhin empfohlen.14 Der offensichtliche Nachteil der In-situ-Fixierung ist die Deformität im Schenkelhals-Epiphysen-Übergangsbereich, die bestehen bleibt. Aus Beobachtungen im Rahmen von offenen Epiphysenrepositionen durch die modifizierte Dunn-Osteotomie wissen wir, dass Labrum- und Knorpelschäden nahezu immer auftreten, auch bei mittelgradigen ECFs und auch bei ECFs, die als akut oder akut auf chronisch eingestuft sind.14 Somit ist die In-situ-Fixierung als definitive Behandlungsmethode bei geringgradigen Abrutschwinkeln geeignet.
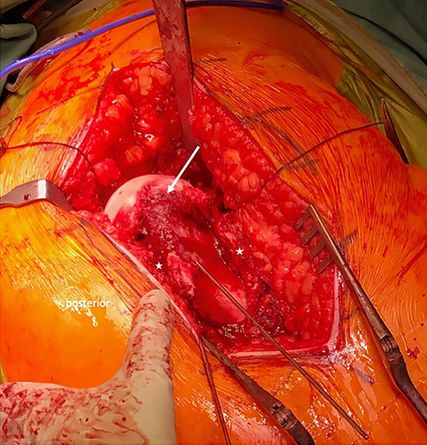
Abb. 3: Intraoperativer Situs desselben Patienten, modifizierte Dunn-Osteotomie rechte Hüfte (s. Abb. 2). Pfeil: Kallus, Sterne: zirkumferent abpräparierter Periostschlauch inkl. Retinakulum posterior
Weiters ist bekannt, dass das Remodelingpotenzial bei jüngeren Patienten (Mädchen <10 Jahre, Buben <12 Jahre) höher ist und daher in dieser Altersgruppe Fehlstellungen eher akzeptabel sind.15 Verlaufskontrollen sind jedenfalls obligat, um das Remodeling zu beobachten. Bei mittel- und hochgradigen ECF sollte jedoch eine Reposition der Epiphyse erfolgen. Hier hat sich mittlerweile die modifizierte Dunn-Osteotomie etabliert. Der Zugang erfolgt wie zur chirurgischen Hüftluxation mit Trochanter-Flip-Osteotomie und Kapsulotomie. Der wesentliche Schritt ist die Präparation eines Weichteillappens, in dem der R. profundus der A. circumflexa femoris medialis, das Periost, ein Anteil der posterioren Kapsel, der M. pririformis und die Außenrotatoren enthalten sind. Das Periost wird zirkumferent vom Schenkelhals abpräpariert, sodass die Epiphyse schließlich frei an dem Periostschlauch hängt und der Schenkelhals luxiert werden kann. Je nach Stabilität und Chronizität der ECF löst sich die Epiphyse leicht oder muss durch Kallusresektion oder Entfernung eines Knochenkeils mobilisiert werden. Die Modellierung des Schenkelhalses erfolgt durch die Entfernung des Kallus und fallweise vorsichtige Rückkürzung des Schenkelhalses, bis die Epiphyse spannungsfrei reponiert werden kann. Dabei muss darauf geachtet werden, dass genügend Schenkelhalslänge erhalten bleibt, um einen ausreichenden Offset zu erlangen und ein Abknicken des Gefäßstiels zu verhindern. Umgekehrt darf der Periostschlauch nicht zu gespannt sein, damit die Gefäße nicht abreißen. Der Vorteil dieser Technik liegt darin, dass die anatomische Reposition und sichere Kontrolle der Durchblutung möglich sind. Letztere ist durch Anbohren der Epiphyse vor und nach Reposition zu überprüfen. Der Nachteil ist, dass diese Technik entsprechende Erfahrung und Praxis erfordert und damit nur in spezialisierten Zentren mit adäquaten Fallzahlen durchgeführt werden sollte. Die Ergebnisse aus dem Zentrum des Erfinders der Technik zeigten keine AVN im 10-Jahres-Follow-up. Allerdings konnten diese Ergebnisse in anderen Zentren nicht reproduziert werden: AVN-Raten zwischen 4% und 43% wurden angegeben. Die höchsten Raten betreffen hochgradige instabile ECF.8
Die modifizierte Dunn-Osteotomie stellt somit keinen Eingriff dar, der im Notfallsetting an jeder Abteilung durchgeführt werden sollte. Allerdings ist die zeitnahe Versorgung mit entsprechender Transferierung an ein Zentrum anzustreben. Sollte dies logistisch nicht möglich sein, macht es Sinn, eine In-situ-Fixierung durchzuführen, die die sicherste Variante zur Vermeidung der AVN darstellt.
Je nach verbleibender Deformität sollte ein Sekundäreingriff geplant werden. In diesem Kontext kommt der Hüftarthroskopie immer mehr Bedeutung zu. Hüftkopfdeformitäten im Sinne eines CAM-Impingements können sekundär arthroskopisch therapiert werden. Für milde Abrutschformen sind auch die In-situ-Fixierung und gleichzeitige arthroskopische Hüftkopfmodellierung möglich.16
Hochgradige Deformitäten, die neben der funktionellen Einschränkung additiv Schäden an Knorpel und Labrum verursachen, sollten einer geplanten Korrektur zugeführt werden. Dazu zählt heute auch eine umfassende radiologische Abklärung. Neben den konventionellen Röntgenaufnahmen hat das MRT besonderen Stellenwert. Die radiäre Rekonstruktion von Schenkelhals und Hüftkopf ermöglicht die dreidimensionale Erfassung der Hüftkopf- und Schenkelhalsanatomie. Bei fraglichen Durchblutungsstörungen kann mittels Kontrastmittel-MRT eine inzipiente AVN erkannt werden, was auch forensische Bedeutung hat. Hochauflösende Knorpelsequenzen dokumentieren bereits vorhandene Knorpel- oder Labrumschäden. Die modifizierte Dunn-Osteotomie hat hier das größte Korrekturpotenzial, da die Deformität direkt an ihrem Ursprung behoben wird. Die Imhäuser-Osteotomie ist ein extraartikuläres Verfahren, bei dem die Osteotomie intertrochantär erfolgt und im Sinne einer Flexions-Valgisierungs- und Antetorsionsosteotomie durchgeführt wird. Vorteil ist das geringe Risiko für eine AVN, Nachteil ist die extraanatomische Korrektur, die eine sekundäre Deformität verursacht. Die Langzeitergebnisse sind insgesamt positiv zu bewerten.17
Zusammenfassung
Bis heute ist kein klarer Behandlungsalghorithmus für die ECF etabliert. Aus der Literatur lässt sich ableiten, dass die instabile ECF das höchste Risiko für Komplikationen aufweist. Die Zuordnung in akut und chronisch ist nicht immer eindeutig möglich, weshalb die klinische Beurteilung der Stabilität (Klassifikation nach Loder) das Hauptkriterium für die Erstbegutachtung und Entscheidung über die Dringlichkeit der Versorgung darstellt. Inwiefern der Zeitpunkt der Versorgung eine Rolle spielt, wird kontrovers diskutiert. Es gibt Fallserien, in denen eine Akutversorgung innerhalb von 24 Stunden geringere AVN-Raten zeigte. Die Versorgung im Zeitfenster zwischen 24 Stunden und 7 Tagen zeigte die höchsten AVN-Raten. Ebenso gibt es zahlreiche Studien, die dies widerlegen.18
Somit relativiert sich die absolute Notwendigkeit der Akutversorgung unter 24 Stunden. Im klinischen Alltag ist eine Akutversorgung auch nicht immer realistisch durchzuführen. Die Patienten kommen häufig verzögert ins Krankenhaus, sodass bereits dadurch das Zeitfenster überschritten ist. Wenn die Möglichkeit besteht, Patienten rasch in ein spezialisiertes Zentrum zu transferieren, sollte diese wahrgenommen werden. Eine differenzierte Abklärung mittels MRT optimiert die Auswahl des idealen und wenn möglich definitiven Operationsverfahrens; dieses ist heute in vielen Fällen die modifizierte Dunn-Osteotomie. Andernfalls ist die In-situ-Fixierung als sicherste Methode zu empfehlen. Danach sollten unbedingt regelmäßige radiologische und klinische Kontrollen stattfinden, um notwendige Sekundäreingriffe zu planen und Folgeschäden zu verhindern, sollte kein ausreichendes Remodeling eintreten. Geschlossene Repositionsmanöver haben ein sehr hohes Risiko für die AVN und sollten unterbleiben.
Literatur:
1 Loder RT et al.: Acute slipped capital femoral epiphysis: the importance of physeal stability. J Bone Joint Surg Am 1993; 75(8): 1134-40 2 Millis MB: SCFE: clinical aspects, diagnosis, and classification. J Child Orthop 2017; 11(2): 93-8 3 O’Brien ET, Fahey JJ: Remodeling of the femoral neck after in situ pinning for slipped capital femoral epiphysis. J Bone Joint Surg Am 1977; 59(1): 62-8 4 Boyer DW et al.: Slipped capital femoral epiphysis. Long-term follow-up study of one hundred and twentyone patients. J Bone Joint Surg Am 1981; 63: 85–95 5 Southwick WO: Osteotomy through the lesser trochanter for slipped capital femoral epiphysis. J Bone Joint Surg Am 1967; 49(5): 807-35 6 Zaltz I et al.: Unstable SCFE: review of treatment modalities and prevalence of osteonecrosis. Clin Orthop Relat Res 2013; 471(7): 2192-8 7 Ganz R et al.: Surgical dislocation of the adult hip a technique with full access to the femoral head and acetabulum without the risk of avascular necrosis. J Bone Joint Surg Br 2001; 83-B: 1119-24 8 Tannast M et al.: The modified Dunn procedure for slipped capital femoral epiphysis: the Bernese experience. J Child Orthop 2017; 11(2): 138-46 9 Ziebarth K et al.: Clinical stability of slipped capital femoral epiphysis does not correlate with intraoperative stability. Clin Orthop Relat Res 2012; 470: 2274-9 10 Dietz FR: Traction reduction of acute and acute-on-chronic slipped capital femoral epiphysis. Clin Orthop Relat Res 1994; (302): 101-10 11 Parsch K et al.: Open reduction and smooth Kirschner wire fixation for unstable slipped capital femoral epiphysis. J Pediatr Orthop 2009; 29(1): 1-8 12 Carney BT et al.: Long-term follow-up of slipped capital femoral epiphysis. J Bone Joint Surg Am 1991; 73: 667-74 13 Lederer C et al.: Fixationstechniken bei der Epiphyseolysis capitis femoris. Orthopäde 2019; 48(8): 659-7 14 Schultz WR et al.: Prophylactic pinning of the contralateral hip in slipped capital femoral epiphysis: evaluation of long-term outcome for the contralateral hip with use of decision analysis. J Bone Joint Surg Am 2002; 84-A(8):1305-14 15 Bellemans J et al.: Slipped capital femoral epiphysis: a long-term follow-up, with special emphasis on the capacities for remodeling. J Pediatr Orthop B 1996; 5(3): 151-7 16 Leunig M et al.: In situ pinning with arthroscopic osteoplasty for mild SCFE. Clin Orthop Relat Res 2010; 468: 3160-7 17 Parsch K et al.: Intertrochanteric corrective osteotomy for moderate and severe chronic slipped capital femoral epiphysis. J Pediatr Orthop B 1999; 8(3): 223-30 18 Ng WX et al.: The unstable slipped capital femoral epiphysis: does the rate of osteonecrosis really depend on the timing of surgery and surgical technique? J Pediatr Orthop B 2019; 28(5): 458-64
Das könnte Sie auch interessieren:
Präventive Strategie: extrakorporale Stoßwellentherapie
Die extrakorporale Stoßwellentherapie (ESWT) hat sich von einer ursprünglich lithotriptischen Methode zu einem vielseitigen biologischen Stimulationsverfahren entwickelt. ...
Gangpathologien nach hüftgelenksnahen Frakturen
Der routinemäßige Einsatz biomechanischer Motion-Capture-Systeme (MoCap) in einem Ganglabor liefert durch eine präzise Diagnostik wertvolle Informationen über Gangpathologien und stellt ...
Die PRS-Rekonstruktionspfanne mit zentraler Ileumschraube
Neben komplexen Frakturmorphologien erschweren osteoporotische Knochenqualität, vorbestehende Degeneration des Hüftgelenks sowie der Anspruch an eine rasche postoperative Mobilisation ...