Welche Substanzen in der Upstream-Therapie einsetzen?
Autorin:
OÄ Dr. Anna Rab
Fachärztin für Kardiologie, Innere Medizin und Intensivmedizin
Herzinsuffizienz-Spezialistin,
Leitende Kardiologin, LKH Villach
E-Mail: office@rab-kardio.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Mit der Upstream-Therapie versuchen wir seit mehr als 10 Jahren, additive Wege in der Therapie des Vorhofflimmerns (VHF) zu beschreiten. Diese neue Therapieform befasst sich nicht mit der Behandlung der Rhythmusstörung selbst, sondern zielt darauf ab, mithilfe bestimmter Pharmaka die kardialen Grunderkrankungenzu beeinflussen und in der Folge atriale Remodeling-Prozesse zu verlangsamen oder ihnen vorzubeugen.
Keypoints
-
Die 5 vorgestellten Substanzen konnten in unterschiedlichen Studien einen Effekt nicht nur auf das Auftreten, sondern auch auf die Häufigkeit von Vorhofflimmerepisoden zeigen.
-
Die Stärken der Omega-3-Fettsäuren und Statine liegen in der Reduktion der VHF-Relaps- Rate nach Kardioversion.
-
ACE-H, Sacubitril/Valsartan und SGLT2-I scheinen auch über lange Beobachtungszeiträume die Inzidenz von VHF in einem Hochrisikokollektiv zu reduzieren.
-
Wenn der Erhalt von Sinusrhythmus für den Patienten wichtig ist, so kann ein individualisierter Einsatz dieser Substanzen durchaus unterstützend wirken. Studien, die diesen Effekt gerade bei den SGLT2-I weiter untersuchen, sind in Vorbereitung.
Können wir mittels Upstream-Therapie die VHF-Rezidivraten reduzieren?
Eins vorweg, Substanzen der Upstream-Therapie gehören nicht zur Gruppe der Antiarrhythmika!
Strukturelle Ursachen für ein VHF-Onset sind:
-
Interstitielle Fibrose der Vorhöfe – Remodeling
-
Vorhofvergrößerung
-
Verkürzung des Aktionspotenzials durch Kalzium-Overload
-
Verstärkte Aktivierung des Angiotensin-II-Systems
-
Proinflammatorische Prozesse
-
Oxidativer Stress
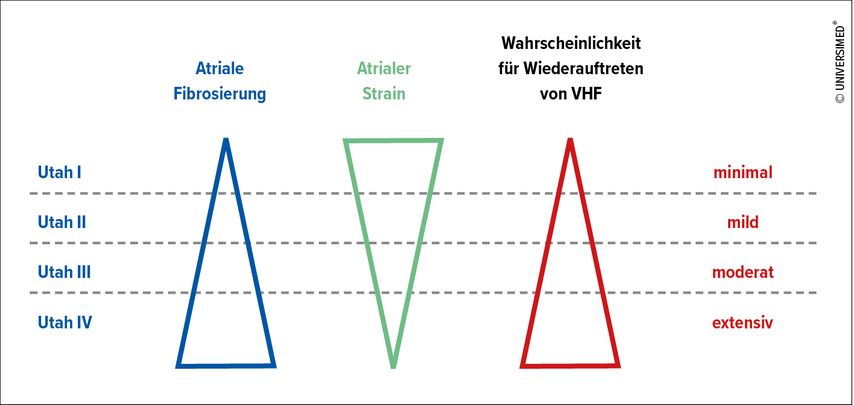
Anhand der Utah-Kriterien von 2014 ist gut zu erkennen, dass ein Zusammenhang zwischen der atrialen Fibrosierung (i.e. bindegewebige Umbauprozesse, Remodeling) und dem Auftreten von VHF besteht.1
Abb. 1: Utah-Kriterien: Eine Abnahme des atrialen Strains korreliert mit einer vermehrten Fibrosierung und VHF-Episoden (nach Longobardo L et al.)1
Omega-3-Fettsäuren reduzieren oxidativen Stress, indem sie einem Ca-Overload entgegenwirken
Bekannt ist, dass regelmäßiger Verzehr von Fisch für den Omega-3-Fettsäuren-Gehalt im Blut zuträglich ist. Weniger bekannt ist jedoch die Tatsache aus einer Beobachtungsstudie mit einem Follow-up von bis zu 12 Jahren, dass der Konsum von hochwertigem Fisch die VHF-Inzidenz um bis zu 30% reduziert.2 Ein interessanter Aspekt jener Studie von Mozaffarian et al. ist auch, dass das Ausmaß der Inzidenzreduktion direkt mit der Zubereitungsart des Fisches korreliert. Will heißen: „Gekochter und gegrillter Fisch und ein Genuss von >5x/Woche verhindern am besten das Auftreten von VHF.“ Bei gebratenem Fisch oder Fischsandwiches wurden dagegen keine positiven Auswirkungen hinsichtlich einer Reduktion von VHF festgestellt.
Des Weiteren ist der präventive Effekt von Omega-3-Fettsäuren nach Kardioversion zu erwähnen. In einer 2011 publizierten Studie von Nodari et al. konnte gezeigt werden, dass in den Studiengruppen ACE-H/ATB + Amiodaron mit Omega-3-Fettsäuren und ohne diese deutliche Unterschiede im Auftreten von VHF erkannt wurden.3 Bei der Gruppe mit Kombination von Omega-3-Fettsäuren fand sich eine 33%igeReduktion des relativen Risikos im Hinblick auf den VHF-Relaps.
Statine zeigen pleotrope Effekte zur Prävention der atrialen Fibrose
Statine verhindern durch eine Reihe von potenziellen Wirkmechanismen das Auftreten von VHF. Der positive Einfluss der Statine auf chronische Inflammation und antioxidative Effekte zählen zu ihren wirkungsvollsten Vorteilen. In einer Metaanalyse von Rahimi et al.4 aus dem Jahr 2011 konnte das oben beschriebene Potenzial der Statine allerdings nur in Studien mit kurzem Follow-up verifiziert werden. Die Reduktion des relativen Risikos beim Auftreten von VHF lag bei 39% in Bezug auf die Inzidenz und auf Relaps. In den Studien mit langem Follow-up konnte diese Beobachtung nicht bestätigt werden.
In einer aktuellen Publikation aus Österreich von Fiedler et al.5 wurde der Statineffekt nach Kardioversion untersucht. Die Autoren der Studie fanden dabei eine Reduktion des absoluten Risikos für einen VHF-Relaps von 27% unter 12-monatiger Statintherapie, wobei die Beobachtungsgruppen nach Geschlecht und Alter stratifiziert wurden („propensity-matched analysis“).
ACE-Hemmer und Angiotensin-II-Rezeptorblocker bewirken eine RAAS-Blockade
Durch die Blockade der neurohumoralen Aktivierung des Sympathikus und des RAAS-Systems durch ACE-Hemmer bzw. Angiotensin-II-Rezeptorblocker(ARB) kommt es zur positiven Beeinflussung des Remodelings der Vorhöfe. Gleiches gilt auch für die Beeinflussung der Herzkammern und die Entstehung einer Herzinsuffizienz. 2010 publizierten Schneider et al. auf Basis einer Metaanalyse,6 dass bestimmte Subgruppen durch die RAAS-Blockade signifikant im Hinblick auf Auftreten von VHF profitieren. Patienten der untersuchten Subgruppe „frühe Herzinsuffizienzstudien mit ACE-Hemmer“ und der Subgruppe „nach elektrischer Kardioversion“ profitierten signifikant mehr von der RAAS-Blockade als jene, die unter der Subgruppe „nach Myokardinfarkt“ eingeschlossen wurden. Unter den mehr als 80000 Patienten, welche bei dieser Metaanalyse im Rahmen der Primär- als auch Sekundärprävention berücksichtigt wurden, zeigte sich insgesamt eine Reduktion des relativen Risikos von 22% in Bezug auf VHF-Prävention.
Sacubitril/Valsartan verlängert die Halbwertszeit der natriuretischen Peptide
Neben der RAAS-Blockade durch den Valsartan-Anteil von Sacubitril/Valsartan bewirkt die Erhöhung von Neprilysin durch den Sacubitril-Anteil hohe ANP- und BNP-Spiegel und führt damit zur Reduktion der Druck- und Volumenbelastung von Vorhöfen und Kammern und der kardialen Fibrose. Ein weiterer positiver Aspekt ist, dass die damit verbundene verstärkte Diurese auch das „reverse remodeling“ positiv beeinflusst.7 Dazu sei bemerkt, dass in der Studie von Martens et al. Sacubitril/Valsartan neben dem oben genannten Einfluss auf das „reverse remodeling“ auch einen positiven Einfluss auf ventrikuläre Rhythmusstörungen zeigt.
SGLT2-Inhibitoren reduzieren Blutdruck, Körpergewicht, Inflammation, oxidativen Stress und eine Sympatikus-Überaktivität
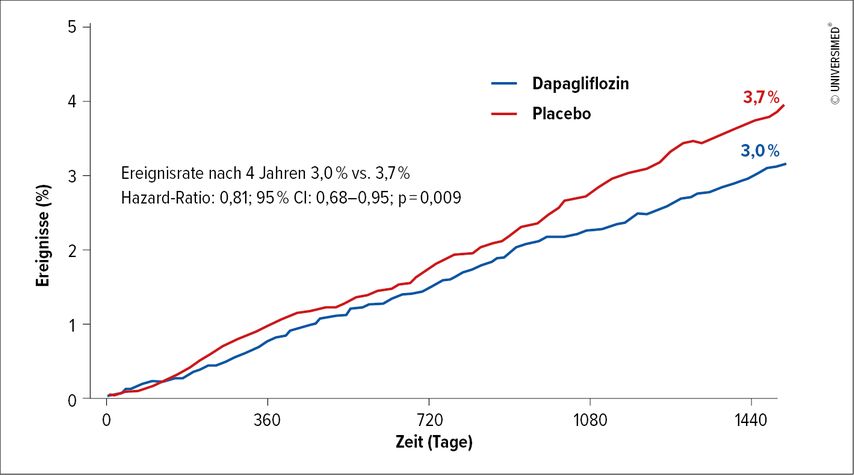
Dass SGLT2-Inhibitoren nicht nur für die Behandlung des Diabetes mellitus bekannt sind, sondern auch bei der Herzinsuffizienz Hospitalisation und kardiovaskuläre Mortalität reduzieren, ist schon hinlänglich bekannt. Neu ist jedoch nun eine weitere Facette im Wirkprofil dieser Substanzgruppe. Danach scheinen Daten aus der Post-hoc-Analyse der DECLARE-TIMI-58-Studie mit Dapagliflozin zu offenbaren, dass diese Inhibitoren eben auch Vorhofflattern und -flimmern bei Diabetespatienten reduzieren.8 Nach einem Beobachtungszeitraum von 4 Jahren waren die Arrhythmieepisoden in der Dapagliflozin-Gruppe signifikant um 19% niedriger als in der Placebogruppe (Abb. 2). Dabei war es nicht relevant, ob eine Anamnese von Vorhofflimmern oder -flattern oder einer manifesten Herzinsuffizienz bestand oder ob eine gesicherte arteriosklerotische Gefäßerkrankung vorgelegen hat.
Abb. 2: Die Ereignisrate von Vorhofflattern und -flimmern bei Diabetespatienten aus einer Post-hoc-Analyse der DECLARE-TIMI-58-Studie ist unter Dapagliflozin um 19% vs. Placebo reduziert (nach Zelniker TA et al.)8
Literatur:
1 Longobardo L et al.: Role of imaging in assessment of atrial fibrosis in patients with atrial fibrillation: state-of-the-art review. Eur Heart J Cardiovasc Imaging 2014; 15(1): 1-5 2 Mozaffarian DS et al.: Fish intake and risk of incident atrial fibrillation. Circulation 2004; 110(4): 368-73 3 Nodari S et al.: N-3 polyunsaturated fatty acids in the prevention of atrial fibrillation recurrences after electrical cardioversion: a prospective, randomized study. Circulation 2011; 124(10): 1100-6 4 Rahimi K et al.: Effect of statins on atrial fibrillation: collaborative meta-analysis of published and unpublished evidence from randomised controlled trials. BMJ 2011; 342: d1250 5 Fiedler L et al.: Upstream statin therapy and long-term recurrence of atrial fibrillation after cardioversion: apropensity-matched analysis. J Clin Med 2021; 10(4): 807 6 Schneider MP et al.: Prevention of atrial fibrillation by renin-angiotensin system inhibition a meta-analysis. J Am Coll Cardiol 2010; 55(21): 2299-307 7 Martens P et al.: Sacubitril/valsartan reduces ventricular arrhythmias in parallel with left ventricular reverse remodeling in heart failure with reduced ejection fraction. Clin Res Cardiol 2019; 108(10): 1074-82 8 Zelniker TA et al.: Effect of dapagliflozin on atrial fibrillation in patients with type 2 diabetes mellitus: insights from the DECLARE-TIMI 58 trial. Circulation 2020; 141(15): 1227-34
Das könnte Sie auch interessieren:
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
(Neue) Blutdruckziele im klinischen Alltag?
Die Diskussion um optimale Blutdruckwerte erhält durch eine aktuelle Analyse aus den USA eine neue Dynamik: Im klinischen Alltag war ein systolischer Blutdruck zwischen 130 und 139mmHg ...