Smartphones, Wearables & Co – brauchen wir noch Holter-EKGs und Loop-Rekorder?
Autoren: Dr. med. Behnam Subin
PD Dr. med. Patrick Badertscher
Universitäres Herzzentrum Basel
Universitätsspital Basel
E-Mail: patrick.badertscher@usb.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die diagnostische Landschaft der Herzrhythmusüberwachung befindet sich derzeit in einem grundlegenden Wandel. Neben klassischen Verfahren wie dem Holter-EKG, EKG-Patches und implantierbaren Loop-Rekordern treten zunehmend mobile Endgeräte wie Smartwatches in den klinischen Fokus. Diese Entwicklung wird nicht nur durch technologische Fortschritte vorangetrieben, sondern auch durch ein wachsendes Bedürfnis nach niedrigschwelliger und kontinuierlicher Diagnostik.
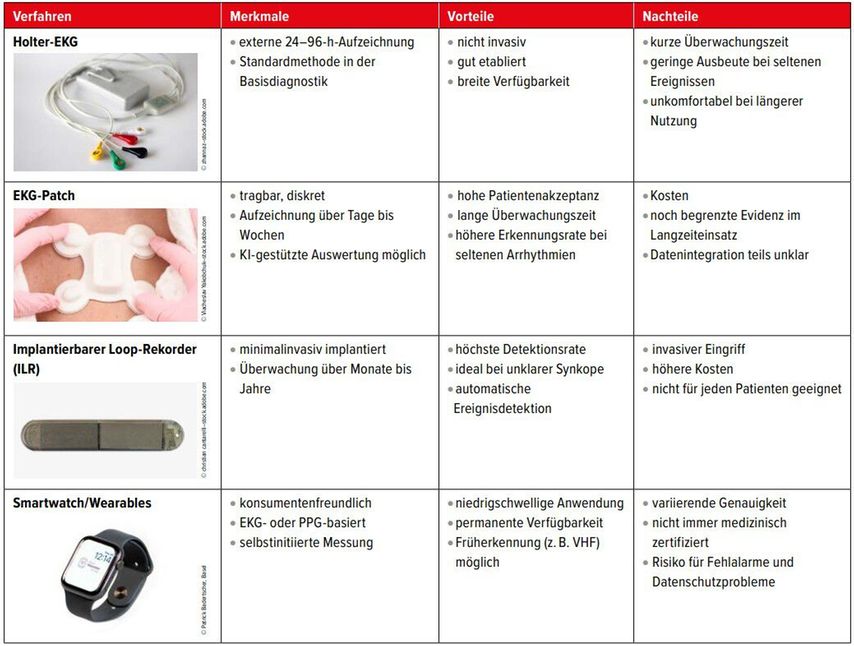
Die derzeit für die Herzrhythmusüberwachung verfügbaren diagnostischen Systeme lassen sich wie folgt differenzieren: Das Holter-EKG gilt als etabliertes Mittel zur nichtinvasiven Rhythmusdiagnostik, ist jedoch in seiner Aussagekraft begrenzt. Damit eine Arrhythmie erkannt werden kann, muss sie während des kurzen Aufzeichnungszeitraums von typischerweise 24 bis 96 Stunden auftreten. Diese zeitliche Begrenzung macht das Verfahren insbesondere bei seltenen oder asymptomatischen Episoden anfällig für falsch negative Befunde. EKG-Patches ermöglichen eine längere und für den Patienten angenehmere Überwachung, sind einfach in der Handhabung und bieten zunehmend durch künstliche Intelligenz (KI) gestützte Auswertung. Implantierbare Loop-Rekorder (ILR) wiederum stellen die invasive, aber effektivste Langzeitlösung bei unklaren Synkopen oder paroxysmalen Arrhythmien dar. ILR sind gleichzeitig jedoch das mit Abstand teuerste Rhythmusdiagnostiktool. Jede dieser Methoden besitzt spezifische Stärken und Limitationen im Hinblick auf Indikation, Anwendung und Zielgruppe.
Parallel dazu treten sogenannte Smart Devices, insbesondere Smartwatches mit integrierten Sensoren und EKG-Funktion, zunehmend in den Vordergrund. Sie versprechen eine kontinuierliche und jederzeit verfügbare Überwachung des Herzrhythmus – unabhängig von Ort, Zeitpunkt oder ärztlicher Veranlassung.
Eine Übersicht der aktuell verfügbaren Modalitäten zur Rhythmusüberwachung bietet Tabelle 1. Doch wie zuverlässig sind diese Geräte wirklich? Wo liegen ihre diagnostischen und systembedingten Grenzen? Und welche Folgen ergeben sich daraus für die klinische Praxis?
Diese Übersichtsarbeit beleuchtet die derzeitige Evidenzlage, die technischen Grundlagen sowie die klinischen Perspektiven der Rhythmusdiagnostik mittels Smartwatches. Ziel ist es, das Potenzial, die Herausforderungen und den sinnvollen Einsatz dieser Technologien im Vergleich zu etablierten Verfahren kritisch zu analysieren.
Smartwatches in der Rhythmusdiagnostik: Potenzial, Evidenz und Herausforderungen
Smartwatches mit integrierter EKG-Funktion gelten als vielversprechendes Werkzeug zur Diagnostik von Arrhythmien. Zwei Studien aus dem Universitätsspital Basel lieferten kürzlich wichtige Erkenntnisse zur diagnostischen Genauigkeit dieser Geräte. In der BASEL Wearable Study wurde eine Sensitivität zwischen 58% (Withings) und 85% (Apple, Samsung) bei automatisierter Erkennung von Vorhofflimmern (VHF) im Vergleich zum 12-Kanal-EKG ermittelt.1 In rund einem Fünftel der Fälle blieben die Ableitungen jedoch algorithmisch nicht auswertbar. Eine manuelle kardiologische Nachbefundung dieser Messungen war in 99% der Fälle möglich und erreichte eine Sensitivität von bis zu 98%. Eine Folgestudie über den Zeitraum von 2021 bis 2023 zeigte, dass sich die Zahl der nicht interpretierbaren Ableitungen tendenziell verringerte, ein Hinweis auf fortlaufende algorithmische Optimierung.2
Ein Ansatz zur Integration dieser Technologien in die klinische Versorgung stellt die Basel Wearable Clinic dar, eine digitale Plattform, über die Patientinnen und Patienten ihre EKG-Daten aus Smartwatches direkt zur ärztlichen Befundung einreichen können ( www.wearableclinic.ch , Abb.1).
Abb. 1: Logo der Basel Wearable Clinic und des Universitätsspitals Basel mit Beispielaufruf zur digitalen EKG-Übermittlung
Dieses Modell zeigt exemplarisch, wie sich digitale Selbstvermessung mit ärztlicher Expertise sinnvoll verbinden lässt.
Trotz dieser Entwicklungen bleiben wesentliche Herausforderungen bestehen: Nicht alle Smartwatches verfügen über eine medizinische Zulassung und ihre Klassifikation als Lifestyle-Produkt schränkt regulatorische Anforderungen sowie die Erstattungsfähigkeit ein. Der Fokus auf selbstinitiierte Diagnostik kann insbesondere bei gesundheitsbewussten, aber nicht vorerkrankten Nutzern zu erhöhter Sorge und Verunsicherung führen, insbesondere bei falsch positiven Befunden. Zugleich wirft der Umgang mit personenbezogenen Gesundheitsdaten neue datenschutzrechtliche Fragestellungen auf. Auch die Flut an ungefragten oder ausserhalb regulärer Zeiten erhobenen EKG-Aufzeichnungen konfrontiert Ärztinnen und Ärzte mit logistischen und rechtlichen Unklarheiten: Wer trägt die Verantwortung? Welche Dokumentationspflicht besteht? Und in welchem Rahmen darf oder soll eine medizinische Bewertung erfolgen?
Die Integration von Smartwatches in die klinische Rhythmusdiagnostik erfordert nicht nur technische Weiterentwicklung, sondern auch ein klar strukturiertes Versorgungskonzept mit definierten Zuständigkeiten, Interventionsgrenzen und Entscheidungsalgorithmen.
Rhythmusmonitoring mittels PPG über Smartphones
Rhythmusmonitoring ist auch über ein Smartphone möglich. In diesem Fall macht man sich die Kamera und den LED-Blitz zunutze, um über den Finger auf der Linse pulsabhängige Lichtreflexionen zu erfassen und daraus die Herzfrequenz sowie Rhythmusunregelmässigkeiten abzuleiten (Photoplethysmografie, PPG). Diese Methode erlaubt ein einfaches, ortsunabhängiges Selbstscreening. Studien zeigen, dass PPG-basierte Systeme Hinweise auf Vorhofflimmern erkennen können, wenngleich die Datenqualität stark von Nutzungsverhalten und Umgebungsbedingungen abhängt. Da jedoch kein elektrisches Signal erfasst wird und Artefaktanfälligkeit besteht, bleibt die Methode ein unterstützendes Instrument und ist kein Ersatz für eine EKG-basierte Diagnostik. Auch beim Smartphone-basierten VHF-Screening besteht klinisch weiterhin Unsicherheit hinsichtlich des Nutzens, der Risikostratifikation und der therapeutischen Konsequenzen.
Die PPG-basierte Rhythmusmessung über Smartphones hat den Grundstein für die Entwicklung moderner Smartwatch-Technologien gelegt, insbesondere für die Integration von EKG-Funktionen. Während sie als frühe Form der digitalen Selbstvermessung eine wichtige Rolle spielten, verlieren sie zunehmend an Relevanz, da Smartwatches inzwischen sowohl PPG als auch medizinisch validierte EKGs direkt am Handgelenk anbieten und damit eine präzisere und klinisch verwertbarere Diagnostik ermöglichen.
EKG-Patches: neue Wege in der Rhythmusdiagnostik
EKG-Patches ermöglichen eine kontinuierliche, unauffällige Rhythmusüberwachung über mehrere Tage oder sogar Wochen hinweg, ohne die Einschränkungen klassischer Holter-Systeme. Insbesondere bei selten auftretenden Arrhythmien bieten sie den Vorteil, relevante Episoden mit höherer Wahrscheinlichkeit zu detektieren. Neben dem technischen Fortschritt aufseiten der Sensorik spielt auch die algorithmische Auswertung eine zunehmend zentrale Rolle. Ein prominentes Beispiel ist die Studie von Hannun et al., veröffentlicht in Nature Medicine im Jahr 2019. Dort wurde ein Deep-Learning-Modell auf 91232 einkanaligen EKGs von 53549 Patienten trainiert und validiert.3 Das resultierende neuronale Netz erreichte eine beeindruckende AUC von 0,97 bei der Klassifikation unterschiedlicher Arrhythmien und bewegte sich damit auf dem diagnostischen Niveau erfahrener Kardiologen.
Darüber hinaus eröffnen Patches neue Versorgungsansätze. Durch die einfache Handhabung und hohe Patientenakzeptanz steigt nicht nur die diagnostische Ausbeute, sondern auch die Effizienz der Abläufe, insbesondere dann, wenn die Daten algorithmisch voranalysiert und telemedizinisch weiterverarbeitet werden. Gleichzeitig bleiben Fragen offen, etwa hinsichtlich der tatsächlichen Auswirkungen auf Gesundheitsressourcen, die stark vom jeweiligen Versorgungssystem abhängen. Hier bedarf es weiterer belastbarer Daten. Unbestritten ist jedoch: Patches verändern bereits heute die Art und Weise, wie wir Rhythmusdiagnostik denken, und schaffen Raum für patientenzentrierte, flexible und zugleich hochpräzise Versorgungspfade.
Holter-EKG vs. ILR – diagnostische Ausbeute bei unklarer Synkope
Bei der Abklärung unklarer Synkopen hat das klassische 24- oder 48-Stunden-Holter-EKG weiterhin seinen festen Platz, insbesondere bei häufig auftretenden Episoden.4 Doch bei seltenen, unvorhersehbaren Ereignissen stösst es an seine diagnostischen Grenzen. Implantierbare Loop-Rekorder (ILR) bieten hier eine überlegene Alternative. Sie ermöglichen eine kontinuierliche Langzeitüberwachung über Monate bis Jahre hinweg und damit eine deutlich höhere Wahrscheinlichkeit, die Synkopen auslösende Rhythmusstörung zu detektieren.
Eine Metaanalyse randomisierter Studien, publiziert in den ESC-Leitlinien zur Synkope 2018, zeigt eindrucksvoll die Überlegenheit der ILR-Strategie. Die gepoolte diagnostische Ausbeute lag in der ILR-Gruppe bei 46% gegenüber nur 12% in den Kontrollgruppen mit konventioneller Diagnostik bei einer relativen Wahrscheinlichkeit von 3,6 (95% CI: 2,4–5,3; p=0,001). Besonders auffällig ist die Konstanz des Effekts über verschiedene Studien hinweg, ungeachtet der jeweils verwendeten Kontrollstrategie.4
Entsprechend ist der Einsatz eines ILR bei Patienten mit hohem Risiko und fehlendem Anhalt für eine strukturelle Ursache nach umfassender Abklärung mit einer Klasse-I-Empfehlung (Evidenzgrad A) versehen. Für das Holter-EKG hingegen bleibt festzuhalten: Es eignet sich zur kurzfristigen Erfassung häufiger Arrhythmien, bietet aber in der Abklärung seltener, unklarer Synkopen nur begrenzten diagnostischen Mehrwert.
Fazit
Smartphones, Wearables, Patches und KI-basierte Analyseverfahren revolutionieren die Rhythmusdiagnostik. Sie ermöglichen eine bislang ungeahnte Niedrigschwelligkeit, Verfügbarkeit und Datenfülle. Doch ersetzen sie damit konventionelle Verfahren wie das Holter-EKG oder implantierbare Loop-Rekorder? Die Antwort ist differenziert: In der Erfassung häufiger Arrhythmien bei kurzfristiger Fragestellung bleibt das Holter-EKG weiterhin ein bewährtes Instrument, wenngleich auch zunehmend unter Druck. Bei seltenen, unvorhersehbaren Synkopen hingegen sind Loop-Rekorder der diagnostische Goldstandard, wie die ESC-Leitlinien eindrücklich belegen.
Wearables und Patches eröffnen neue Wege, sind aber bisher nur für ausgewählte Indikationen zugelassen und häufig nicht in strukturierte Versorgungspfade eingebettet. Ihr volles Potenzial entfalten sie erst dann, wenn technische Präzision, algorithmische Auswertung und klinische Relevanz sauber ineinandergreifen. Bis dahin gilt: nicht entweder – oder, sondern die richtige Methode für die richtige Fragestellung beim richtigen Patienten. Die Zukunft der Rhythmusdiagnostik liegt in der intelligenten Kombination traditioneller Verfahren mit digitalen Innovationen.
Literatur:
1 Mannhart D et al.: Clinical validation of 5 direct-to-consumer wearable smart devices to detect atrial fibrillation: BASEL Wearable Study. JACC Clin Electrophysiol 2023; 9: 232-42 2 Isenegger C et al.: Accuracy of smartwatches for atrial fibrillation detection over time: insights from the Basel Wearable Study. JACC Clin Electrophysiol 2024; 10: 2735-7 3 Hannun AY et al.: Cardiologist-level arrhythmia detection and classification in ambulatory electrocardiograms using a deep neural network. Nat Med 2019; 25: 65-9 4 Brignole M et al.: 2018 ESC Guidelines for the diagnosis and management of syncope. Eur Heart J 2018; 39: 1883-948
Das könnte Sie auch interessieren:
Funktionsstörung des Myokards: wenn die Entspannung des Herzens gestört ist
Die hypertropheobstruktive Kardiomyopathie (HOCM) ist dadurch charakterisiert, dass die Entspannung des Myokards funktionsgestört ist. Die Folge ist eine zunehmende Verdickung der ...
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...