Diabetes mellitus: Welcher Patient hat ein kardiales Risiko und was hilft präventiv?
Autoren:
Dr. Suriya Prausmüller
Priv.-Doz. DDr. Thomas Zelniker, MSc
Abteilung für Kardiologie
Universitätsklinik für Innere Medizin II
Medizinische Universität Wien
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Eine Diabeteserkrankung ist mit einem deutlich erhöhten kardiovaskulären Risiko assoziiert. Eine frühzeitige Diagnose und Behandlung sind daher entscheidend. Die aktuellen ESC/EASD-Diabetesleitlinien berücksichtigen die Ergebnisse großer prospektiver kardiovaskulärer Endpunktstudien, die eine Prognoseverbesserung durch SGLT2-Inhibitoren und GLP-1-Rezeptoragonisten belegen.
Keypoints
-
Um das kardiovaskuläre Risiko von Patienten mit Diabetes langfristig zu senken, bedarf es eines multifaktoriellen Therapieansatzes, der die Behandlung der kardiovaskulären Risikofaktoren berücksichtigt.
-
In den ESC/EASD-Leitlinien zählt die Behandlung mit SGLT2-Inhibitoren/GLP-1-Rezeptoragonisten als medikamentöse First-Line-Therapie bei Patienten mit neu diagnostiziertem Typ-2-Diabetes und hohem/sehr hohem kardiovaskulärem Risiko.
-
SGLT2-Inhibitoren und GLP-1-Rezeptoragonisten sind kardio- und nephroprotektive Antidiabetika, die das Management von T2D-Patienten maßgeblich veränderten.
-
Neben konventionellen Risikoalgorithmen gilt der Biomarker NT-proBNP als hilfreicher Marker zur Risikostratifizierung von Herzinsuffizienz und kardiovaskulärem Tod bei Patienten mit Diabetes mellitus.
Diabetes und kardiovaskuläres Risiko
Patienten mit Typ-2-Diabetes mellitus (T2D) haben ein deutlich erhöhtes Risiko für das Auftreten von koronarer Herzerkrankung, Herzinsuffizienz, Herzrhythmusstörungen und chronischer Niereninsuffizienz.1 Das erhöhte kardiovaskuläre Risiko betrifft jedoch nicht alle Patienten mit T2D gleichermaßen.2 Dies unterstreicht die Notwendigkeit einer differenzierten und individualisierten Risikostratifizierung. Zudem erfordert die signifikant erhöhte kardiovaskuläre Morbidität und Mortalität bei T2D ein umfassendes Risikomanagement. Hier eröffnen die kardio- und nephroprotektiven Antidiabetika SGLT2-Inhibitoren (SGLT2-I) und GLP-1-Rezeptoragonisten (GLP-1-RA) neue therapeutische Perspektiven.
Wie das Risiko abschätzen?
Konventionelle Risikoalgorithmen
Die 2019 veröffentlichten ESC-EASD-Leitlinien zu Diabetes, Prädiabetes und kardiovaskulären Erkrankungen empfehlen eine Risikokategorisierung basierend auf den Risikogruppen „sehr hohes Risiko“, „hohes Risiko“ und „moderates Risiko“ zur Abschätzung des 10-Jahres-Risikos für tödliche kardiovaskuläre Erkrankungen bei Menschen mit Diabetes (Tab. 1).3
-
Zur Gruppe von Patienten mit sehr hohem Risiko werden Diabetespatienten mit bestehender kardiovaskulärer Erkrankung, mit Zeichen von Endorganschäden (Proteinurie, eGFR <30ml/min/1,73m2, linksventrikuläre Hypertrophie, Retinopathie), mit ≥3 Risikofaktoren (Alter, Hypertonie, Dyslipidämie, Rauchen, Adipositas) oder mit einer Typ-1-Diabetesdauer >20 Jahre gezählt.
-
Ein hohes Risiko liegt bei einer Diabetesdauer länger als 10 Jahre ohne Endorganschaden, aber mit zusätzlichen Risikofaktoren vor.
-
Zur Population mit moderatem Risiko zählen jüngere Patienten (Typ-1-Diabetes und <35 Jahren oder T2D und <50 Jahren) mit einer Diabetesdauer von weniger als 10 Jahren ohne jegliche Risikofaktoren.
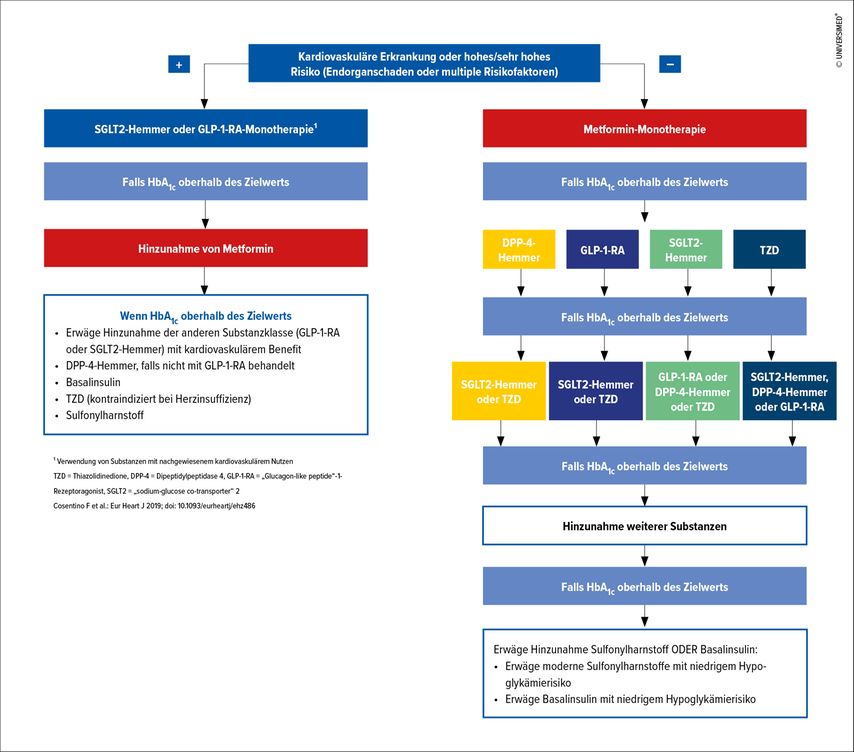
Wenngleich jüngste epidemiologische Daten zeigen, dass nach dieser Risikobewertung der Großteil der Diabetiker in die Gruppen „hohes“ und „sehr hohes Risiko“ fällt,4 empfehlen die ESC/EASD-Leitlinien, die medikamentösen Behandlungsentscheidungen auf der Grundlage dieses Modells zu treffen (Abb. 1). Hervorzuheben ist hier, dass SGLT2-I und GLP-1-RA erstmals Metformin als First-Line-Therapie bei therapienaiven Diabetikern mit hohem oder sehr hohem kardiovaskulärem Risiko ablösen.
Abb. 1: Behandlungsalgorithmus bei therapienaiven Typ-2-Diabetespatienten mit kardiovaskulärer Erkrankung oder hohem/sehr hohem kardiovaskulärem Risiko (adaptiert nach Cosentino F et al.)3
Dass SGLT2-I und GLP-1-RA dem Metformin vorgezogen werden sollen, wird derzeit allerdings von anderen Fachgesellschaften wie der American Diabetes Association und der Österreichischen Diabetes Gesellschaft nicht empfohlen. Im Gegensatz zu den ESC/EASD-Leitlinien empfehlen diese weiterhin Metformin als First-Line-Therapie bei therapienaiven Patienten mit T2D. Unabhängig vom HbA1c soll bei Atherosklerose-assoziierter Erkrankung eine Therapie mit SGLT2-I oder GLP-1-RA etabliert werden. Steht eine Herzinsuffizienz oder eine chronische Niereninsuffizienz im Vordergrund, soll eine Therapie mit SGLT2-I begonnen werden.
Um speziell das individuelle Herzinsuffizienzrisiko bei Patienten mit T2D zu erfassen, wurde 2019 von der TIMI Study Group ein Risikoscore entwickelt, der auf fünf einfach zu erhebenden klinischen Variablen basiert (Herzinsuffizienz, Vorhofflimmern, koronare Herzkrankheit, glomeruläre Filtrationsrate und die Albumin-Kreatinin-Ratio).5 Mittlerweile wurde der TIMI-Risikoscore in mehreren unabhängigen Kollektiven validiert und stellt somit ein hilfreiches Tool zur Herzinsuffizienz-Risikoabschätzung bei T2D dar.5–7
Integrative Risikobewertung durch kardiale Marker
Neben der Risikoeinteilung mittels klassischer Risikofaktoren gilt NT-proBNP als zuverlässiger kardialer Biomarker zur Einschätzung des individuellen Risikos für Herzinsuffizienz bei T2D. Zudem scheinen erhöhte NT-proBNP-Konzentrationen auch mit einem erhöhten Risiko für eine Progression einer chronischen Niereninsuffizienz bei T2D assoziiert zu sein.8
Zahlreiche Studien zeigten, dass erhöhte NT-proBNP-Werte (>125pg/ml) selbst in T2D-Patienten ohne vorbekannte kardiovaskuläre Erkrankung und unabhängig von Risikofaktoren mit einem stark erhöhten kardiovaskulären Risiko einhergehen.9,10 In der bedeutenden PONTIAC-Studie konnte gezeigt werden, dass durch Bestimmung natriuretischer Peptide T2D-Patienten ohne kardiovaskuläre Erkrankungen identifiziert werden können, die von einer frühzeitigen kardioprotektiven Therapie mit RAAS-Hemmern und Betablockern besonders profitieren.11 Die Bestimmung von NT-proBNP scheint daher die Aussagekraft vieler Risikofaktoren zusammenzufassen und ermöglicht so eine integrative Bewertung des kardiovaskulären und des Mortalitätsrisikos sowohl bei Personen mit als auch ohne bekannte Risikofaktoren.12 Aufgrund dieser Evidenzlage erhielt das NT-proBNP dieses Jahr eine CE-Zertifizierung als Risikomarker bei Diabetes.13
Wie kardiovaskuläres Risiko senken?
Multifaktorielles Management
Eine optimale Behandlung zur Senkung des kardiovaskulären Risikos beinhaltet ein umfassendes Management von Lebensstil, Risikofaktoren sowie pharmakologischer Therapie. So konnte bereits in der STENO-2-Studie eindrücklich gezeigt werden, dass ein multifaktorieller Therapieansatz bei T2D zu einer bis um die Hälfte niedrigeren Rate an makrovaskulären sowie mikrovaskulären Komplikationen führt.14
Blutzuckerkontrolle
Evidenzlage
In großen prospektiven, randomisierten kontrollierten Studien wie ACCORD, ADVANCE und VADT mit insgesamt mehr als 23000 Studienteilnehmern führte eine intensivierte Blutzuckereinstellung zu einer Reduktion der Rate an mikrovaskulären Komplikationen. Ein Benefit hinsichtlich makrovaskulärer Komplikationen konnte jedoch nicht gezeigt werden.15–17 Langzeitdaten der UKPDS-Studie suggerieren, dass sich eine strikte Blutzuckerkontrolle vornehmlich bei Patienten mit kurzer Diabetesdauer ohne relevante Komorbiditäten günstig auf das kardiovaskuläre Outcome auswirkt.18 Insgesamt deuten diese Daten darauf hin, dass die alleinige Blutzuckersenkung unzureichend ist, um das kardiovaskuläre Risiko bei Patienten mit Diabetes zu senken. Zudem sollte unbedingt das Risiko für Hypoglykämien reduziert werden.
Therapieempfehlung (ESC/EASD 2019)
Prinzipiell wird eine strenge Glukosekontrolle empfohlen, die auf ein nahezu normales HbA1c (<7,0% oder <53mmol/mol) abzielt, um mikrovaskuläre Komplikationen bei Diabetes zu verringern (Empfehlungsgrad 1, Evidenz A). Die HbA1c-Ziele sollen jedoch nach Dauer des Diabetes, Begleiterkrankungen und Alter individuell festgelegt werden (Empfehlungsgrad 1, Evidenz C).
Kardioprotektion durch Einsatz neuer Antidiabetika
Neben der Kontrolle konventioneller Risikofaktoren eröffnen kardio- und nephroprotektive Antidiabetika neue therapeutische Möglichkeiten, um das kardiorenale Risiko zu senken. So konnte in großen randomisiert kontrollierten kardiovaskulären Endpunktstudien gezeigt werden, dass der Einsatz von SGLT2-I sowie GLP-1-RA unabhängig von der HbA1c-Senkung zu einer Reduktion des kardiorenalen Risikos führt.
SGLT2-Inhibitoren
Evidenzlage
SGLT2-I reduzieren vor allem Hospitalisationen wegen Herzinsuffizienz und verlangsamen die Progression einer chronischen Niereninsuffizienz.19 Der therapeutische Nutzen dürfte aber nicht nur auf T2D-Patienten beschränkt sein: In groß angelegten Studien konnte gezeigt werden, dass auch Patienten mit chronischer Niereninsuffizienz und Herzinsuffizienz mit reduzierter Ejektionsfraktion unabhängig vom Diabetesstatus von SGLT2-I profitieren.20,21 Darüber hinaus wurde vor Kurzem ein Nutzen von Empagliflozin bei Herzinsuffizienz mit erhaltener Linksventrikelfunktion in einer Pressemitteilung veröffentlicht.22 Die detaillierten Ergebnisse werden beim diesjährigen europäischen Kardiologiekongress vorgestellt. Der SGLT2-I Dapagliflozin wurde kürzlich auch bei Patienten mit einer SARS-CoV-2-Infektion untersucht. Wenngleich die zwei primären Endpunkte (Prävention von Organversagen oder Mortalität und Genesung von der Erkrankung) nicht signifikant reduziert wurden, konnte das gute Sicherheitsprofil erneut bestätigt werden.23
Indikation zur Therapie (ESC/EASD 2019)
Empagliflozin, Canagliflozin oder Dapagliflozin werden für Patienten mit T2D und etablierter kardiovaskulärer Erkrankung oder mit einem hohen/sehr hohen kardiovaskulären Risiko empfohlen, um kardiovaskuläre Ereignisse zu reduzieren (Empfehlungsgrad I, Evidenzgrad A).
GLP-1-Rezeptoragonisten
Evidenzlage
GLP-1-RA reduzieren vor allem Atherosklerose-assoziierte Ereignisse.24 Zudem verzögert die Anwendung von GLP-1-RA das Risiko für das Voranschreiten einer Nierenschädigung (insbesondere die Progression einer Albuminurie) und führt zu einer langfristigen Gewichtsreduktion.25
Indikation zur Therapie (ESC/EASD 2019)
Liraglutid, Semaglutid oder Dulaglutid werden für Patienten mit T2D und kardiovaskulärer Erkrankung oder einem sehr hohen/hohen kardiovaskulären Risiko empfohlen, um kardiovaskuläre Ereignisse zu reduzieren (Empfehlungsgrad 1, Evidenz A).
Lipidsenkung
Evidenzlage
Über zwei Drittel der Diabetiker weisen eine Lipidstoffwechselstörung auf, die maßgeblich zu einem erhöhten kardiovaskulären Risiko beiträgt.26 Zahlreiche klinische Studien haben die positiven Auswirkungen einer Statintherapie hinsichtlich kardiovaskulären Outcomes bei Patienten mit und ohne koronare Herzerkrankung gezeigt.27,28 Eine Metaanalyse, die Daten von über 18000 Patienten mit Diabetes aus 14 randomisierten Studien zur Statintherapie umfasst, zeigte für jedes mmol/l (39mg/dl) Senkung des LDL-Cholesterins eine proportionale Reduktion der Gesamtmortalität um 9% und der kardiovaskulären Mortalität um 13% auf.29
Therapieempfehlung (ESC/EASD 2019)
Bei Patienten mit T2D und einem sehr hohen kardiovaskulären Risiko wird ein LDL-Cholesterinzielwert <55mg/dl und eine mindestens 50%ige LDL-C-Reduktion empfohlen (Empfehlungsgrad 1, Evidenz B).
Antihypertensive Therapie
Evidenzlage
Hypertonie zählt zu einer der häufigsten Komorbiditäten des Diabetes und geht mit einem signifikant erhöhten kardiovaskulären Risiko einher. So konnte in den drei großen Interventionsstudien ABCD, UKPDS und HOT eindrücklich gezeigt werden, dass eine intensive Blutdruckeinstellung zu einer Senkung der Rate an mikro- und auch makrovaskulären Komplikationen führt.30-32 Eine rezent publizierte Metaanalyse, die 48 randomisierte Studien mit 344716 Patienten umfasste, zeigte, dass die Senkung des systolischen Blutdrucks um 5mmHg zu einer signifikanten Reduktion des relativen Risikos für schwerwiegende kardiovaskuläre Ereignisse um etwa 10% selbst bei Patienten mit normalen oder leicht erhöhten Werten führt.33 Bei der Behandlung des Bluthochdrucks sollten Kombinationspräparate bevorzugt werden, da dadurch die Compliance erhöht wird und der Blutdruck langfristig gesenkt werden kann.34
Therapieempfehlung (ESC/EASD 2019)
Die Blutdruckzielwerte haben sich in den vergangenen Jahrzehnten mehrfach geändert. Die ESC und die EASD empfehlen die Einleitung einer blutdrucksenkenden medikamentösen Behandlung bei Diabetikern mit einem Praxis-Blutdruck >140/90mmHg (Empfehlungsgrad 1, Evidenz A). Der Blutdruckzielwert sollte laut ESC/EASD bei Diabetikern <130mmHg liegen, bei älteren Patienten (>65 Jahre) sollte der systolische Blutdruckzielwert in einem Bereich von 130–139mmHg liegen (Empfehlungsgrad 1, Evidenz A).
Lebensstilintervention
Evidenzlage
Die Änderung des Lebensstils stellt einen wesentlichen Bestandteil des Managements des kardiovaskulären Risikos dar.
Therapieempfehlung (ESC/EASD 2019)
-
Eine Raucherentwöhnung unter strukturierter Beratung wird allen Patienten mit Diabetes oder Prädiabetes empfohlen (Empfehlungsgrad 1, Evidenz A).
-
Eine reduzierte Kalorienaufnahme wird empfohlen, um ein Normalgewicht anzustreben (Empfehlungsgrad 1, Evidenz A).
-
Eine mittlere bis intensive körperliche Aktivität, insbesondere eine Kombination aus aerobem Ausdauertraining und Krafttraining, von ≥150 Minuten/Woche wird empfohlen (Empfehlungsgrad 1, Evidenz A).
Literatur:
1 Einarson TR et al.: Prevalence of cardiovascular disease in type 2 diabetes: a systematic literature review of scientific evidence from across the world in 2007-2017. Cardiovasc Diabetol 2018; 17: 83 2 Bertoluci MC et al.: Cardiovascular risk assessment in patients with diabetes. Diabetol Metab Syndr 2017; 9: 1-13 3 Cosentino F et al.: 2019 ESC Guidelines on diabetes, pre-diabetes, and cardiovascular diseases developed in collaboration with the EASD. Eur Heart J 2019: 1-69 4 Prausmüller S et al.: Performance of the recommended ESC/EASD cardiovascular risk stratification model in comparison to SCORE and NT-proBNP as a single biomarker for risk prediction in type 2 diabetes mellitus. Cardiovasc Diabetol 2021; 20: 34 5 Berg DD et al.: Heart failure risk stratification and efficacy of sodium-glucose cotransporter-2 inhibitors in patients with type 2 diabetes mellitus. Circulation 2019; 140: 1569-77 6 Elharram M et al.: Prediction of heart failure outcomes in patients with type 2 diabetes mellitus: validation of the Thrombolysis in Myocardial Infarction Risk Score for Heart Failure in Diabetes (TRS-HFDM) in patients in the ACCORD trial. Diabetes Obes Metab 2021; 23: 782-90 7 Verma S et al.: Empagliflozin reduces the risk of mortality and hospitalization for heart failure across Thrombolysis in Myocardial Infarction Risk Score for Heart Failure in Diabetes categories: post hoc analysis of the EMPA-REG OUTCOME trial. Diabetes Obes Metab 2020; 22: 1141-50 8 Zelniker TA et al.: Cardiac and inflammatory biomarkers are associated with worsening renal outcomes in patients with type 2 diabetes mellitus: observations from SAVOR-TIMI 53. Clin Chem 2019; 65: 781-90 9 Nambi V et al.: Natriuretic peptides and integrated risk assessment for cardiovascular disease: an individual-participant-data meta-analysis. Lancet Diabetes Endocrinol 2016; 4: 840-9 10Zelniker TA et al.: Relationship between baseline cardiac biomarkers and cardiovascular death or hospitalization for heart failure with and without sodium-glucose co-transporter 2 inhibitor therapy in DECLARE-TIMI 58. Eur J Heart Fail 2021; 23: 1026-36 11 Huelsmann M et al.: PONTIAC (NT-proBNP selected prevention of cardiac events in a population of diabetic patients without a history of cardiac disease): a prospective randomized controlled trial. J Am Coll Cardiol 2013; 62: 1365-72 12 Malachias MVB et al.: NT-proBNP by itself predicts death and cardiovascular events in high-risk patients with type 2 diabetes mellitus. J Am Heart Assoc 2020; 9(19): e017462 13 Roche launches new ways to use their cardiovascular tests empowering clinicians to improve diagnosis and treatment of millions of people. https://www.roche.com/media/releases/med-cor-2021-04-28b.htm (accessed July 28, 2021) 14 Gaede P et al.: Effect of a multifactorial intervention on mortality in type 2 diabetes. N Engl J Med 2008; 358: 580-91 15 Gerstein HC et al.: Effects of intensive glucose lowering in type 2 diabetes. N Engl J Med 2008; 358: 2545-59 16 Patel A et al.: Intensive blood glucose control and vascular outcomes in patients with type 2 diabetes. N Engl J Med 2008; 358: 2560-72 17 Duckworth W et al.: Glucose control and vascular complications in veterans with type 2 diabetes. N Engl J Med 2009; 360: 129-39 18 Holman RR et al.: 10-year follow-up of intensive glucose control in type 2 diabetes. N Engl J Med 2008; 359: 1577-89 19 Zelniker TA et al.: SGLT2 inhibitors for primary and secondary prevention of cardiovascular and renal outcomes in type 2 diabetes: a systematic review and meta-analysis of cardiovascular outcome trials. Lancet 2019; 393: 31-9 20Heerspink HJL et al.: Dapagliflozin in patients with chronic kidney disease. N Engl J Med 2020; 383: 1436-46 21 McMurray JJV et al.: Dapagliflozin in patients with heart failure and reduced ejection fraction. N Engl J Med 2019; 381: 1995-2008 22 Breakthrough results for empagliflozin confirm EMPEROR-Preserved as first and only successful trial for heart failure with preserved ejection fraction. https://www.boehringer-ingelheim.com/press-release/emperor-preserved-heart-failure-toplineresults (accessed July 28, 2021) 23 Kosiborod MN et al.: Dapagliflozin in patients with cardiometabolic risk factors hospitalised with COVID-19 (DARE-19): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Diabetes Endocrinol 2021. doi: 10.1016/S2213-8587(21)00180-7 24 Kristensen SL et al.: Cardiovascular, mortality, and kidney outcomes with GLP-1 receptor agonists in patients with type 2 diabetes: a systematic review and meta-analysis of cardiovascular outcome trials. Lancet Diabetes Endocrinol 2019; 7: 776-85 25 Vilsbøll T et al.: Effects of glucagon-like peptide-1 receptor agonists on weight loss: systematic review and meta-analyses of randomised controlled trials. BMJ 2012; 344: d7771 26 Kaze AD et al.: Metabolic dyslipidemia and cardiovascular outcomes in type 2 diabetes mellitus: findings from the Look AHEAD Study. J Am Heart Assoc 2021; 10: e016947 27 Mihaylova B et al.: The effects of lowering LDL cholesterol with statin therapy in people at low risk of vascular disease: meta-analysis of individual data from 27 randomised trials. Lancet 2012; 380: 581-90 28 Baigent C et al.: Efficacy and safety of cholesterol-lowering treatment: prospective meta-analysis of data from 90,056 participants in 14 randomised trials of statins. Lancet 2005; 366: 1267-78 29Kearney PM et al.: Efficacy of cholesterol-lowering therapy in 18,686 people with diabetes in 14 randomised trials of statins: a meta-analysis. Lancet 2008; 371: 117-25 30 Schrier RW et al.: Appropriate blood pressure control in hypertensive and normotensive type 2 diabetes mellitus: a summary of the ABCD trial. Nat Clin Pract Nephrol 2007; 3: 428-38 31 Hansson L et al.: Effects of intensive blood-pressure lowering and low-dose aspirin in patients with hypertension: principal results of the Hypertension Optimal Treatment (HOT) randomised trial. HOT Study Group. Lancet 1998; 351: 1755-62 32 Tight blood pressure control and risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 38. UK Prospective Diabetes Study Group. BMJ 1998; 317: 703-13 33 Blood Pressure Lowering Treatment Trialistsʼ Collaboration: Pharmacological blood pressure lowering for primary and secondary prevention of cardiovascular disease across different levels of blood pressure: an individual participant-level data meta-analysis. Lancet 2021; 397: 1625-36 34 Chow CK et al.: Quarter-dose quadruple combination therapy for initial treatment of hypertension: placebo-controlled, crossover, randomised trial and systematic review. Lancet 2017; 389: 1035-42
Das könnte Sie auch interessieren:
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
(Neue) Blutdruckziele im klinischen Alltag?
Die Diskussion um optimale Blutdruckwerte erhält durch eine aktuelle Analyse aus den USA eine neue Dynamik: Im klinischen Alltag war ein systolischer Blutdruck zwischen 130 und 139mmHg ...