HIV-Remission, perinatale Transmission und neuer Therapieansatz bei Kindern
Bericht:
Mag. Birgit Leichsenring
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Zwischen 13. und 24. Februar 2022 fand die 29. Conference on Retroviruses and Opportunistic Infections, kurz CROI 2022, statt. Obwohl die Konferenz bereits zum dritten Mal im Zuge der Coronaviruspandemie online durchgeführt wurde, hat sie nichts von ihrem speziellen Ambiente verloren.
Auch online ist die Anzahl der Teilnehmer der CROI 2022 streng limitiert – heuer waren es 3300 Personen. Das rein wissenschaftlich ausgerichtete Programm inkludierte ca. 900 Beiträge, davon 92 allgemeine Vorträge, 17 „Late breaking“-Vorträge und 768 Posterpräsentation. Der Anspruch an die präsentierten Daten zeigt sich im Auswahlverfahren: Nur etwas über 50% der eingereichten Abstracts wurden angenommen. Zu Recht gilt die CROI daher als jährlicher Höhepunkt in der HIV-Forschung.
Highlight: Fall einer HIV-Remission
Als mediales Highlight darf der präsentierte Fall einer weiteren HIV-Remission gewertet werden.1 Bei einer 2013 mit HIV diagnostizierten und unter effektiver HIV-Therapie stehenden US-amerikanischen Frau mittleren Alters entwickelte sich zusätzlich eine akute myeloische Leukämie (AML). Für die nachfolgende Stammzelltransplantation wurde erstmals Nabelschnurblut mit homozygoter CCR5-Δ32-Deletion verwendet. Diese selten auftretende Mutation führt zu einem veränderten CCR5-Oberflächenrezeptor auf CD4-Zellen, welcher im Regelfall für Fusion und folglich Infektion der Zelle durch HIV notwendig ist. Mit ca. 1% hat diese CCR5-Mutation in der nordeuropäischen Bevölkerung die höchste Prävalenz.
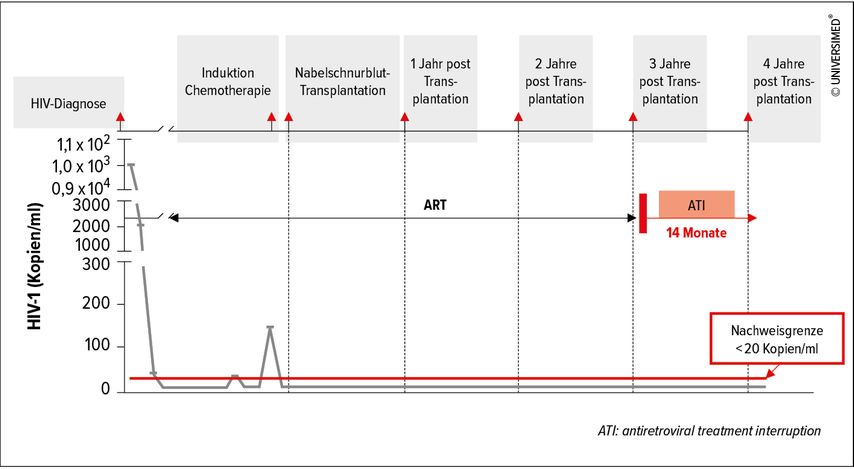
Die Patientin tolerierte Transplantation und Chemotherapie gut, insbesondere kam es zu keiner akuten oder chronischen GVHD („graft versus host disease“). 37 Monate nach Transplantation wurde die HIV-Therapie (antiretrovirale Therapie; ART) abgesetzt. Die Patientin nimmt aktuell seit knapp 1,5 Jahren keine ART ein und es kam zu keinem viralen Rebound. Es ist keine HIV-1-DNA nachweisbar und mittlerweile ist die Patientin seronegativ (Abb.1).1 Es handelt sich somit um den dritten publizierten Fall einer vermutlichen Heilung. Bisher wurde beim sog. Berliner und beim Londoner Patienten ebenfalls nach einer Knochenmarkstransplantation inklusive Donor mit CCR5-Δ32-Deletion die ART abgesetzt und kein viraler Rebound beobachtet. Das Besondere in diesem Fall ist nicht nur, dass es sich erstmals um eine Frau handelt, sondern zusätzlich ihr gemischter ethnischer Hintergrund. Hier gestaltet sich das Finden eines passenden Donors besonders schwierig. Der Ansatz, auf Nabelschnurblut zurückzugreifen, könnte daher wegweisend für zukünftige ähnlich gelagerte Fälle sein.
Abb. 1: Zeitlicher Ablauf der Behandlung vs. Viruslastprofil der Studienteilnehmerin für HIV-1 vor und nach der Stammzellentransplantation mit Nabelschnurblut mit homozygoter CCR5-Δ32-Deletion (modifiziert nach Bryson Y et al. 2022)1
Unterschiede im HIV-Lebenszeitrisiko
Die Ungleichverteilung von HIV-Prävalenz und Inzidenz aufgrund soziodemografischer und gesellschaftspolitischer Aspekte ist hinlänglich bekannt. Dennoch verändert sich diese Situation trotz vieler Bemühungen nur marginal, wie eine US-amerikanische Studie erneut aufzeigte.2
Basierend auf den Daten des NHSS (National HIV Surveillance System) wurde das Risiko für eine HIV-Infektion auf Lebenszeit in den USA berechnet.2 Im Zeitraum 2017–2019 lag das Gesamtrisiko bei 1:120, jedoch mit signifikanten Unterschieden in Bezug auf Geschlecht und Ethnie.2 Das Lebenszeitrisiko für afroamerikanische Männer lag bei 1:27, für weiße Männer hingegen bei 1:171. Noch deutlicher war die Differenz bei Frauen zu sehen: Afroamerikanische Frauen hatten ein HIV-Lebenszeitrisiko von 1:75 und weiße Frauen von 1:874.
Es wurden zwar 11% Reduktion des Gesamtrisikos im Vergleich zu 2010–2014 beobachtet, jedoch nicht gleichwertig in allen Populationsgruppen.2 Die Daten zeigen deutlich, dass die Bemühungen in HIV-Prävention und in der Verfügbarkeit der HIV-Therapie weiterhin verstärkt werden müssen.
Unterschiede in Covid-19-Impfraten der HIV-positiven Bevölkerung
HIV-positive Menschen haben aus diversen Gründen ein statistisch erhöhtes Risiko für einen schwereren Covid-19-Verlauf. Die Covid-19-Impfung ist daher besonders empfohlen. Eine Auswertung einer internationalen (Covid-19-unabhängigen) Studie gab Einsicht in die Impfraten der HIV-positiven Bevölkerung.3
Die REPRIEVE-Studie untersuchte kardiovaskuläre Ereignisse bei HIV-positiven Patienten in über 100 Zentren auf 5 Kontinenten. Es wurde von knapp 7000 dieser Patienten der Impfstatus erhoben. Die durchschnittliche Durchimpfungsrate lag bei 47%, wobei regional drastische Unterschiede zu verzeichnen waren. In den USA und Peru z.B. lagen die Raten bei 67% und 60%, hingegen in Südafrika und Uganda bei 11% und 3%.
Neben den regionalen Unterschieden gab es die höchsten Impfraten bei Männern und Menschen mit weißer Hautfarbe.
Die Studienautoren betonen, dass mehr Bemühungen notwendig sind, um die Covid-19-Impfraten insbesondere bei vulnerablen Bevölkerungsgruppen, wie HIV-positiven Menschen, zu erhöhen.
Keine perinatalen Transmissionen bei ART-Start vor Schwangerschaft
Das Risiko für eine vertikale HIV-Transmission von Mutter zu Kind ist direkt mit der Viruslast und dem Therapiestatus der Mutter assoziiert. Eine französische Studie zeigte eindrücklich den Effekt einer HIV-Therapie (ART) der Schwangeren auf das Risiko für perinatale Transmission (PT).4
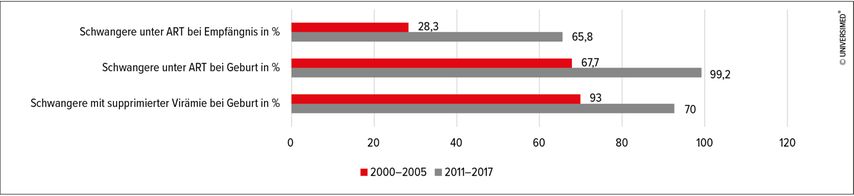
Es wurden Schwangerschaften von 14630 HIV-positiven Frauen im Zeitraum 2000–2017 analysiert. Der Anteil an Frauen, die bereits zum Zeitpunkt der Empfängnis unter ART standen, stieg im Laufe der Jahre von 28,3% auf 65,8% an.Gleichfalls erhöhte sich der Anteil an Schwangeren unter ART zum Zeitpunkt der Geburt von 67,7% auf 99,2%. Hatten zu Beginn des Beobachtungszeitraums 70% eine supprimierte Virämie zum Zeitpunkt der Geburt, waren es am Ende 93% der Frauen (Abb. 2).
Abb. 2: Zunahme der antiretroviralen Therapie (ART) bei Schwangeren (modifiziert nach Sibiude J et al. 2022)4
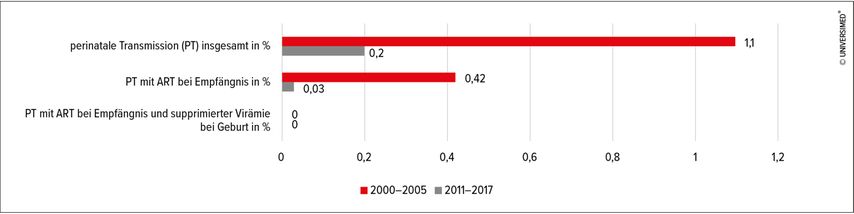
Der Effekt der ART auf die Übertragungen war deutlich sichtbar: Insgesamt sank die PT-Rate von 1,1% auf 0,2%. In der Gruppe der Frauen, die bereits bei Empfängnis eine ART einnahmen, sank die PT-Rate von 0,42% auf 0,03%. Und bei den 5482 Frauen, die sowohl bereits zum Zeitpunkt der Empfängnis eine ART einnahmen als auch zum Zeitpunkt der Geburt eine Viruslast unter der Nachweisgrenze aufwiesen, wurde keine einzige PT beobachtet (Abb. 3).
Zu beachten ist, dass die Frauen nicht stillten und daher potenzielle Übertragungen in der Stillperiode nicht bewertet werden können. Die Studie unterstreicht jedoch, dass dank des Einsatzes einer effektiven ART bereits von Beginn der Schwangerschaft PT ausgeschlossen werden könnten.
Einsatz neutralisierender Breitbandantikörper bei Kindern
Erstmals wurde eine Kombination aus zwei bNAb(„broadly neutralising antibodies“) als Alternative zur herkömmlichen HIV-Therapie bei Kindern untersucht.5
Die TATELO-Studie aus Botswana schloss HIV-positive Kinder ein, die in der ersten Woche nach Geburt mit einer HIV-Therapie begonnen hatten und eine supprimierte Viruslast aufwiesen. Die Kinder, die im Alter zwischen 2 und 6 Jahren waren und eine durchschnittliche CD4-Zellzahl von ca. 1200/µl hatten, erhielten zunächst in einer Brückenphase sowohl ihre ART als auch die beiden bNAb (VRC01LS und 10-1074) in Form einer Infusion alle 4 Wochen. Anschließend wurde die ART abgesetzt. 44% der Kinder (11/25) wiesen nach 6 Monaten mit ausschließlicher bNAb-Therapie nach wie vor eine Viruslast unter der Nachweisgrenze auf.
Die Behandlung wurde gut vertraten und nach Angabe des Autors von den Eltern favorisiert, da die monatliche Infusion im Alltag der Kinder einfacher war als eine tägliche Einnahme. Auch betonte der Autor, dass es sich ausschließlich um eine „Proof of concept“-Studie handle.
Mit der zukünftigen Weiterentwicklung von neutralisierenden Breitbandantikörpern in der HIV-Therapie kann sich hier jedoch eine Option für die Behandlung von HIV-positiven Kindern eröffnen.
Literatur:
1 Bryson Y et al.:HIV-1 remission with CCR5Δ32Δ32 haplo-cord transplant in a U.S. woman: Impaact P1107. CROI 2022, Abstract #65 2 Singh S et al.:Estimating the lifetime risk of a diagnosis of HIV-infection in the United States. CROI 2022, Abstract #45 3 Fulda ES et al.:Covid-19 vaccination rates in a global HIV-Cohort. CROI 2022, Abstract #50 4 Sibiude J et al.:Perinatal HIV-1 transmission in France: U=U for mothers on ART from conception. CROI 2022, Poster #P03 5 Shapiro RL et al.:Treatment with broadly neutralizing antibodies in children with HIV in Botswana. CROI 2022, Abstract #32
Das könnte Sie auch interessieren:
Einsatz von Reserveantibiotika – neue Empfehlungen für die Praxis
Infektionen mit multiresistenten Erregern (MRE) verlaufen häufig schwer bis lebensbedrohlich. Eine neue Leitlinie unterstützt bei der raschen, mikrobiologisch fundierten ...
Guidelines 2025: ein Update
Im Oktober 2025 präsentierte die European AIDS Clinical Society (EACS) eine aktuelle Version ihrer europäischen Behandlungsleitlinien zum Thema HIV/Aids. Seit zwei Jahrzehnten stellen ...
Problemkeimen auf der Spur: mikrobiologisches Screening im Krankenhaus
Mikrobiologisches Screening auf eine Reihe relevanter Erreger zählt zu den Aufgaben der Krankenhaushygiene und verfolgt das Ziel, die Übertragung bestimmter Erreger auf der Station zu ...