Behandlung des nichtmetastasierten kastrationsresistenten Prostatakarzinoms: Welche Substanz ist die beste?
Department für Urologie, <br>Medizinische Universität Innsbruck<br>E-Mail: isabel-maria.heidegger@i-med.ac.at
Klinik und Poliklinik für Urologie und <br>Kinderurologie, Universitätsmedizin Mainz
Department für Urologie, <br>Technische Universität München
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
In den vergangenen Jahren hat die Entwicklung von drei neuen Androgenrezeptor-Antagonisten (AR-Antagonisten) der zweiten Generation (Enzalutamid, Apalutamid und Darolutamid) die Behandlungslandschaft des nichtmetastasierten kastrationsresistenten Prostatakarzinoms (nmCRPC) signifikant verändert, sodass die alleinige Androgendeprivationstherapie mittlerweile eine Ausnahmesituation darstellt.
Keypoints
-
Mit Apalutamid, Darolutamid und Enzalutamid stehen nun drei Androgenrezeptor-Antagonisten der zweiten Generation in der Behandlung des nichtmetastasierten kastrationsresistenten Prostatakarzinoms zur Verfügung.
-
Alle drei Substanzen haben in klinischen Studien einen Benefit im metastasenfreien Überleben (primärer Endpunkt), aber auch im Gesamtüberleben (sekundärer Endpunkt) gezeigt.
-
Alle drei Substanzen sind gut verträglich, sodass die Therapieentscheidung individuell getroffen werden muss.
Apalutamid
Apalutamid ist ein Antiandrogen, das direkt an die Ligandenbindungsdomäne desAR bindet (Abb. 1). Apalutamid wurde von der FDA und von der EMA für die Behandlung des nmCRPC zugelassen, nachdem in einer randomisierten kontrollierten Phase-III-Studie (SPARTAN) ein Vorteil für das metastasenfreie Überleben (MFS) nachgewiesen wurde.1 In dieser Studie wurden 1207 Männer im Verhältnis 2:1 randomisiert, die entweder Apalutamid oder Placebo erhalten hatten. Haupteinschlusskriterien waren das Vorhandensein eines nmCRPC in einer klinischen Hochrisikosituation mit einer PSA-Verdopplungszeit (PSADT) ≤10 Monaten. Das Staging umfasste einen Technetium-99m-Knochenscan und eine Computertomografie (CT). Während das Vorhandensein von Fernmetastasen ein Ausschlusskriterium war, durften Patienten mit Lymphknotenmetastasen <2cm im Becken an der Studie teilnehmen.
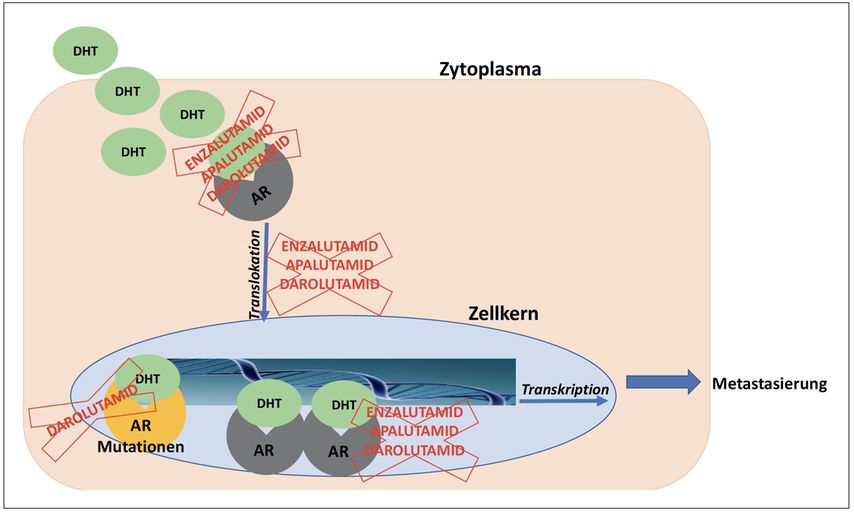
Abb. 1: Angriffspunkte von Apalutamid, Enzalutamid und Darolutamid. AR=Androgenrezeptor, DHT=Dihydrotestosteron
Der primäre EndpunktMFS wurde erreicht, nachdem 378 Ereignisse aufgetreten waren. In der Apalutamid-Gruppe war das MFS mit einem Medianwert von 40,5 Monaten signifikant länger als in der Placebogruppe mit 16,2 Monaten (Hazard-Ratio [HR]: 0,28; 95% Konfidenzintervall [95% CI]: 0,23–0,35; p <0,001).
Vor Kurzem wurden die Überlebensdaten (OS) der SPARTAN-Studie nachgeliefert, welche eine Reduktion der Mortalität um 25% in der Apalutamid-Gruppe im Vergleich zu Placebo zeigten (HR: 0,75; 95% CI: 0,59–0,96; p=0,0197).2 Eine Übersicht über die sekundären Endpunkte der Studie und die häufigsten Nebenwirkungen findet sich in Tabelle 1.
Enzalutamid
Der AR-Inhibitor Enzalutamid wurde ursprünglich für das metastasierte CRPC (AFFIRM- und PREVAIL-Studien) zugelassen und nun auch im nmCRPC getestet. Die Zulassung von Enzalutamid beim nmCRPC basiert auf den Ergebnissen der randomisierten kontrollierten Phase-III-PROSPER-Studie, in der 1401 Patienten mit nmCRPC in einer 2:1-Randomisierung mit Placebo verglichen wurden.3 Auch in dieser Studie hatten alle Patienten ein hohes Metastasierungsrisiko mit einer PSADT von ≤10 Monaten und einem PSA-Ausgangswert von ≥2ng/ml. Das Staging wurde mit CT, Magnetresonanztomografie (MRT) und Knochenscan durchgeführt. Nach 219 (23%) und 228 (49%) Ereignissen zum primären Endpunkt in der Enzalutamid- und der Placebo-Gruppe betrug das mediane MFS 36,6 und 14,7 Monate, wobei Enzalutamid gegenüber Placebo bevorzugt wurde (HR: 0,29; 95% CI: 0,24–0,35; p<0,001) mit einer mittleren Nachbeobachtungszeit von 18,5 und 15,1 Monaten. Vor wenigen Wochen wurde ein Update zum Gesamtüberleben publiziert, welches ein medianes OS von 67 Monaten im Enzalutamid-Arm vs. 56,3 Monate im Placebo-Arm (HR 0,73; 95%CI: 0,61-0,89, p=0001) demonstrierte.4 Eine Übersicht über die sekundären Endpunkte der Studie und die häufigsten Nebenwirkungen ist in Tabelle 1 dargestellt.
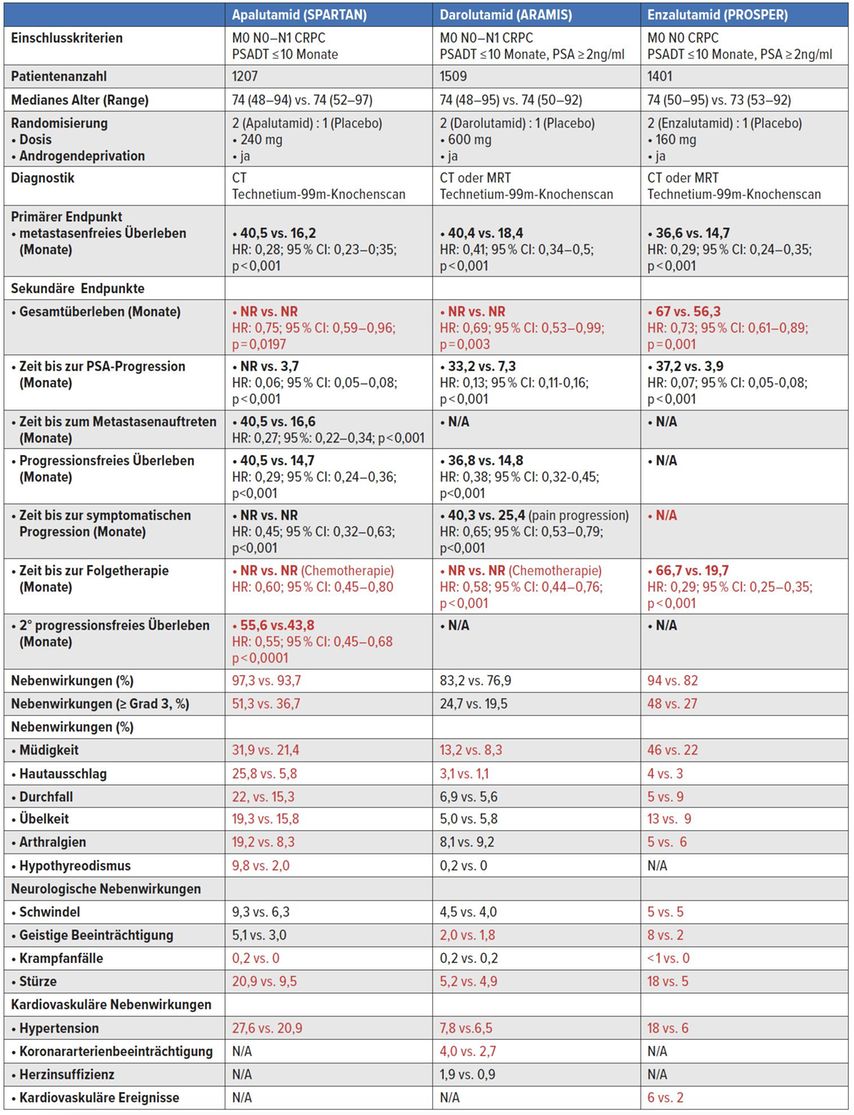
Tab. 1: Überblick über die Ergebnisse von SPARTAN, ARAMIS und PROSPER. Schwarz: Daten der Zulassungsstudien; rot: Updates der Overall-Survival-Studien; NR = nicht erreicht, HR = Hazard-Ratio, PSADT=PSA doubling time, MRT = Magnetresonanztomografie, CT = Computertomografie
Darolutamid
Darolutamid ist wie Enzalutamid und Apalutamid ein nichtsteroidaler AR-Antagonist (Abb. 1). Präklinische Studien zeigten, dass Darolutamid den AR stärker hemmt als andere Antiandrogene der zweiten Generation. Darüber hinaus kann Darolutamid zusätzlich die F876L-Mutation inhibieren, welche unter Enzalutamid- oder Apalutamid-Behandlung entstehen kann.5
Darolutamid hat auch ein geringes Risiko, die Blut-Hirn-Schranke zu passieren, sodass es theoretisch ein geringeres Risiko für zerebrale Nebenwirkungen aufweist als Enzalutamid oder Apalutamid. Das mediane MFS betrug in der Darolutamid-Gruppe 40,4 Monate im Vergleich zu 18,4 Monaten in der Placebo-Gruppe (HR: 0,41; 95% CI: 34–0,50; p <0,001).6 Vor wenigen Wochen wurden am virtuell durchgeführten ASCO2020 die Überlebensdaten nach dem Auftreten von 254 Todesfällen präsentiert, bei denen sich ein Überlebensvorteil von 36 Monaten (HR: 0,69; 95% CI: 0,53-0,88; p=0,003) ergab (J Clin Oncol 38: 2020 [suppl; abstr. 5514]).
Vergleich der Substanzen
Head-to-Head-Studien zu Enzalutamid, Apalutamid und Darolutamid sind nicht verfügbar, daher ist ein direkter Vergleich zwischen den Studien nicht wirklich legitim.
ARAMIS, PROSPER und SPARTAN erreichten jedoch alle ihren primären Endpunkt MFS, der sekundäre Endpunkt OS wurde von allen 3 Substanzen rezent aktualisiert und zeigte in allen 3 Studien einen Benefit im Vergleich zu Placebo.
Festgehalten werden muss auch, dass in die PROSPER-Studie nur Patienten ohne Lymphknotenmetastasen eingeschlossen wurden, während in den StudienSPARTAN und ARAMISLymphknoten mit einem Durchmesser von bis zu 2cm unterhalb der Aortenbifurkation erlaubt waren. Subgruppenanalysen in beiden Studien zeigen einen potenziellen Nutzen von Apalutamid und Darolutamid im N1-Status im Vergleich zu N0 (HR: 0,15 vs. 0,33 bzw. HR: 0,28 vs. 0,46). Apalutamid konnten auch Patienten mit einem PSA Wert <2ng/ml erhalten, wenn die PSADT bei unter 12 Monaten lag, während in den beiden anderen Studien ein PSA-Wert von mindestens 2ng/ml ein Einschlusskriterium war. In Hinblick auf die Nebenwirkungen gibt es ebenfalls keinen direkten Vergleich zwischen Darolutamid, Apalutamid oder Enzalutamid. Darolutamid scheint jedoch weniger Nebenwirkungen zu habenals Apalutamid im Hinblick auf Stürze und Hautausschläge sowie im Vergleich zu Enzalutamid bei Stürzen, Schwindel, psychischen Störungen, Bluthochdruck oder Müdigkeit.
Zusammenfassung
Mit Apalutamid, Darolutamid und Enzalutamid stehen uns seit Kurzem für die Indikation des nmCRPC drei verschiedene Substanzen zur Verfügung, welche alle in klinischen Studien ihre Effektivität bewiesen haben und ein zufriedenstellendes Sicherheitsprofil aufweisen. Daher muss die Entscheidung individuell anhand des Patientenprofils getroffen werden.
Allerdings muss festgehalten werden, dass in den Zulassungsstudien CT und Knochenscans zur Metastasendetektion verwendet wurden, sodass ein nmCRPC-Patient in der Ära des PSMA-PET-CTs in der Rezidivdiagnostik eine Rarität darstellt.
Literatur:
1 Smith MR et al.: Apalutamide treatment and metastasis-free survival in prostate cancer. N Engl J Med 2018; 378(15): 1408-18 2 Small EJ et al.: Apalutamide and overall survival in non-metastatic castration-resistant prostate cancer. Ann Oncol 2019; 30(11): 1813-20 3 Hussain M et al.: Enzalutamide in men with nonmetastatic, castration-resistant prostate cancer. N Engl J Med 2018; 378(26): 2465-74 4 Sternberg CN et al.: Enzalutamide and survival in nonmetastatic, castration-resistant prostate cancer. N Engl J Med 2020; 382(23): 2197-206 5 Korpal M et al.: An F876L mutation in androgen receptor confers genetic and phenotypic resistance to MDV3100 (enzalutamide). Cancer Discov 2013; 3(9): 1030-43 6 Fizazi K et al.: Darolutamide in Nonmetastatic, Castration-resistant prostate cancer. N Engl J Med 2019; 380(13): 1235-46
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Anamnese oder präoperatives Gerinnungsscreening?
Blutgerinnungsstörungen können zu intra- wie auch postoperativen Blutungen führen, die abhängig von Lokalisation und Schweregrad ernste Folgen nach sich ziehen können. Ziel einer ...
CAR-T-Zellen: Stellenwert – klinische Evidenz – Herausforderungen
„Chimeric antigen receptor“(CAR)-T-Zellen sind eine der bedeutendsten Innovationen der modernen Hämatologie. Es handelt sich dabei um autologe, genetisch modifizierte T-Zellen, die ex ...