.jpg)
Die Krux mit Pflastern: Rötungen, Pusteln und allergische/irritative Hauterscheinungen
Autor:innen:
OÄ Priv.-Doz. Dr. Gersina Rega-Kaun
Dr. Alfa Wenkenstetten-Holub
Prim. Univ.-Prof. Dr. Peter Fasching
5. Medizinische Abteilung mit Endokrinologie, Rheumatologie und Akutgeriatrie, Klinik Ottakring, Wien
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Steigende Zahlen der auf der Haut haftenden Diabetesgeräte führen immer öfter zu Hautproblemen. Wie häufig sind diese Komplikationen wirklich? Was sind die Auslöser? Und was können wir tun? Im Folgenden einige Tipps und Tricks.
Keypoints
-
Hautreaktionen bei Trägern von Diabetesdevices sind häufig und können auch nach Monaten erstmalig auftreten.
-
Es gilt, die häufigere irritative (80%) von der allergischen (20%) Kontaktdermatitis zu unterscheiden, da Letztere eine absolute Allergenkarenz bzw. Schutz mittels Barrieren notwendig macht.
-
Beim Management der Hautkomplikationen spielt die Prophylaxe mittels Barriereschutz und Hautpflege eine große Rolle.
Der Einsatz von Insulinpumpen (CSII = „continuous subcutaneous insulin infusion“), CGM („continuous glucose monitoring“)- und FGM(„flash glucose monitoring“)-Systemen hat in den letzten Jahren deutlich zugenommen, weil sie die glykämische Kontrolle und die Lebensqualität von Menschen mit Diabetes verbessern.1 Zudem sind die Geräte kleiner, genauer und kostengünstiger geworden und ihr Einsatz wird in den Leitlinien propagiert.2,3 Jedoch werden diese Devices auf der Haut mittels Pflaster mit einer durchgehenden Tragedauer von 3 bis 14 Tagen fixiert. Die Haut ist wiederholt chemischen und mechanischen Reizen ausgesetzt. Berichte über akute und chronische Hautprobleme nehmen zu.4,5
Hau(p)tprobleme – wie groß ist das Problem wirklich?
In der rezenten multizentrischen Querschnittsstudie (CUTADIAB Study) von Diedisheim et al. wurden über 7 Monate alle Menschen mit Diabetes eingeschlossen, die in den letzten 10 Jahren eine Pumpe (schlauchlos: Omnipod®, Schlauchpumpen: Paradigm®, Animas®, MiniMedTM 640G) oder einen Sensor (FreeStyle Libre®, Dexcom®, Enlite®) getragen hatten (76% mit Diabetes mellitus Typ 1, 15% mit Diabetes mellitus Typ 2, insgesamt n=851, Alter >18 Jahre, Fragenbogen-basiert). Es wurde eine Prävalenz von Hautreaktionen von 28% (CGM) bzw. von 29% (Insulinpumpen) dokumentiert. 12% der CGM-Träger mit Hautreaktionen (3,2% aller Träger) und 7% der CSII-Träger mit Hautreaktionen (2,1% aller Träger) beendeten die Verwendung ihrer Devices.6
Irritativ vs. allergisch: Wie reagiert die Haut?
In der Arbeit von Diedisheim et al. traten die ersten Hautsymptome bei 22% (CGM) bis 24% (CSII) der Patienten schon innerhalb der ersten 24 Stunden, jedoch bei 38% (CGM) bis 47% (CSII) erst nach mehr als 6 Monaten auf. Bei 70–75% der Patienten mit Hautreaktionen wurden Rötungen und Juckreiz, bei 20–25% Schmerzen, bei 12–15% Blasen- und Schuppenbildung beschrieben.6 Durch die Reizstoffe in den Klebstoffen, Plastikkathetern und Gehäusen der Devices kann sich eine Kontaktdermatitis entwickeln. Zu unterscheiden ist hierbei die irritative von der allergischen Kontaktdermatitis.
Die irritative Kontaktdermatitis (Abb. 1)
-
Sehr häufig (80% der Hautreaktionen)
-
Ursache: unspezifische Reaktion mit Freisetzung von Entzündungsmediatoren aus den Epidermalzellen auf chemische Reizstoffe, Okklusion, Schwitzen/Feuchtigkeit unter dem Device oder auf mechanische Reize durch das Entfernen von Pflastern.
-
Symptome: Brennen, intermittierend und unterschiedlich ausgeprägte Rötung, Schuppung, evtl. Juckreiz. Meist tritt die Symptomatik früher als bei der allergischen Kontaktdermatitis auf.7
Die allergische Kontaktdermatitis (Abb. 2)
-
Seltener (20% der Hautreaktionen), nur bei ca. 0,7–0,8% der CGM-tragenden Patienten.8
-
Ursache: auslösendes Allergen, T-Zell- vermittelte Typ-IV-Allergie mit Sensibilisierung und Latenz auch nach Monaten bis Jahren möglich.
-
Die Symptomatik entwickelt sich typischerweise nach längerer Tragedauer: Juckreiz immer und oft sehr stark. Rötung, Schuppung, evtl. Bläschen, Pusteln, Nässen mit Tendenz, sich über die Grenzen des Pflasters auszudehnen. Ohne Allergenstopp sind die Symptome anhaltend.
-
Diagnostik: der Patchtest (=Epikutantest) gilt als Goldstandard, jedoch mit begrenzter Sensitivität (70%).9
Bei der irritativen Dermatitis zeigt sich im Verlauf des Patchtests zunächst eine Reaktion, die jedoch abnimmt, während eine allergische Reaktion am 3. bis 4. Tag zunimmt. Da die Hersteller allerdings nicht verpflichtet sind, die Inhaltsstoffe ihrer Devices anzugeben, kann sich die Suche nach dem auslösenden Allergen schwierig gestalten.10,11,4 Die Differenzialdiagnose der irritativen vs. der allergischen Kontaktdermatitis ist oft nicht leicht, da beide Subtypen auch gleichzeitig bestehen können.
Worauf reagiert die Haut?
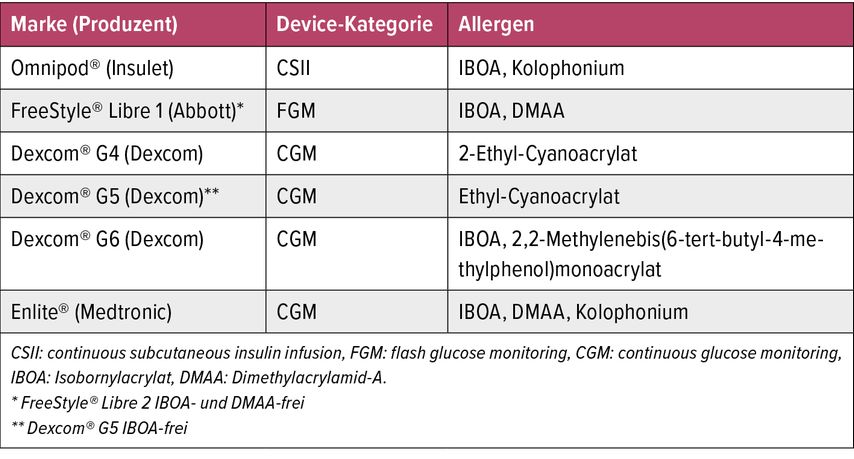
Die häufigsten Allergene in der Diabetestechnologie, auf die reagiert wird, sind Acrylate (Tab.1). Isobornylacrylat (IBOA) konnte 2017 erstmals als Hauptauslöser der Kontaktallergien durch FreeStyle Libre1® (Abbott) identifiziert werden12 und wurde daraufhin 2020 von der American Contact Dermatitis Society zum Kontaktallergen des Jahres auserkoren.10 Die Hersteller reagierten darauf: FreeStyleLibre2® ist IBOA-frei.13 Weitere Stoffe und Devices, die ebenfalls Kontaktdermatitis auslösen, sind in Tabelle 1 aufgelistet.
Tab. 1: Insulinpumpen, Glukosemonitor-Devices und relevante Kontaktallergene (nach Dupuy E et al. 2022 und Cameli N et al. 2022)13, 14
Leitlinien
Trotz zunehmender Problematiken mit Hautkomplikationen, gibt es wenige universell akzeptierte Empfehlungen bezüglich des Managements.
In den Leitlinien der Österreichischen Diabetes Gesellschaft (ÖDG) zu Diabetes mellitus im Kindes- und Jugendalter (Update 2023) sowie in den Leitlinien der International Society for Pediatric and Adolescent Diabetes (ISPAD) 2022 werden bei Follow-up-Untersuchungen routinemäßige Kontrollen der Injektions- bzw. Katheterinsertionsstellen (Cave: Lipohypertrophien/Lipoatrophien und Hautirritationen) und der CGM-Stellen (Ekzeme/Hautirritationen/Abszesse) empfohlen.16,2 Vorbeugend werden eine Rotation der Pumpeninsertions- und der Sensorstellen, eine Vorbereitung und Reinigung der Haut (Klebereste entfernen, evtl. mildes Peeling bei fettiger Haut, Haare trimmen, Haut vollständig trocknen lassen), die Verwendung eines Antitranspirants bei starkem Schwitzen (danach 10–15min abwarten), ein Steroidspray (z.B. „off-label“ zwei Hübe Fluticason-Spray und danach 2min abwarten), eine prophylaktische Hautpflege sowie Schulungen für die selbstständige Inspektion der Haut angeraten.2
Hautkomplikationen durch Pflaster: Management sowie Tipps & Tricks
Die Liste der folgenden Produkte stellt eine Auswahl dar. Diese Auflistung erhebt keinen Anspruch auf Vollständigkeit. Allergische und irritative Veränderungen können ähnlich behandelt werden, jedoch wirken die Maßnahmen oft weniger gut bei allergischen Reaktionen.
Allergische Kontaktdermatitis
Ein neuerlicher Kontakt mit dem Allergen sollte vollständig bzw. möglichst über einen längeren Zeitraum vermieden werden. Topische Kortiskosteroide (dünne Cremefilme bzw. Cortisonspray über sehr kurze Dauer) gelten als therapeutischer Goldstandard, jedoch können bei längerem Gebrauch Nebenwirkungen wie Hautatrophie, Störungen der Hautbarriere oder eine erhöhte Empfindlichkeit gegenüber Reizstoffen zum Tragen kommen. Auch können antihistaminerge bzw. entzündungshemmende Salben verwendet werden.17 Bei ausgedehnter Hautreaktion bzw. bei bakterieller Superinfektion kann eine systemische Kortikosteroid- bzw. eine lokale antibiotische Therapie notwendig werden.18
Irritative Kontaktdermatitis
Die Erstlinientherapie besteht aus physikalischem Schutz der Haut und pflegenden Cremen.19
Hautreaktionen verhindern
Auf Rotation der Applikationsstellen muss geachtet werden. Hände müssen vor Entfernen und Wechsel der Pumpen, Kanülen und Sensoren gründlich gewaschen werden. Zunächst muss die Haut gut vorbereitet werden: Es sollte eine Stelle gewählt werden, die nicht ständig bewegt wird, die Haut soll mit pH-neutraler Seife gewaschen und danach sorgfältig getrocknet werden. Bei CGM-Systemen kann evaluiert werden, ob auf Alkoholdesinfektion verzichtet werden kann (Neigung zu Infektionen geringer, da keine Infusion stattfindet).20 Es sollen keine rückfettenden Desinfektionsmittel verwendet werden (z.B. Braun Softa® Swabs Alkoholtupfer, Embecta BD® Alkoholtupfer) und diese sollten vor Applikation eines Devices unbedingt trocknen. Im „off-label use“ können topische Steroide oder Tracrolimuscreme als Vorbereitung vor Insertion und evtl. nach Abnahme appliziert werden. Auch hier gibt es Bedenken bezüglich Hautveränderungen und Nebenwirkungen bei Langzeitanwendung.21 Wenn möglich sollte auf zusätzliche Fixierung des Devices verzichtet werden.
Als flüssiger Barriereschutz können Allergieblocker auf die Haut aufgetragen werden. Sie dienen als Schutzfilm zwischen Haut und Klebstoff. Eine Schicht ist ausreichend und die Präparate sind bei normaler Körperpflege abwaschbar (z.B. 3MCavilon® reizfreier Hautschutzfilm als Spray mit Abstand von 10–15cm oder Stick 30 Sek. eintrocknen lassen – Cave: potenziell allergen, keine Verwendung bei Allergieanamnese, da Sensibilisierung gefördert werden kann, alkoholfrei, lt. Hersteller soll die Einstichstelle frei von Cavilon® bleiben; Braun Askina® Hautschutzfilm Spray, alkoholfrei und bis 72 Stunden wirksam; Coloplast Brava® Spray, Creme oder Tücher). Der Nutzen der Barrieresprays und -flüssigkeiten scheint jedoch limitiert zu sein.22
Als weiterer fester Barriereschutz können potenziell hypoallergene Hydrokolloid- und/oder Silikon-Pflaster, Folienverbände, Kanülenpflaster oder selbsthaftende Basisplatten zwischen Haut und Device platziert werden, um den direkten Kontakt zu verhindern (z.B. 3M Tegaderm Hydrocolloid THIN® Hydrokolloidverband, Mölnlycke Mepore® Folienverband, Hansaplast® oder Compeed® Blasenpflaster aus Hydrokolloid, Hartmann Cosmopor I.V.® Kanülenfixierverband, Coloplast Brava® Hautschutzplatte). Sie können entweder direkt auf die Haut geklebt, dann von Sensor/Kanüle/Pod durchstochen werden oder vorher an die Unterseite des Gerätes angebracht werden. Messfehler müssen im Anschluss mittels blutiger Messungen ausgeschlossen werden. Leider können Hydrokolloide kolophoniumähnliche Derivate enthalten und sind somit keine Option für kolophoniumsensibilisierte Patienten.23,24,13
Beim Abnehmen des Gerätes ist das Pflaster vorsichtig, evtl. mit Baby-Öl, zu entfernen. Spezielle Klebstoffentferner („Remover“), wie z.B. BSN Leukotape Remover® in Sprayform, Coloplast Pflasterentferner® als Spray und Tücher (auch für Kinder unter2 Jahren geeignet), können für verbleibende Klebstoffreste verwendet werden. Anschließend soll die Haut mit warmem Seifenwasser gereinigt, gut abgespült und eingecremt werden. In dem Bereich sollte mind. eine Woche bzw. bis die Haut sich vollständig erholt hat, kein Device appliziert werden.
Einblutungen verhindern
Die Hautstelle kann 10 Minuten bevor das Device gesetzt wird, mit einem Coolpack gekühlt werden. Bei stärkeren, wiederkehrenden Blutungen kann Emla®-Salbe vor der Applikation aufgetragen werden. Jedoch wurden auch positive Patchtestreaktionen auf Emla®-Salbe beschrieben.25
Meldung von Hautreaktionen
Eine Hautreaktion ist ein unerwünschtes Ereignis von auf der Haut haftenden Diabeteshilfsmitteln und sollte gut dokumentiert werden. Eine Meldung an den medizinischen Anbieter sowie an das Bundesamt für Sicherheit im Gesundheitswesen ( https://www.basg.gv.at/marktbeobachtung/meldewesen/medizinprodukte ) wird empfohlen. Dem Patienten wird geraten, sich an den Kundendienst des Unternehmens zu wenden. Neben den pflasterassoziierten Hautkomplikationen (80%) seien abschließend noch weitere von Diabetesdevices hervorgerufene unerwünschte Nebenwirkungen erwähnt, wie Komplikationen an der Einstichstelle („insertion-related complications“ 20%), Insulinallergien oder Lipodystrophien.26
Zusammenfassung
Praxistipp
Besprechen Sie die Hautpflege routinemäßig vor dem Einsatz von auf der Haut haftenden Diabeteshilfsmitteln und erfragen Sie regelmäßig die Hautverträglichkeit.Hautirritationen und (seltener) Kontaktallergien sind bei Verwendung von Pumpen und Sensoren häufig. Die Kontaktallergie (Typ-IV-Allergie, somit nur nach Sensibilisierung) kann auch erst Monate nach Erstkontakt auftreten, wobei die häufigsten Allergene Acrylate wie Isobornylacrylat (IBOA), N,N-Dimethylacrylamid und Kolophonium sind. Leider gibt es bisher noch keine Pflicht der Gerätehersteller, die Inhaltsstoffe zu deklarieren. Jedoch können dank Prävention durch gute Hautpflege und evtl. Barriereschichten (wie Sprays und Pflastern etc.) die Produkte bei den meisten Hautreaktionen weiter verwendet werden.
Literatur:
1 Hartsough EM, Hylwa SA: Wearable woes: Allergens in diabetic devices. Dermat Contact Atopic Occup Drug 2021; 32(1): 19-31 2 Fröhlich-Reiterer E et al.: ISPAD Clinical Practice Consensus Guidelines 2022: Other complications and associated conditions in children and adolescents with type 1 diabetes. Pediatr Diabetes 2022; 23(8): 1451-67 3 Orr CJ et al.: Long-term efficacy of insulin pump therapy on glycemic control in adults with type 1 diabetes mellitus. Diabetes Technol Ther 2015; 17(1): 49-54 4 Herman A et al.: Allergic contact dermatitis caused by medical devices for diabetes patients: A review. Contact Dermat 2018; 79(6): 331-5 5 Kamann S et al.: Further evidence of severe allergic contact dermatitis from isobornyl acrylate while using a continuous glucose monitoring system. J Diabetes Sci Technol 2018; 12(3): 630-3 6 Diedisheim M et al.: Prevalence and description of the skin reactions associated with adhesives in diabetes technology devices in an adult population: Results of the CUTADIAB study. Diabetes Technol Ther 2023; 25(4): 279-86 7 Aerts O et al.: FreeStyle Libre: Contact irritation versus contact allergy. Lancet 2017; 390(10103): 1644 8 Hyry HSI et al.: Allergic contact dermatitis caused by glucose sensors in type 1 diabetes patients. Contact Dermatitis 2019; 81(3): 161-66 9 Nethercott JR: Practical problems in the use of patch testing in the evaluation of patients with contact dermatitis. Curr Probl Dermatol 1990; 2(4): 97-123 10 Nath N et al.: Isobornyl acrylate and diabetic devices steal the show for the 2020 American Contact Dermatitis Society Allergen of the year. Cutis 2020; 105(6): 283-5 11 Kamann S et al.: Modern diabetes devices for continuous blood sugar measuring: Limitations due to contact allergies. Review J Dtsch Dermatol Ges 2021; 19(12): 1715-21 12 Herman A et al.: Allergic contact dermatitis caused by Isobornyl Acrylate in FreeStyle Libre®, a newly introduced glucose sensor. Contact Dermatitis 2017; 77(6): 367-73 13 Dupuy E et al.: What we have learned-milestones in pediatric contact dermatitis. Review Curr Dermatol Rep 2022; 11(1): 1-12 14 Cameli N et al.: Allergic contact dermatitis, an important skin reaction in diabetes device users: A systematic review. Dermatitis 2022; 33(2): 110-5 15 Herman A et al.: Position statement: The need for EU legislation to require disclosure and labelling of the composition of medical devices. Review J Eur Acad Dermatol Venereol 2021; 35(7): 1444-8 16 Rami-Merhar B et al.: Diabetes mellitus im Kindes- und Jugendalter (Update 2023). Wien Klin Wochenschr 2023; 135(1): 106-14 17 Li Y, Li L: Contact dermatitis: Classifications and management. Clin Rev Allergy Immunol 2021; 61(3): 245-81 18 Bonamonte D et al.: Noneczematous contact dermatitis. ISRN Allergy 2013; 2013: 361746 19 Johnston GA et al.: British Association of Dermatologists’ Guidelines for the management of contact dermatitis 2017. Br J Dermatol 2017; 176: 317-29 20 Messer LH: Skin integrity, tips, tricks and hacks for sustained device use (ID 226); presented at ATTD 2023; Abstract No. IS029 21 Paret M et al.: „Out of the box“ solution for skin problems due to glucose-monitoring technology in youth with type 1 diabetes: Real-life experience with fluticasone spray. Observational Study Acta Diabetol 2020; 57(4): 419-24 22 Pyl J et al.: Prevalence and prevention of contact dermatitis caused by FreeStyle Libre: A monocentric experience. Diabetes Care 2020; 43(4): 918-20 23 Kamann S et al.: Usage of hydrocolloid-based plasters in patients who have developed allergic contact dermatitis to Isobornyl Acrylate while using continuous glucose monitoring systems. J Diabetes Sci Technol 2020; 14(3): 582-5 24 Kamann S, Oppel E: Hydrocolloid blister plaster decreases allergic contact dermatitis caused by FreeStyle Libre and isobornylacrylate. Contact Dermat 2019; 81(5): 380-1 25 da Silva CA et al.: Contact dermatitis in children caused by diabetes devices. Contact Dermat 2022; 87(5): 406-13 26 Asarini NAM et al.: Cutaneous complications with continuous or flash glucose monitoring use: Systematic review of trials and observational studies. J Diabetes Sci Technol 2020; 14(2): 328-37
Das könnte Sie auch interessieren:
Diabetes erhöht das Sturzrisiko deutlich
Eine dänische Studie kommt zu dem Ergebnis, dass sowohl Patienten mit Typ-1- als auch Patienten mit Typ-2-Diabetes öfter stürzen und häufiger Frakturen erleiden als Menschen aus einer ...
Neue Studiendaten zu Typ-2-Diabetes und Lebensstil
Dass gesunde Ernährung und Bewegung das Diabetesrisiko sowie verschiedene Risiken von Patienten mit Diabetes senken, ist seit Langem bekannt. Und das Detailwissen zur Bedeutung von ...
Wie oft wird Diabetes nicht oder spät erkannt?
Im Allgemeinen wird von einer hohen Dunkelziffer an Personen mit undiagnostiziertem Typ-2-Diabetes ausgegangen. Ein Teil davon sind von Ärzten „übersehene“ Fälle. Eine von der University ...
.jpg)
.jpg)