Bewährte und neue medikamentöse Optionen zur Cholesterinsenkung
Autoren:
Cand. med. Leonard Kozarzewski
Priv.-Doz. Dr. med. Thomas Bobbert
Charité – Universitätsmedizin Berlin,
corporate member Freie Universität Berlin und Humboldt-Universität zu Berlin,
Klinik für Endokrinologie und Stoffwechselmedizin, Berlin
E-Mail: leonard.kozarzewski@charite.de
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die medikamentöse Cholesterinsenkung zur kardiovaskulären Prävention bestand lange Zeit nur im Einsatz von Statinen und Ezetimib und eventuell Gallensäurebindern. Die Zulassung der Proproteinkonvertase-Subtilisin/Kexin-Typ-9-Inhibitoren (PCSK9-Inhibitoren) Evolocumab und Alirocumab in der EU im Jahr 2015 hat einen weiteren Durchbruch gebracht. Jetzt sind erneut neue effektive Medikamente verfügbar und Erfolg versprechende Therapieansätze in Aussicht.
Keypoints
-
Bempedoinsäure und Inclisiran ergänzen die Optionen zur Therapie der Hypercholesterinämie und füllen bisher nicht besetzte Lücken in der kardiovaskulären Prävention – insbesondere bei Unverträglichkeit von Statinen und PCSK9-AK.
-
Eine deutliche medikamentöse Senkung von Lipoprotein(a) ist möglich und zukünftig eventuell eine Alternative zur Lipoproteinapherese bei Hyperlipoproteinämie (a).
-
Viele der in Entwicklung befindlichen Präparate regulieren die Translation der mRNA. Antisense-Oligonukleotide und „small interfering RNA“ werden in Zukunft weiter an Bedeutung gewinnen.
Risikofaktor LDL-Cholesterin und Entwicklung der Zielwerte
Es ist heute unumstritten, dass die Konzentration des Low-Density-Lipoproteins (LDL) im Blut einen zentralen und kausalen Faktor in der Entwicklung der Arteriosklerose darstellt. Die Auswirkung des LDL-Cholesterins (LDL-C) auf das kardiovaskuläre Risiko scheint dabei sowohl von der Höhe als auch von der Gesamtdauer der Exposition abzuhängen.1 Entsprechend werden die Zielwerte für die primäre und sekundäre Prävention von kardiovaskulären Erkrankungen seit Jahren nach unten korrigiert. So gilt nach den Leitlinien der European Society of Cardiology (ESC) und der European Atherosclerosis Society (EAS) aus dem Jahr 2019 erstmals ein LDL-C-Zielwert von unter 55mg/dl für Patienten mit sehr hohem kardiovaskulärem Risiko bzw. nach kardiovaskulärem Ereignis.2 Sollte es unter Einhaltung dieses Zielwertes innerhalb von zwei Jahren nach einem kardiovaskulären Ereignis zu einem erneuten Ereignis kommen, kann gar ein Zielwert von unter 40mg/dl in Betracht gezogen werden. Es gibt bisher keine starken Hinweise darauf, dass ein unterer Grenzwert in der medikamentösen Senkung des LDL-C existiert.3
Lebensstiloptimierung als Basis der Cholesterinsenkung
Die Optimierung des Lebensstils stellt die Grundlage der cholesterinsenkenden Behandlung dar. Die Reduktion von gesättigten und Trans-Fettsäuren in der Nahrung kann zu einer LDL-C-Senkung um bis zu 20% führen.4 Zudem können eine Gewichtsreduktion und sportliche Aktivität einen positiven Effekt auf die LDL-C-Konzentration bzw. die LDL-C-Partikelgröße haben.
Medikamentöse Therapie zur LDL-Cholesterinsenkung
Statine: bewährt und sicher, aber nicht immer verträglich
In der medikamentösen Therapie sind Statine Mittel der ersten Wahl. Statine hemmen die 3-Hydroxy-3-Methylglutaryl-Coenzym-A-Reduktase (HMG-CoA-Reduktase), welche das geschwindigkeitsbestimmende Enzym in der Cholesterinbiosynthese ist. Eine hoch dosierte Statintherapie kann das LDL-C um bis zu 50% reduzieren. In Kombination mit Ezetimib, welches die Aufnahme von Cholesterin im Darm hemmt, liegt die LDL-C-Reduktion bei bis zu 65%. Sowohl für die Mono- als auch für die Kombinationstherapie sind kardioprotektive Effekte gezeigt worden. In der klinischen Praxis werden die geltenden Zielwerte trotz Lebensstilmodifikation und Einsatz der bisher gängigen oralen Therapeutika nicht regelmäßig erreicht. Es existieren große interindividuelle Unterschiede im Ansprechen auf die Statintherapie, was möglicherweise auf genetische Variationen zurückgeführt werden kann.5
Zudem stellen die von bis zu 15% der Patienten beklagten Statin-assoziierten muskulären Symptome (SAMS) einen limitierenden Faktor für die Therapie dar. SAMS sind klinisch heterogen. Meist werden symmetrische Schmerzen und Verspannungen der proximalen Muskulatur beklagt. Die Kreatinkinase (CK) ist häufig nicht oder nur leicht erhöht. Schwere Muskelschäden im Sinne einer Rhabdomyolyse, die mit einer Freisetzung von Myoglobin und einer CK-Erhöhung über das Zehnfache der oberen Grenze des Normalbereichs einhergehen, sind mit einer Inzidenz von 1 pro 100000 Patienten sehr selten.6 Interessanterweise werden SAMS in klinischen Studien deutlich weniger häufig beschrieben, als in „Real-World-Studien“. Dies liegt natürlich zum einen an der Selektion der Studienteilnehmer, zum anderen aber auch an vielen weiteren Effekten, wie z.B. dem Nocebo-Effekt.7 Bei Auftreten von SAMS ohne stark erhöhte CK sollten zunächst weitere Statine ausprobiert werden.
Fibrate: bei kombinierter Hypercholesterinämie/Hypertriglyzeridämie
Als Agonisten der Peroxisom-Proliferator-aktivierten Rezeptoren vom Typ a (PPAR-a) haben Fibrate Einfluss auf verschiedene Schritte im Lipidstoffwechsel. Sie werden vor allem im Bereich der Hypertriglyzeridämie eingesetzt, weisen jedoch auch einen LDL-C-senkenden Effekt von bis zu 20% auf. Der kardioprotektive Effekt von Fibraten ist nicht eindeutig geklärt und scheint vor allem bei Patienten mit hohen Triglyzeridwerten zu bestehen,8 weswegen ihr Stellenwert in der kardiovaskulären Prävention auf diese Patientengruppe begrenzt ist.
Gallensäurebinder: begrenzter Effekt durch Dosislimitation
Auch für die Gallensäurenbinder wurde ein bis zu 20%iger LDL-C-senkender Effekt gefunden. Sie verhindern die Wiederaufnahme von aus Cholesterin synthetisierten Gallensäuren im Darm im Rahmen des enterohepatischen Kreislaufs. Kardioprotektive Effekte korrelieren mit der Cholesterinsenkung.9 In der klinischen Praxis führt die für eine signifikante LDL-C-Senkung benötigte Dosis jedoch in den meisten Fällen zu erheblichen gastrointestinalen Nebenwirkungen wie Flatulenz, Obstipation und Übelkeit.
PCSK9-Inhibitoren: bei Nichterreichen der LDL-C-Ziele trotz oraler Medikation
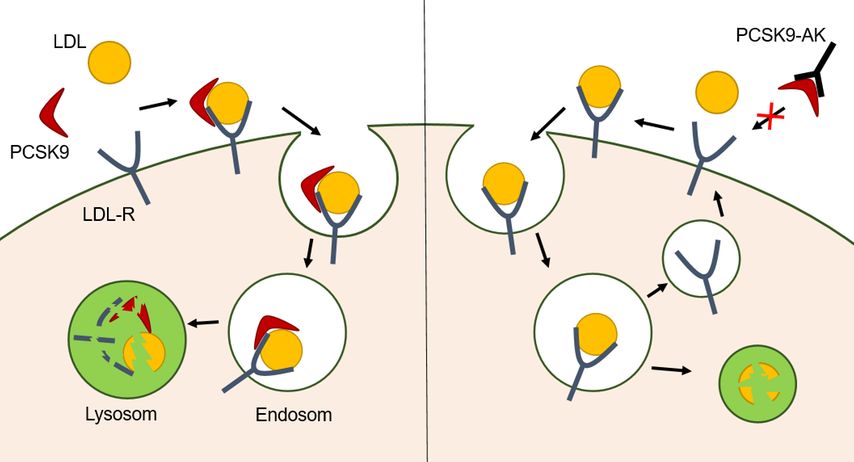
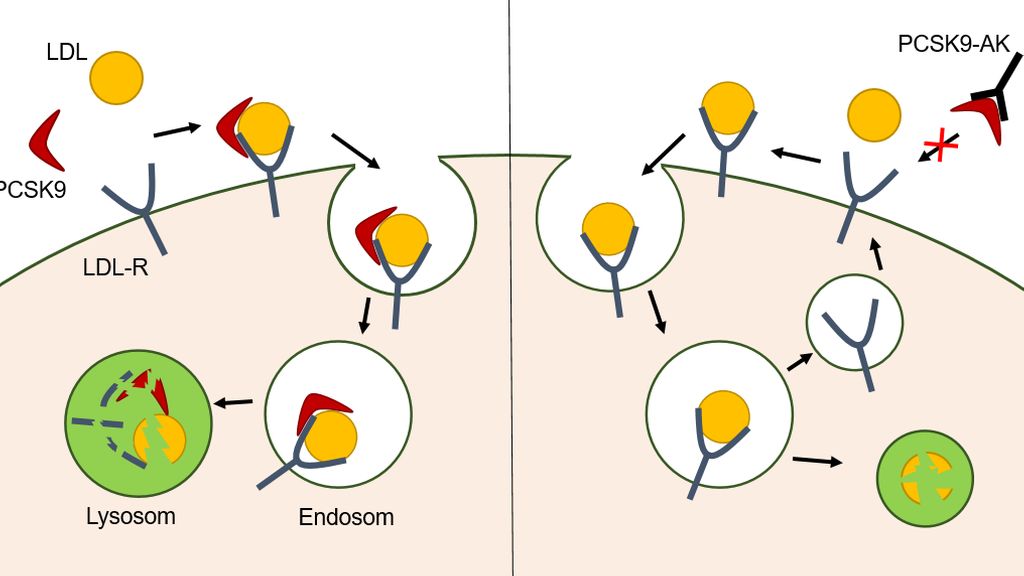
Insbesondere Patienten mit sehr hohem kardiovaskulärem Risiko, deren Cholesterinwerte trotz maximal verträglicher oraler Medikation nicht im Zielbereich liegen, haben von der Einführung der monoklonalen Anti-PCSK9-Antikörper (PCSK9-AK) Evolocumab und Alirocumab profitiert. PCSK9 vermittelt den lysosomalen Abbau des LDL-Rezeptors (LDL-R) und trägt so zu einer erhöhten LDL-C-Konzentration bei, PCSK9-Inhibitoren inhibieren diesen Abbau (Abb. 1). Die Wirkung beider Präparate scheint vergleichbar zu sein. Der durchschnittliche LDL-C senkende Effekt liegt bei Monotherapie mit PCSK9-AK bei 60% und in Kombination mit Statin und Ezetimib bei 85%. Bisherige Studien zeigten eine relative Reduktion der kardiovaskulären Endpunkte (kardiovaskulärer Tod, Herzinfarkt, Schlaganfall, Hospitalisierung mit unstabiler Angina pectoris, koronare Revaskularisation) um ca. 15%.10,11 Die Applikation erfolgt subkutan alle zwei bis vier Wochen. Nebenwirkungen sind relativ selten. Als häufigste Nebenwirkung beklagen die Patienten grippeähnliche Symptomatik und lokale Entzündungsreaktionen an der Einstichstelle.
Abb. 1: LDL-Rezeptor-Prozessierung in Gegenwart von PCSK9 und bei PCSK9-Inhibierung: Die Proproteinkonvertase Subtilisin/Kexin Typ 9 (PCSK9) bindet den Low-Density-Lipoprotein-Rezeptor (LDL-R) an der Leberzelle und vermittelt den lysosomalen Abbau des Komplexes aus PCSK9, LDL-Rezeptor und LDL. Wenn PCSK9 von Anti-PCSK9-Antikörpern (PCSK9-AK) gebunden wird, wird der lysosomale Abbau des LDL-Rezeptors inhibiert. Es wird mehr LDL-R recycelt. Dies führt zu einer erhöhten LDL-Aufnahme aus dem Blut in die Zelle.
Inclisiran: geringere Frequenz der Applikation als bei PCSK9-Inhibitoren nötig
Ende 2020 hat Inclisiran, das ebenfalls PCSK9 als Angriffspunkt verwendet (Abb. 2 unten), die Zulassung in Europa erhalten. Bei Inclisiran handelt es sich um eine kleine interferierende Ribonukleinsäure („small interfering ribonucleic acid“, siRNA). Die siRNA ist ein kleines doppelsträngiges RNA-Stück, das den katalytischen Abbau der mRNA für PCSK9 bewirkt. Um die Aufnahme in die Hepatozyten zu erleichtern, ist die RNA mit triantennärem N-Acetylgalactosamin (GalNAc) konjugiert. Die LDL-C-Reduktion liegt bei ca. 50%.12 Relevante Nebenwirkungen wurden bisher nicht verzeichnet. Ein wesentlicher Unterschied zu Evolocumab und Alirocumab ist die Frequenz der Applikation: Inclisiran wird nach der initialen Gabe einmalig nach 3 Monaten, dann nur alle sechs Monate subkutan injiziert. Damit könnte es einen hohen Stellenwert bei Einschränkung der selbstständigen Applikation oder Unverträglichkeit der PCSK9-AK einnehmen. Der Effekt auf kardiovaskuläre Endpunkte wird aktuell im Rahmen der ORION-4-Studie noch untersucht.
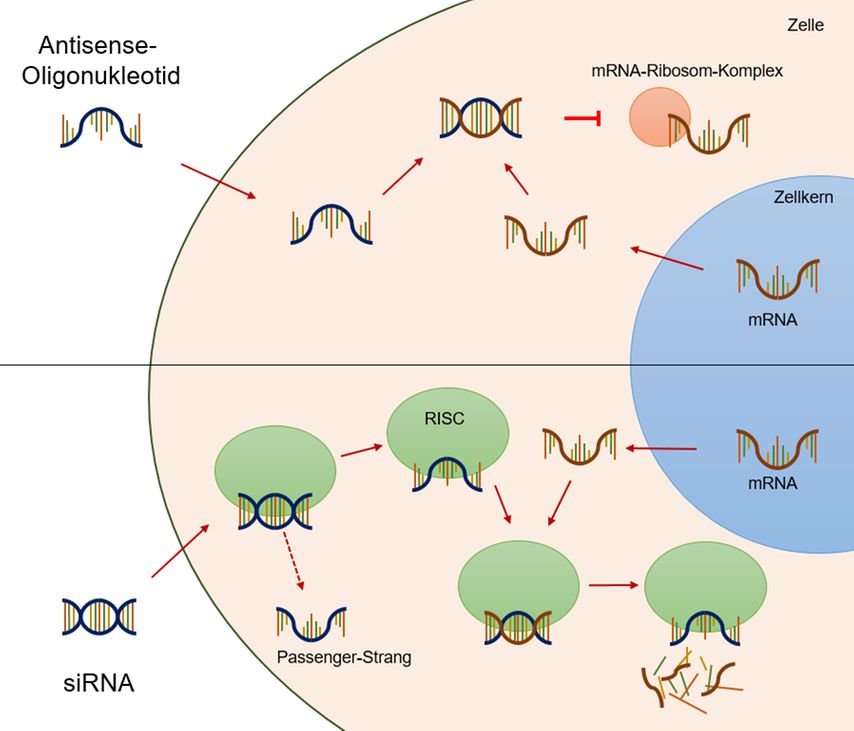
Abb. 2: Funktionsprinzip der Antisense-Oligonukleotid- und der siRNA-Präparate: Ein Antisense-Oligonukleotid (z.B. Mipomersen, Pelacarsen) ist eine kurzkettige synthetische Nukleinsäure. Nach Aufnahme in die Zelle bindet es über komplementäre Basenpaarung an eine Nukleinsäure, deren Basenabfolge dazu exakt passt (Sense-Nukleinsäure). Durch die spezifische Bindung an eine Messenger-RNA (mRNA) wird die Translation des Zielgens inhibiert. Bei der „small interfering RNA“ (siRNA, z.B. Inclisiran) handelt es sich um kurze doppelsträngige Ribonukleinsäure-Moleküle. Nach Eintritt in die Zelle bildet ein Strang der siRNA mit speziellen Proteinkomponenten den „RNA-induced silencing complex“ (RISC), der andere (Passenger-)Strang wird nicht benötigt. Die zur siRNA komplementäre mRNA wird vom RISC zerstört.
Bempedoinsäure: zwischen Statin/Ezetimib und PCSK9-Inhibitoren
Mit der Bempedoinsäure ist seit letztem Jahr eine weitere orale Medikation verfügbar. Bempedoinsäure ist ein Prodrug, dessen aktiver Metabolit wie die Statine in die Cholesterinbiosynthese eingreift. Angriffspunkt ist das Enzym Adenosintriphosphat-Citrat-Lyase (ACL), welches der HMG-CoA-Reduktase im Cholesterinstoffwechsel vorgelagert ist. Bei Monotherapie wird eine ca. 25%ige Reduktion des LDL-C erreicht. Bei bestehender Statintherapie wird eine zusätzliche LDL-Senkung um ca. 16% erreicht. Die Kombination von Bempedoinsäure und Ezetimib erbringt bei bestehender Statintherapie eine LDL-C-Senkung um ca. 29%.13 Das zur Aktivierung der Bempedoinsäure benötigte Enzym ist hauptsächlich in der Leber und nicht im Muskel vorhanden, daher sind muskuläre Nebenwirkungen im Vergleich zu Statinen seltener. Häufige Nebenwirkungen umfassen Hyperurikämie und Anämie. Insgesamt besteht eine gute Verträglichkeit. Mit einer moderaten LDL-C-Senkung kann die Bempedoinsäure so eine Lücke im therapeutischen Algorithmus zwischen der Statin- und Ezetimib-Therapie und der PCSK9-Inhibitor-Therapie füllen. Kardiovaskuläre Endpunkte werden aktuell in der CLEAR-Outcomes-Studie untersucht.
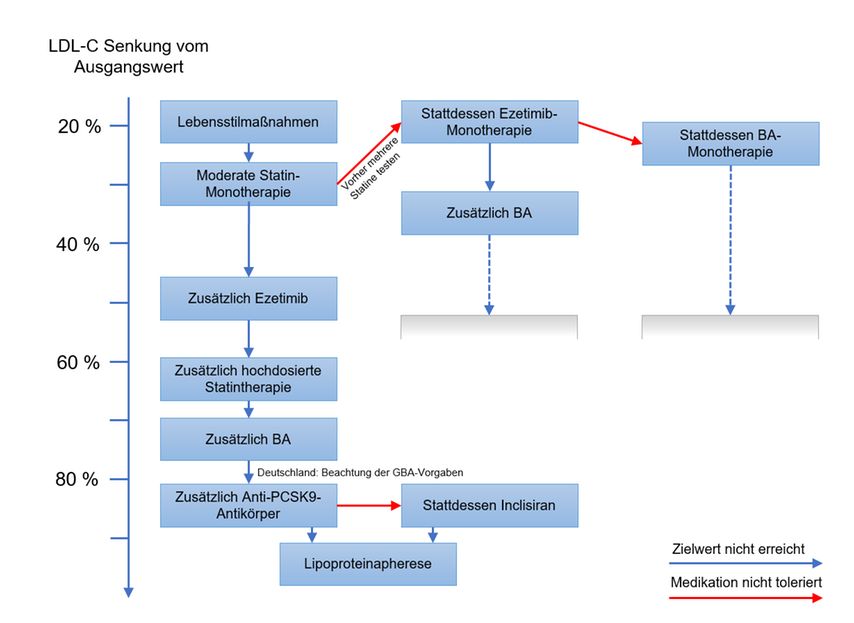
Ein möglicher medikamentöser Algorithmus der Cholesterinsenkung mit den genannten Präparaten und die erreichbaren LDL-C-Reduktionen sind in der Abbildung 3 dargestellt.
Abb. 3: Möglicher medikamentöser Algorithmus der Cholesterinsenkung: Dargestellt sind die therapeutischen Schritte der Cholesterinsenkung in der kardiovaskulären Prävention und die durchschnittliche LDL-C-Senkung der Präparate bzw. der Kombinationen. Der Algorithmus in Spalte 2 und 3 entspricht der in Spalte 1 und ist daher nicht komplett dargestellt. BA: Bempedoinsäure
Ausblick auf künftige Therapieoptionen
Evinacumab: FDA-Zulassung bei homozygoter familiärer Hypercholesterinämie
Zukünftig könnte insbesondere für Patienten mit homozygoter familiärer Hypercholesterinämie (hoHF) das Ausschalten des Angiopoietin-like-3-Gens (ANGPTL3) einen Durchbruch bedeuten. ANGPTL3 vermittelt u.a. über eine Aktivierung der Lipolyse in Fettgewebe und Muskeln einen Anstieg von Triglzycerid-reichen Lipoproteinen, hat jedoch auch Effekte auf den Cholesterinstoffwechsel. Evinacumab, ein monoklonaler Antikörper, senkte bei Patienten mit hoHF das LDL-C um ca. 50%14 und zeigt sich bisher nebenwirkungsarm. In den USA hat es im April 2021 die Zulassung erhalten.
Pelacarsen: Daten zur Lp(a)-Reduktion vielversprechend
Neben dem LDL-C rückt das Lipoprotein(a) [Lp(a)] als Ziel einer gerichteten Therapie zunehmend in den Vordergrund. Es handelt sich um ein LDL-Partikel, dessen Proteinbestandteil Apolipoprotein(a) [Apo(a)] beinhaltet. Als Risikofaktor für Arteriosklerose ist es schon seit vielen Jahren bekannt, und bis jetzt gilt die Lipoproteinapherese als einzige Möglichkeit zur effektiven Elimination. Diese Therapie ist in der Regel aber Patienten vorbehalten, bei denen es zu einem Progress einer kardiovaskulären Erkrankung unter maximaler Therapie aller anderen Risikofaktoren kommt. Während Statine den Lp(a)-Wert eventuell sogar erhöhen können, bewirken die PCSK9-AK eine Absenkung um ca. 20%, die klinisch relevant sein könnte.15 Allerdings sind die PCSK9-AK nicht zur Therapie einer Hyperlipoproteinämie (a) zugelassen.
Mit Pelacarsen, einem Antisense-Oligonukleotid (ASO), ist eine vielversprechende Substanz aktuell in einer Phase III-Studie. Pelacarsen bindet die LPA-Gen-mRNA und verhindert die Translation von Apo(a) (Abb. 2 oben). Erste Daten zeigen eine Lp(a)-Reduktion von bis zu 80%.16 Der Abschluss der HORIZON-Studie, in der kardiovaskuläre Endpunkte untersucht werden, ist für 2024 geplant. Sollten sich diese ersten Daten bestätigen, bestünde erstmalig die Option einer medikamentösen Therapie der Hyperlipoproteinämie (a). Pelacarsen könnte eine Alternative zur Lipoproteinapherese darstellen, die u.a. zu einer bedeutenden Verbesserung der Lebensqualität der Patienten führen würde.
Fazit
Zusammenfassend lässt sich feststellen, dass nach der Lebensstilmodifikation Statine weiterhin Mittel der ersten Wahl zur Therapie der Hypercholesterinämie sind. Nebenwirkungen unter Statinen sind selten, und vor der Diagnose einer Statinintoleranz sollten wenn möglich mehrere Statine ausprobiert werden. Der Einsatz von Ezetimib und PCSK9-AK stellt eine etablierte additive Therapie bzw. Alternative dar. Mit Inclisiran und Bempedoinsäure sind nun weitere Optionen zur Therapie der Hypercholesterinämie verfügbar. Endpunktstudien zu beiden Präparaten werden in den nächsten Jahren erwartet. Sie ersetzen keines der bisher gängigen Präparate, besetzen jedoch therapeutische Lücken.
Literatur:
1 Ference BA et al.: Low-density lipoproteins cause atherosclerotic cardiovascular disease. 1. Evidence from genetic, epidemiologic, and clinical studies. A consensus statement from the European Atherosclerosis Society Consensus Panel. Eur Heart J 2017; 38(32): 2459-72 2 Mach F et al.: 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J 2020; 41(1): 111-88 3 Olsson AG et al.: Can LDL cholesterol be too low? Possible risks of extremely low levels. J Intern Med 2017; 281(6): 534-53 4 Bruckert E et al.: Lowering LDL-cholesterol through diet: potential role in the statin era. Curr Opin Lipidol 2011; 22(1): 43-8 5 Chasman DI et al.: Genetic determinants of statin-induced low-density lipoprotein cholesterol reduction: the Justification for the Use of Statins in Prevention: an Intervention Trial Evaluating Rosuvastatin (JUPITER) trial. Circ Cardiovasc Genet 2012; 5(2): 257-64 6 Law M et al.: Statin safety: a systematic review. Am J Cardiol 2006; 97(8A): 52C-60C 7 Gupta A et al.: Adverse events associated with unblinded, but not with blinded, statin therapy in the Anglo-Scandinavian Cardiac Outcomes Trial-Lipid-Lowering Arm (ASCOT-LLA): a randomised double-blind placebo-controlled trial and its non-randomised non-blind extension phase. Lancet 2017; 389(10088): 2473-81 8 Bruckert E et al.: Fibrates effect on cardiovascular risk is greater in patients with high triglyceride levels or atherogenic dyslipidemia profile: a systematic review and meta-analysis. J Cardiovasc Pharmacol 2011; 57(2): 267-72 9 The Lipid Research Clinics Coronary Primary Prevention Trial. Results of 6 years of post-trial follow-up. The Lipid Research Clinics Investigators. Arch Intern Med 1992; 152(7): 1399-410 10 Sabatine MS et al.: Open-Label Study of Long-Term Evaluation against LDL Cholesterol (OSLER) Investigators. Efficacy and safety of evolocumab in reducing lipids and cardiovascular events. N Engl J Med 2015; 372(16): 1500-9 11 Schwartz GG et al.: Alirocumab and cardiovascular outcomes after acute coronary syndrome. N Engl J Med 2018; 379(22): 2097-107 12 Ray KK et al.: Inclisiran in patients at high cardiovascular risk with elevated LDL cholesterol. N Engl J Med 2017; 376(15): 1430-40 13 Niman S et al.: A review of the efficacy and tolerability of bempedoic acid in the treatment of hypercholesterolemia. Am J Cardiovasc Drugs 2020; 20(6): 535-48 14 Doggrell SA.: Will evinacumab become the standard treatment for homozygous familial hypercholesterolemia? Expert Opin Biol Ther, 2021; 21(3): 299-302 15 O‘Donoghue ML et al.: Lipoprotein(a), PCSK9 inhibition, and cardiovascular risk. Circulation 2019; 139(12): 1483-92 16 Tsimikas S et al.: Lipoprotein(a) reduction in persons with cardiovascular disease. N Engl J Med 2020; 382(3): 244-55
Das könnte Sie auch interessieren:
Diabetes erhöht das Sturzrisiko deutlich
Eine dänische Studie kommt zu dem Ergebnis, dass sowohl Patienten mit Typ-1- als auch Patienten mit Typ-2-Diabetes öfter stürzen und häufiger Frakturen erleiden als Menschen aus einer ...
Neue Studiendaten zu Typ-2-Diabetes und Lebensstil
Dass gesunde Ernährung und Bewegung das Diabetesrisiko sowie verschiedene Risiken von Patienten mit Diabetes senken, ist seit Langem bekannt. Und das Detailwissen zur Bedeutung von ...
Wie oft wird Diabetes nicht oder spät erkannt?
Im Allgemeinen wird von einer hohen Dunkelziffer an Personen mit undiagnostiziertem Typ-2-Diabetes ausgegangen. Ein Teil davon sind von Ärzten „übersehene“ Fälle. Eine von der University ...