Ist Pelargonium sidoides eine Therapieoption bei Kindern mit Hand-Fuss-Mund-Krankheit?
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Eine Studie hat den Pelargonium-sidoides-Wurzelextrakt EPs®7630 erstmals bei Kindern mit Hand-Fuss-Mund-Krankheit untersucht und eine signifikante Reduktion des Beschwerdegrads und der Krankheitsdauer bei den behandelten Kindern nachgewiesen.1
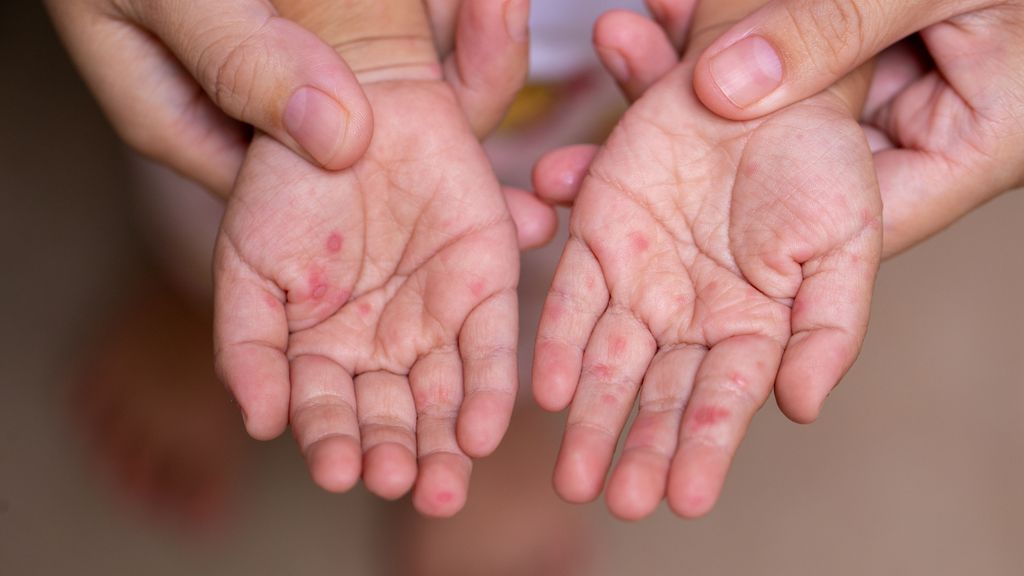
Die Hand-Fuss-Mund-Krankheit (HFMD) ist eine weit verbreitete, ansteckende virale Infektionskrankheit bei Kindern, die durch humane Enteroviren und Coxsackie-Viren verursacht wird. Es gibt keine spezifische Behandlungsmöglichkeit für HFMD. Die antiviralen, antibakteriellen und immunmodulatorischen Eigenschaften des Wurzelextrakts aus Pelargonium sidoides EPs®7630 wurden bereits in mehreren In-vitro- und In-vivo-Studien nachgewiesen,2,3 ebenso wie seine Wirksamkeit bei respiratorischen Infekten.4–8 EPs®7630 hat sich vor allem gegen behüllte Viren als wirksam erwiesen, darunter RSV, Parainfluenza-Virus, Influenza-A-Virus (H1N1, H3N2) und das humane Coronavirus (HCoV-229E). Es wurde aber auch nachgewiesen, dass EPs®7630 das nicht umhüllte Coxsackie-Virus hemmt.7 Die Anwendung dieses pflanzlichen Arzneimittels wurde jedoch noch nicht bei Kindern mit HFMD untersucht.
EPs®7630 bei Kindern mit HFMD
Sütçü et al. führten deshalb eine prospektive randomisierte multizentrische klinische Studie mit 208 Kindern mit HFMD durch. Die Diagnose wurde von Kinderärzten gestellt und die Kinder wurden innerhalb der ersten 48 Stunden nach Auftreten der Symptome (erstes Auftreten von Fieber und Hautsymptomen) in die Studie aufgenommen. Sie wurden in zwei Gruppen eingeteilt: eine EPs®-7630-Gruppe mit 94 Kindern und eine Kontrollgruppe mit 96 Kindern. Das Durchschnittsalter betrug 27 Monate (12–112), das Verhältnis von Buben zu Mädchen 0,98. Alle Kinder wurden vor Beginn der Behandlung beurteilt und zweimal nachuntersucht, 48 Stunden nach der ersten Aufnahme und am 5. bis 7. Tag.
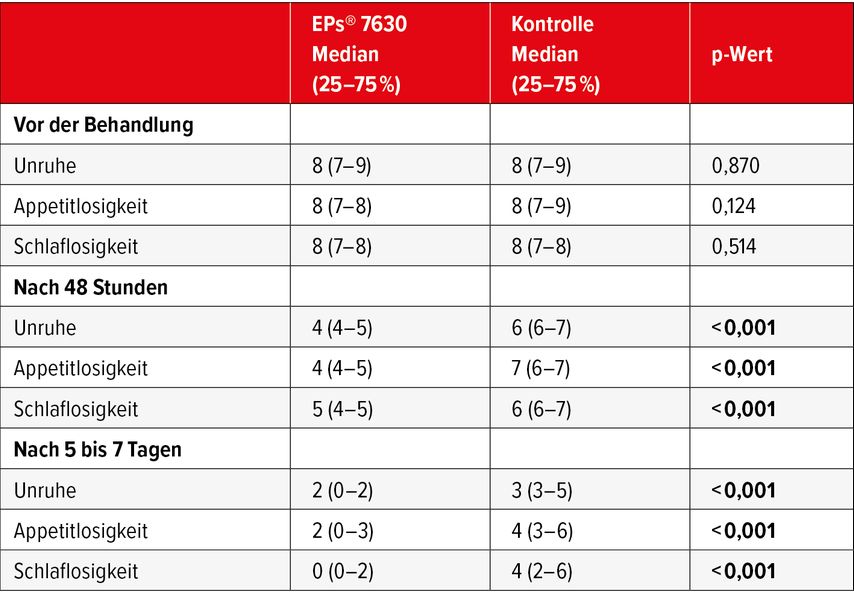
Anlässlich der beiden Nachuntersuchungen war der Beschwerdegrad bei den Kindern, die EPs®7630 erhielten, signifikant niedriger als in der Kontrollgruppe (p<0,001; Tab.1). Die mittlere Krankheitsdauer (± SD) war in der EPs®-7630-Gruppe mit 6,07 ± 0,70 Tagen (95% CI: 5,92–6,21) signifikant kürzer als in der Kontrollgruppe (8,58 ± 0,94 Tage; 95% CI: 8,39–8,77; p<0,001). Ausserdem war die Hospitalisierungsrate bei den Kindern mit EPs®7630 signifikant niedriger (p=0,019). Es wurden keine Nebenwirkungen beobachtet, mit Ausnahme eines unangenehmen Geschmacks, der von 5 Kindern in der EPs®-7630-Gruppe berichtet wurde.
Tab. 1: Beschwerdegrad, beurteilt durch die Eltern auf einer Skala von 0 bis 10, vor der Behandlung und 48 Stunden sowie 5 bis 7 Tage nach Behandlungsbeginn1
Fazit
Die Studie zeigt, dass die Anwendung von EPs®7630 innerhalb von 48 Stunden nach Symptombeginn den Beschwerdegrad bei Kindern mit HFMD signifikant reduziert und gut vertragen wird. Angesichts seines Wirksamkeits- und Sicherheitsprofils sehen die Autoren EPs®7630 als eine praktikable pflanzliche Behandlungsoption für Kinder mit HFMD. Sie stellen aber auch fest, dass weitere Forschungsarbeiten erforderlich sind, um die Wirksamkeit von EPs7630 im Vergleich zu herkömmlichen Therapieansätzen zu bewerten und seine antivirale Wirkung gegen Enteroviren zu untersuchen. (red)
Literatur:
1 Sütçü M et al.: Hand, foot, and mouth disease: could EPs® 7630 be a treatment option? A prospective randomized open-label multicenter clinical study. Front Pediatr 2024; 12: 1274010 2 Timmer A et al.: Cochrane Database Syst Rev 2013; 22: CD006323 3 Matthys H et al.: J Lung Pulm Respir Res 2016; 3: 4-15 4 Careddu D, Pettenazzo A: Int J Gen Med 2018; 11: 91-8 5 Kolodziej H, Kiderlen AF: Phytomedicine 2007: 6: 18-26 6 Thäle C et al.: Planta Med 2017; 77: 718-25 7 Michaelis M et al.: Phytomedicine 2011; 18: 384-6 8 Theisen LL, Muller CP: Antiviral Res 2012; 94: 147-56
Das könnte Sie auch interessieren:
«Planetary Health» – Interaktion von Gesundheit und Klimawandel
Der Klimawandel ist längst bei uns angekommen – in der Schweiz waren die letzten zehn Jahre 2,5°C wärmer als der vorindustrielle Durchschnitt und die Temperaturen steigen weiter an. Dies ...
Nachhaltigkeit im Spital am Beispiel der Radiologie
Betrachtet man das weltweite Gesundheitssystem als Land, liegt es in der globalen Rangliste der Länder mit den höchsten CO2-Emissionen nach China, den USA, Indien und Russland auf Platz 5.1 Innerhalb eines Spitals gehört die Radiologie zu den ...
Geriatrie-Assessment in der Praxis
Im Praxisalltag kann es für Hausärzt:innen mitunter schwierig sein, abzuschätzen, wie gut ihre älteren Patient:innen im Alltag noch funktionieren. Oft gibt erst die Fahreignungsprüfung ...