L’intelligence artificielle en gastroentérologie et hépatologie
Auteur:
Pr Dr méd. Peter Fickert
Klinische Abteilung für Gastroenterologie und Hepatologie
Medizinische Universität Graz
E-mail: peter.fickert@medunigraz.at
La médecine numérique et le nombre croissant de possibilités d’application de dispositifs médicaux assistés par IA (intelligence artificielle) dans le diagnostic et le traitement des maladies gastro-intestinales créent de nombreuses nouvelles possibilités d’amélioration des traitements. En parallèle, de grands défis doivent être relevés. Nous avons besoin d’un large débat de société sur la manière dont nous envisageons cette nouvelle médecine et comment nous voulons la façonner.
Keypoints
-
L’intelligence artificielle (IA) est LE «game-changer» en gastroentérologie.
-
Après une introduction clinique à grande échelle, l’endoscopie du tractus gastro-intestinal sera différente et nouvelle.
-
Les résultats du «deep learning» auront une influence directe sur la quasi-totalité des domaines du diagnostic et du traitement des maladies gastro-intestinales.
-
Notre rôle de médecins dans la prise de décision concernant le diagnostic et le traitement des maladies gastro-intestinales doit être redéfini.
-
Nous devons lancer dès maintenant une réforme de la formation.
La dynamique et les progrès en terme de qualité de toutes les solutions numériques dans le domaine de la gastroentérologie et de l’hépatologie sont époustouflants. Depuis 2020, on dénombre plus de 3000 publications sur le thème de l’intelligence artificielle (IA) en gastroentérologie. En 2019, le symposium international de haut niveau «First Global Artificial Intelligence in Gastroenterology and Endoscopy Summit» avait déjà identifié à l’époque les possibilités d’application actuelles (et non futures!) de l’IA dans de nombreux domaines de la gastroentérologie et de l’hépatologie. Étaient déjà considérées comme actuelles en 2019: la détection de polypes, la prédiction du caractère invasif de tumeurs dans le tractus gastro-intestinal, la classification/caractérisation de lésions précancéreuses, l’évaluation par endoscopie par capsule, les solutions d’assistance en échographie, y compris l’échographie endoscopique, la cystoscopie, les différentes possibilités d’application de l’apprentissage automatique pour la stratification des risques (p.ex. lors de résections hépatiques, de greffes du foie, de chimioembolisations transartérielles ainsi que d’analyses prédictives pour le choix du meilleur traitement possible en cas de maladies inflammatoires chroniques de l’intestin) ou encore l’utilisation de journaux numériques des symptômes pour les patient·es.
Statut juridique des dispositifs médicaux assistés par IA
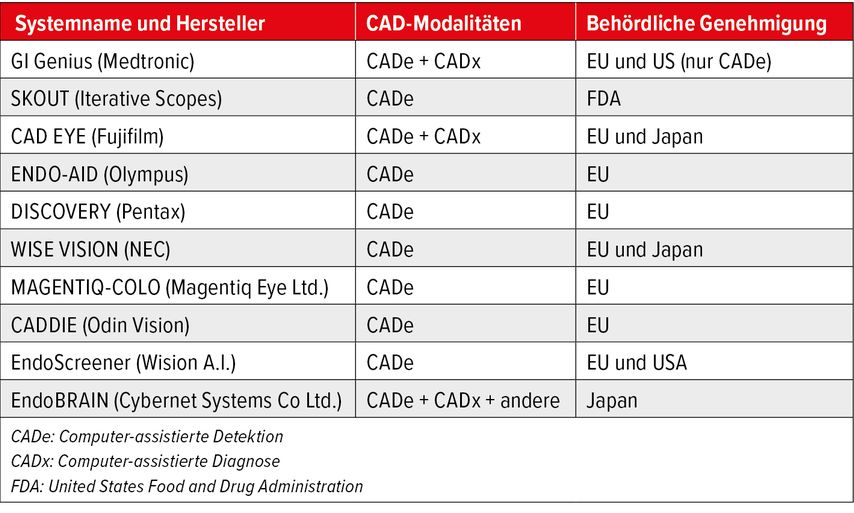
La classification précise des solutions basées sur l’IA et des applications dans le domaine de la gastroentérologie et de l’hépatologie fait également l’objet de réflexions intensives depuis le début des années 2020. Une telle classification (p.ex. la distinction entre un logiciel dans un dispositif médical et un logiciel en tant que dispositif médical) est essentielle pour définir le statut juridique de ces dispositifs médicaux. Seule cette distinction permet une catégorisation précise des logiciels ou des dispositifs basés sur l’IA disponibles ou en cours de développement, ce qui semble nécessaire d’un point de vue juridique. À l’heure actuelle, cette caractérisation et le succès des études cliniques ont conduit à l’autorisation de nombreux dispositifs de diagnostic assisté par ordinateur au sein de l’UE, notamment dans le domaine de l’endoscopie du tractus gastro-intestinal. L’IA est donc déjà disponible dans de nombreux pays en Europe en tant que «machine learning software as medical devices» pour la classification de la sévérité de la colite dans les maladies inflammatoires chroniques de l’intestin, pour la détection des hémorragies gastro-intestinales, pour la détection des dysplasies ainsi que pour la détection et la classification des polypes, y compris une recommandation thérapeutique correspondante. Les systèmes correspondants sont résumés dans le tableau 1.
Tab. 1: Systèmes assistés par ordinateur dans le domaine de l’endoscopie du tractus gastro-intestinal (modifié selon Chawla S et al.: Am J Gastroenterol 2021; 116: 2159-62)
Pour la quasi-totalité des applications médicales d’interprétation d’images assistée par ordinateur, il faut finalement distinguer les termes CADe («computer-aided detection») et CADx («computer-aided diagnosis»). À titre d’exemple, la seule détection de polypes ou de lésions de type polypes lors d’une coloscopie correspond à une CADe, alors que la classification de ces polypes, p.ex. selon le type I à III de la classification NICE, correspond à un CADx.
Des sensibilités et spécificités élevées ont pu être démontrées entre-temps dans un grand nombre d’analyses rétrospectives de grande qualité, mais aussi dans des essais randomisés contrôlés. Par conséquent, la sensibilité et la spécificité de la différenciation des adénomes et des très petits polypes colorectaux hyperplasiques sont désormais nettement supérieures à 90%, de même que la précision de ces méthodes. Les résultats de ces études ont récemment été présentés dans une revue (Okagawa Y et al.: Dig Dis Sci 2022; 67: 1553-72). Un volume de données comparable à celui pour la détection et la différenciation des polypes colorectaux par des méthodes de diagnostic assisté par IA existe également pour la détection et la classification des adénocarcinomes de l’œsophage, des carcinomes épidermoïdes de l’œsophage, pour la détection des carcinomes gastriques précoces et pour la classification des maladies inflammatoires chroniques de l’intestin. L’énorme volume de données provenant de zones de fort endémisme, comme la Chine, a en particulier permis d’améliorer rapidement la précision des gastroscopies de dépistage du carcinome gastrique précoce.
Avons-nous besoin de l’IA dans le domaine de l’endoscopie du tractus gastro-intestinal?
De nombreux travaux montrent qu’il est possible, p.ex. dans le domaine de la coloscopie de dépistage, d’augmenter significativement la sensibilité et la spécificité, et, en fin de compte, d’assurer et d’améliorer sa qualité. L’utilisation supplémentaire de «speedometers», qui enregistrent activement le temps de retrait ou la durée de séjour dans une région pendant le retrait du dispositif, permet d’augmenter davantage la sensibilité des examens. Plusieurs études, également contrôlées, ont aussi révélé que l’utilisation de l’IA améliorait significativement la formation et l’apprentissage de la pratique de l’endoscopie. L’utilisation de solutions d’imagerie/vidéo numériques et de l’endoscopie assistée par IA permet de sensibiliser plus rapidement les apprenant·es et de contrôler ainsi que de comparer les images enregistrées ou les diagnostics posés. Il est étonnant de constater que non seulement les apprenant·es en endoscopie retiennent plus rapidement en utilisant des méthodes assistées par IA, mais que même les examinateur·rices expérimenté·es non formé·es à l’IA peuvent améliorer de manière significative leurs qualités d’examinateur·rice en s’entraînant avec de telles méthodes. En fin de compte, l’utilisation de l’IA en endoscopie permet d’économiser du temps et de l’argent si elle est bien ciblée et utilisée par des personnes formées. On peut citer comme exemple la prévention des biopsies ou des polypectomies inutiles (p.ex. en cas de polypes rectaux hyperplasiques).
Les plus grands défis
Cette dynamique dans le développement et l’introduction de dispositifs basés sur l’IA dans le domaine de l’endoscopie du tractus gastro-intestinal (mais pas seulement) place les utilisateur·rices et les responsables des établissements hospitaliers devant d’énormes défis en matière de ressources (structurelles, financières et humaines). Outre les coûts d’achat, les besoins en matière de grandes capacités de mémoire pour les images, d’analyses standardisées et de mises à jour régulières des logiciels ne sont que quelques-uns des défis et des facteurs de coûts à mentionner. Il ne faut surtout pas oublier le temps de travail nécessaire à la formation et à l’apprentissage de la pratique dans les modèles de planification du personnel! De même, nous travaillons (ou devons travailler) avec des technologies logicielles et matérielles totalement obsolètes, utilisées depuis plus de 25 ans, pour de nombreux examens endoscopiques: le mot-clé est «programmes d’endoscopie». Cette (non-)évolution serait p.ex. totalement inimaginable dans la téléphonie mobile. Les raisons en sont multiples, mais il faut surtout les chercher dans les coûts élevés pour les responsables des structures (comme les responsables d’établissements hospitaliers et les propriétaires de cabinets médicaux), mais aussi dans le manque d’intérêt de l’industrie. On peut également imaginer que les besoins de maintenance croissants et les questions de responsabilité de plus en plus nombreuses sont les moteurs d’une telle (non-)évolution.
Quoi d’autre?
Les méthodes de diagnostic assisté par ordinateur représentent un changement de paradigme dans notre discipline, et pas seulement dans le domaine des techniques d’imagerie telles que l’endoscopie, l’échographie endoscopique ou l’échographie abdominale. La médecine personnalisée, au sens de l’analyse de données cliniques structurées et non structurées, telles que les données de laboratoire et de l’anamnèse, ainsi que l’annotation des données et le développement consécutif de modèles d’entraînement, et le développement de modèles assistés par IA font l’objet de recherches dans tous les domaines des maladies gastroentérologiques complexes telles que les maladies inflammatoires chroniques de l’intestin ou la prise en charge des maladies hépatiques avancées, dans un contexte sous haute pression. Seule l’utilisation de l’IA permet l’intégration très complexe de données issues de techniques d’imagerie, telles que l’échographie, la TDM ou l’IRM, conjointement avec des données histologiques et des biomarqueurs aux fins de développement et d’entraînement de modèles basés sur l’IA. Ces quatre dernières années, de nombreuses publications ont ainsi porté sur la prédiction de la récidive d’un carcinome hépatocellulaire après résection ou greffe du foie, ainsi que sur la réponse après chimioembolisation transartérielle. De tels jeux de données conduiront rapidement à la modification de nos algorithmes thérapeutiques actuels. Des analyses et des procédures comparables ont également été développées et testées pour la classification des tumeurs ou des kystes du pancréas, p.ex., et ont fait l’objet de publications de grande qualité. Le développement rapide des parcours diagnostiques et thérapeutiques basés sur l’IA nous laisse parfois perplexes.
Quand est-ce que tout cela doit avoir lieu?
De nombreuses possibilités d’application des systèmes basés sur l’IA dans le diagnostic et le traitement des maladies gastro-intestinales et hépatologiques ne concernent pas l’avenir, mais existent déjà. Grâce à l’introduction à grande échelle de méthodes basées sur l’IA, tout changera dans le domaine de la gastroentérologie. L’endoscopie du tractus gastro-intestinal deviendra plus précise, plus rapide et mieux guidée sur le plan technique, cela sera peut-être comparable au cas des pilotes d’avion en pilotage automatique.
L’utilisation de méthodes endoscopiques basées sur l’IA deviendra la norme dans les études cliniques et sera de plus en plus demandée par les patient·es, ce qui nous confrontera à d’importants défis structurels et financiers. Il convient également de mentionner le très grand volume de données à traiter ainsi que le besoin de mise à jour régulière et de formation des collaborateur·rices.
Il sera intéressant d’observer à quel moment une directive S3 exigera pour la première fois l’utilisation d’un algorithme spécifique ou d’une méthode endoscopique basée sur l’IA. Notre rôle de médecin dans la prise de décision concernant le diagnostic et le traitement des maladies gastroentérologiques et hépatologiques doit être redéfini. Nous devons également répondre rapidement à ce défi en termes de formation et trouver des solutions adéquates.
Que faut-il encore prendreen compte?
-
Dans tous les développements et efforts déployés, nos patient·es doivent rester au centre de nos préoccupations.
-
Le gain de temps pour les contacts avec les patient·es reste une exigence centrale de la médecine numérique.
-
Les objectifs des méthodes basées sur l’IA ne doivent pas suivre en premier lieu ceux de l’économie de la médecine, mais le bien-être des patient·es.
Littérature:
auprès de l’auteur
Das könnte Sie auch interessieren:
Néphrite lupique: détection en temps voulu et traitement adéquat
La néphrite lupique est l’une des principales manifestations organiques du lupus érythémateux systémique, car elle contribue de manière décisive à la morbidité et à la mortalité de la ...
Petites voies respiratoires, grands effets: «small airways disease»
La maladie des petites voies respiratoires («small airways disease», SAD) joue un rôle central dans les maladies respiratoires chroniques telles que la BPCO et l’asthme. Outre le ...
Réactivation du VHB sous traitement immunosuppresseur
En raison des dynamiques migratoires actuelles, la prévalence de l’infection par le virus de l’hépatite B (VHB) est également en hausse en Autriche. Il faut donc être particulièrement ...