Réactivation du VHB sous traitement immunosuppresseur
Auteure:
Dre méd. Caroline Schwarz
4. Medizinische Abteilung,
Gastroenterologie & Hepatologie
Klinik Ottakring
Wien
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
En raison des dynamiques migratoires actuelles, la prévalence de l’infection par le virus de l’hépatite B (VHB) est également en hausse en Autriche. Il faut donc être particulièrement attentif à une éventuelle réactivation chez les patient·es sous traitement immunosuppresseur. La vaccination prophylactique et le traitement médicamenteux permettent toutefois de lutter contre la réactivation du VHB (rVHB).
Keypoints
-
Avant tout traitement immunosuppresseur, il est obligatoire de déterminer le statut VHB par sérologie.
-
La vaccination est indiquée chez les patient·es jamais infecté·es par le VHB.
-
Une prophylaxie de la réactivation du VHB est indiquée chez les patient·es AgHBs+/ADN VHB+ ou antiHBc+ et présentant un risque élevé de réactivation.
Environ 240 millions de personnes dans le monde sont infectées par le virus de l’hépatite B (AgHBs+) et près d’un tiers de la population mondiale présente des marqueurs sérologiques d’une infection existante ou antérieure.1,2 La disponibilité du vaccin contre le VHB, l’accès aux traitements antiviraux ainsi que les facteurs socio-économiques influencent la prévalence locale du VHB et entraînent des différences géographiques significatives en matière d’épidémiologie. Au sein de la population autrichienne autochtone, la prévalence du VHB est globalement faible (<2%), mais en raison des dynamiques migratoires actuelles, certaines populations présentent parfois des prévalences nettement plus élevées, même dans les pays à faible prévalence.3,4
Parallèlement, les traitements immunosuppresseurs ou immunomodulateurs sont de plus en plus utilisés dans différents domaines de la médecine et ne sont plus limités aux indications oncologiques ou de transplantation depuis longtemps.5–8
Les personnes présentant des signes d’une infection antérieure (AgHBs–/antiHBc+ et/ou antiHBs+) ou existante (AgHBs+) par le VHB peuvent toutefois connaître une rVHB engageant potentiellement le pronostic vital en raison de la persistance de l’ADNccc du VHB dans les hépatocytes sous traitement immunosuppresseur.9
Définition de la réactivation du VHB
Il n’existe aucune définition uniforme de la rVHB dans la littérature, mais les concepts généraux sont globalement similaires.10 Chez les patient·es présentant une infection chronique par le VHB (AgHBs+ pendant ≥6 mois et ADN VHB+), la rVHB se définit par une augmentation de l’ADN VHB par rapport à la référence, bien que les sociétés spécialisées d’hépatologie ne donnent pas de valeurs de référence quantitatives uniformes.9–12 En cas d’infection par le VHB (AgHBs– et antiHBc+), le VHB est présent lorsque l’ADN VHB et/ou l’AgHBs+ (séroréversion) sont détectables dans le sang.10,13 La rVHB est plus souvent observée sous traitement immunosuppresseur, mais elle peut aussi survenir de manière spontanée.5,13–16
Stratification du risque
La possibilité d’une rVHB sous traitement immunosuppresseur résulte de la persistance de l’ADNccc du VHB dans les hépatocytes.11,16–18 Dans le cadre d’une réduction ou d’une perte du contrôle immunitaire de l’organisme, le virus peut se répliquer à nouveau sur la base de l’ADNccc. Le risque de rVHB dépend d’une part du statut VHB des patient·es avant le traitement immunosuppresseur (infection chronique par le VHB/hépatite [AgHBs+] par rapport à infection antérieure par le VHB [AgHBs–]), d’autre part du type de traitement immunosuppresseur.7,10,11,16,19,20
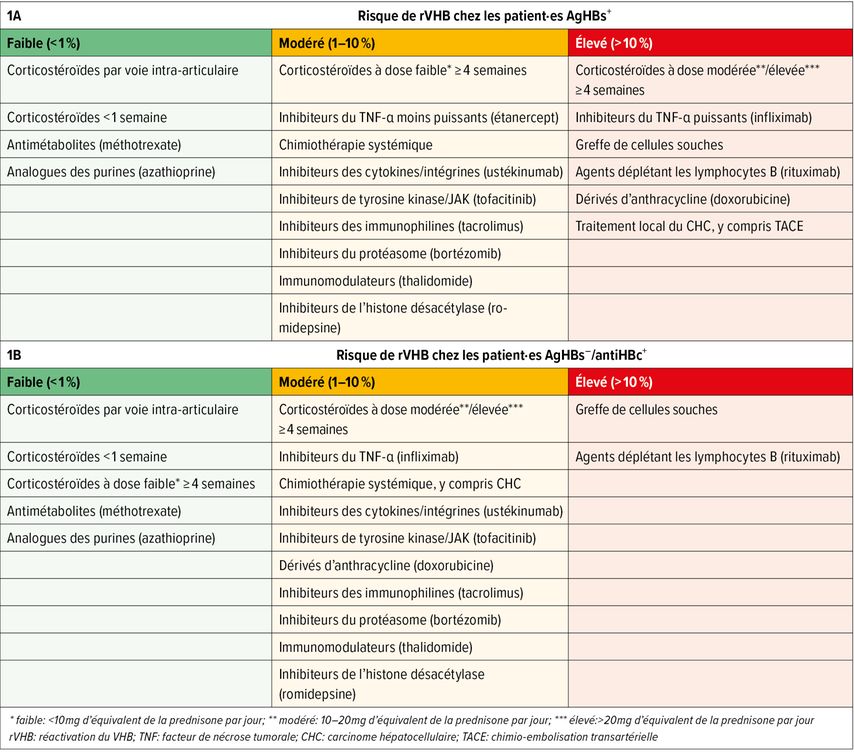
Alors que le risque de rVHB dans le cadre d’un traitement immunosuppresseur est généralement plus élevé chez les patient·es AgHBs+, en particulier en cas d’AgHBe+ et/ou de charge virale de l’ADN VHB élevée, la probabilité d’une rVHB chez les patient·es AgHBs– précédemment infecté·es par le VHB dépend du type de traitement immunosuppresseur.9,16 Le risque de rVHB est classé comme élevé (>10%), modéré (1–10%) ou faible (<1%) selon la cause ou la classe de substances entraînant l’immunosuppression (Fig.1).11,19,20
Fig. 1: Stratification du risque de différents traitements immunosuppresseurs par rapport à la survenue d’une réactivation du VHB, A: chez les patient·es AgHBs+, B: chez les patient·es AgHBs–/antiHBc+ (modifiée selon Morillas RM, López Sisamón D 2019; Choi J, Lim YS 2017; Loomba R, Liang TJ 2017; Smalls DJ et al. 2019; Perrillo RP et al. 2015)9,13,15,16,19
Des facteurs liés à l’hôte, tels que les maladies hématologiques sous-jacentes et le sexe masculin, augmentent également le risque de rVHB.16,21,22
Évolution clinique
La rVHB peut survenir tout au long du traitement immunosuppresseur, en fonction de la maladie sous-jacente, du type de traitement immunosuppresseur et des facteurs spécifiques à l’hôte, mais elle est souvent uniquement observée après une durée de traitement prolongée, voire à la fin du traitement immunosuppresseur.9
Initialement, il n’y a généralement aucun symptôme clinique dans le cadre d’une rVHB. Chez les patient·es AgHBs+, on observe une augmentation rapide de l’ADN VHB pendant cette phase, suivie d’une augmentation des transaminases.10,12
Au début, les patient·es AgHBs– développent à ce stade une séroréversion avec une positivité de l’AgHBs, ce qui entraîne également une augmentation de l’ADN VHB et une variation des transaminases.10,12 La plupart du temps, les patient·es présentant une rVHB restent asymptomatiques au cours de l’évolution, mais on observe parfois un épuisement, des douleurs abdominales hautes du côté droit ou un ictère.9 Une aggravation du tableau clinique avec coagulopathie, ascite et encéphalopathie hépatique au sens d’une insuffisance hépatique aiguë est possible et s’accompagne d’un taux de mortalité nettement plus élevé.15,17,23
Prophylaxie de la réactivation du VHB
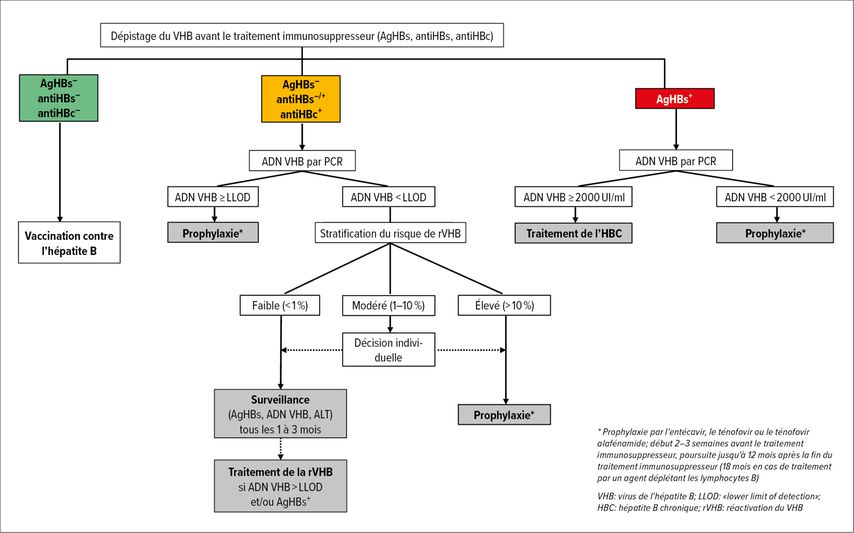
En raison de l’évolution potentiellement fulminante d’une rVHB sous traitement immunosuppresseur, il est crucial d’instaurer une prophylaxie suffisamment tôt. L’European Association for the Study of the Liver recommande de déterminer les marqueurs sérologiques spécifiques du VHB (AgHBs, antiHBs, antiHBc; ADN VHB quantitatif en cas d’AgHBs+ et/ou d’antiHBc+) avant l’instauration de tout traitement immunosuppresseur ainsi qu’en cas de diagnostic d’une infection par le VIH (Fig. 2).11
Les patient·es jamais infecté·es par le VHB (AgHBs–/antiHBs–/antiHBc–) doivent recevoir une vaccination complète contre le VHB le plus tôt possible.9,13,20
Fig. 2: Algorithme d’évaluation de l’indication d’une prophylaxie de la rVHB (modifiée selon Morillas RM, López Sisamón D 2019; EASL 2017)9,11
Chez les patient·es AgHBs+, une consultation en hépatologie et un traitement ou une prophylaxie par l’entécavir (ETV), le ténofovir disoproxil (TDF) ou le ténofovir alafénamide (TAF) sont indiqués. Dans la mesure du possible, l’évaluation hépatologique doit avoir lieu suffisamment tôt avant le début du traitement immunosuppresseur, mais elle ne doit pas retarder un traitement nécessaire.
Chez les patient·es présentant des signes d’exposition antérieure au VHB, l’indication d’une prophylaxie antivirale de la réactivation du VHB dépend de la charge virale de l’ADN VHB et du type de traitement immunosuppresseur prévu (Fig.1, 2).7,10,11,16,20
Traitement de la réactivation du VHB
Un diagnostic et un traitement précoces de la rVHB permettent généralement d’obtenir une réduction rapide de la charge virale du VHB.9,10,13–15 Une suppression spontanée de l’ADN VHB est également possible – si elle se produit, elle est typiquement observée dans le cadre de l’arrêt du traitement immunosuppresseur.9,17 Chez les patient·es qui ont déjà développé une insuffisance hépatique aiguë associée à la rVHB, la probabilité d’un contrôle virologique spontané est extrêmement faible.9,17,23
Si une rVHB est diagnostiquée sous traitement immunosuppresseur, un traitement antiviral par ETV, TDF ou TAF est immédiatement indiqué.11 Les patient·es infecté·es par le VIH doivent recevoir un traitement antirétroviral efficace contre le VHB.11 En cas de traitement immunosuppresseur ou immunomodulateur en cours, il convient de procéder à une évaluation stricte du rapport bénéfice-risque et, si possible, d’arrêter la substance concernée.
Conclusion
Une rVHB sous traitement immunosuppresseur peut entraîner une insuffisance hépatique aiguë dont l’évolution peut engager le pronostic vital. La détermination du statut VHB par sérologie est donc obligatoire avant l’instauration d’un traitement immunosuppresseur ou immunomodulateur ainsi qu’en cas de diagnostic d’une infection par le VIH. Comme les facteurs virologiques, médicamenteux et spécifiques à l’hôte doivent être pris en compte lors de l’évaluation des indications d’une prophylaxie contre le VHB, une évaluation individuelle est essentielle. Les patient·es jamais infecté·es par le VHB doivent recevoir une vaccination contre le VHB suffisamment tôt avant le traitement immunosuppresseur, tandis qu’un traitement antiviral ou une prophylaxie est indiqué·e pour les patient·es AgHBs+. Compte tenu de l’excellente tolérance des substances antivirales modernes ainsi que de l’évolution potentiellement fulminante en cas de rVHB, il est recommandé de poser une indication généreuse pour une prophylaxie de la rVHB, en tenant compte des comorbidités, chez les patient·es précédemment exposé·es au VHB et dont le risque de rVHB n’est pas clair, en particulier en cas de traitement par plusieurs immunosuppresseurs.
Littérature:
1 Schweitzer A et al.: Lancet 2015; 386: 1546-55 2 Trépo C et al.: Lancet 2014; 384: 2053-63 3 Coppola N et al.: Euro Surveill 2015; 20: 30009 4 Schmidbauer C et al.: Liver Int 2021; 41: 2622-34 5 Baumert LS et al.: Med 2024; 5: 126-31.e1 6 Chen LF et al.: Int J Rheum Dis 2017; 20: 859-69 7Fukuda W et al.: Arthritis Res Ther 2019; 21: 255 8 Lan TY et al.: Gut Liver 2023; 17: 288-98 9 Morillas RM, López Sisamón D: Med Clin (Barc) 2019; 152: 107-14 10 Myint A et al.: Clin Liver Dis 2020; 15: 162-7 11 European Association for the Study of the Liver: J Hepatol 2017; 67: 370-98 12Hoofnagle JH: Hepatology 2009; 49: 156-65 13 Choi J, Lim YS: J Infect Dis 2017; 216: 778-84 14 Bessone F, Dirchwolf M: World J Hepatol 2016; 8: 385-94 15 Loomba R, Liang TJ: Gastroenterology 2017; 152: 1297-309 16 Smalls DJ et al.: Pharmacotherapy 2019; 39: 1190-203 17 Anastasiou OE et al.: Viruses 2019; 11: 863 18 Yeo W, Chan HLY: J Gastroenterol Hepatol 2013; 28: 31-7 19 Perrillo RP et al.: Gastroenterology 2015; 148: 221-44.e3 20 Reddy KR et al.: Gastroenterology 2015; 148: 215-9, quiz e16-17 21Cheng AL et al.: Hepatology 2003; 37: 1320-8 22 Yeo W et al.: J Clin Oncol 2009; 27: 605-11 23 Zhu Y et al.: Front Microbiol 2022; 13: 910549
Das könnte Sie auch interessieren:
Les inhibiteurs de CDK4/6 mis en évidence
Le San Antonio Breast Cancer Symposium (SABCS) n’est généralement pas l’endroit où sont présentées des études de grande envergure venant modifier la pratique. Cette année encore, l’ ...
Néphrite lupique: détection en temps voulu et traitement adéquat
La néphrite lupique est l’une des principales manifestations organiques du lupus érythémateux systémique, car elle contribue de manière décisive à la morbidité et à la mortalité de la ...
Petites voies respiratoires, grands effets: «small airways disease»
La maladie des petites voies respiratoires («small airways disease», SAD) joue un rôle central dans les maladies respiratoires chroniques telles que la BPCO et l’asthme. Outre le ...