CAR-T-Zellen: Stellenwert – klinische Evidenz – Herausforderungen
Autorin:
Priv.-Doz. Dr. Alexandra Donschachner
3. Medizinische Abteilung – Zentrum für Hämatologie
Hanusch-Krankenhaus, Wien
E-Mail: alexandra.donschachner@oegk.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
„Chimeric antigen receptor“(CAR)-T-Zellen sind eine der bedeutendsten Innovationen der modernen Hämatologie. Es handelt sich dabei um autologe, genetisch modifizierte T-Zellen, die ex vivo mittels lentiviraler Transduktion einen synthetischen Rezeptor gegen ein tumorspezifisches Antigen exprimieren. Diese Therapie wirkt HLA-unabhängig und ermöglicht damit eine effektive Immunantwort. Die akademische Forschung an CAR-T-Zellen begann bereits in den 1990er-Jahren, erste klinische Fallberichte wurden ab 2010 publiziert, und seit 2018/2019 sind die ersten CAR-T-Zell-Therapien in Europa und den USA zugelassen.
Aufbau von CAR-T-Zellen und zugelassene Produkte
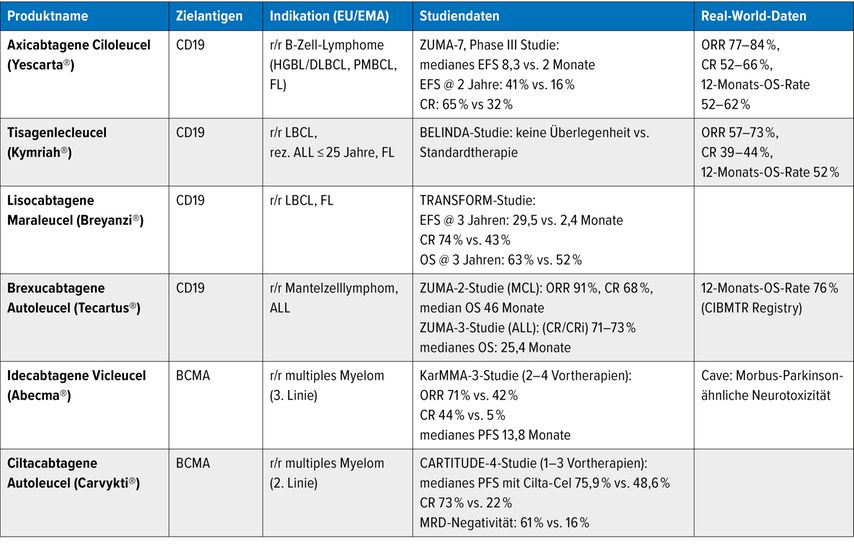
Alle kommerziell erhältlichen CAR-T-Zellen sind „Zweitgenerationskonstrukte“ und bestehen aus einer extrazellulären Antigenbindedomäne (meist scFv), einer Transmembrandomäne, einer intrazellulären Signaldomäne (CD3 zeta) und einer kostimulatorischen Domäne (CD28 oder 4-1BB). Derzeit sind sechs kommerzielle CAR-T-Zell-Produkte verfügbar, gegen zwei Antigene (CD19, BCMA; Tab.1).
Ablauf der CAR-T-Zell-Therapie
Der Ablauf der CAR-T-Zell-Therapie beginnt mit einer sorgfältigen Selektion geeigneter Patient:innen. Voraussetzungen sind vor allem eine möglichst geringe Tumorlast, eine gute allgemeine körperliche Verfassung sowie das Fehlen schwerer Komorbiditäten. Nach dem Stellen der Indikation erfolgt die Leukapherese zur Gewinnung autologer T-Zellen. Dabei sind definierte Blutbildparameter einzuhalten. Zudem ist eine Wash-out-Phase tumorspezifischer Therapien erforderlich, um die Qualität und Funktionalität der gewonnenen T-Zellen nicht zu beeinträchtigen. Das Apheresat wird anschließend an ein spezialisiertes Herstellungszentrum versandt, wo die Zellen ex vivo mittels lentiviraler Transduktion genetisch modifiziert und expandiert werden. Dieser Herstellungsprozess dauert in der Regel etwa drei bis vier Wochen. Die Herstellungsphase kann bei klinischer Notwendigkeit mit einer Holdingtherapie überbrückt werden. Diese soll eine Tumorprogression bis zur Re-Infusion verhindern.
Unmittelbar vor der CAR-T-Zell-Gabe erhalten die Patient:innen eine lymphodepletierende Chemotherapie, bestehend aus Fludarabin/Cyclophosphamid oder alternativ Bendamustin. Ziel dieser Vorbehandlung ist es, eine systemische Inflammation zu minimieren und die Expansion sowie Persistenz der CAR-T-Zellen zu fördern. Die Re-Infusion erfolgt in der Regel als einmalige intravenöse Gabe, im Anschluss ist ein engmaschiges stationäres Monitoring erforderlich. Dieses sollte über einen Zeitraum von 10 bis 14 Tagen an einem spezialisierten Zentrum erfolgen.
Aktuelle Leitlinien und Indikationen
Diffuses großzelliges B-Zell-Lymphom (DLBCL)
Über viele Jahre war beim rezidivierten DLBCL eine platinbasierte Salvage-Chemotherapie mit anschließender autologer Stammzelltransplantation (ASZT) Standard. Der Nutzen beschränkte sich jedoch auf chemosensitive Rezidive, besonders bei einem Rückfall >12 Monate nach Erstdiagnose. Zwei wichtige Studien, ZUMA-7 und TRANSFORM (Tab.1), zeigten ein signifikant verlängertes ereignisfreies Überleben (EFS) gegenüber der Standardtherapie bei primär refraktärer Erkrankung oder frühem Rezidiv innerhalb von zwölf Monaten nach Beendigung der Erstlinientherapie. CAR-T-Zellen gelten in dieser Indikation in den aktuellen Leitlinien als neuer Therapiestandard. Auch bei älteren, nicht hochdosisfähigen Patient:innen konnte eine Wirksamkeit gezeigt werden (ALYCANTE-, PILOT-Studie).
Mantelzelllymphom
Basierend auf den Ergebnissen der ZUMA-2-Studie ist Brexu-cel seit Jänner 2021 zugelassen beim rezidivierten/refraktären Mantelzelllymphom nach einem BTK-Inhibitor. Hier zeigten sich insgesamt hohe Gesamt- und Komplettremissionsraten (CR) mit einem medianen Gesamtüberleben (OS) von 46 Monaten.
Follikuläres Lymphom
CAR-T-Zellen zeigen auch beim follikulären Lymphom hohe Ansprechraten in fortgeschrittenen Therapielinien und werden zunehmend früher im Therapieverlauf evaluiert.
Multiples Myelom
Die Einführung von BCMA-gerichteten CAR-T-Zellen (Cilta-cel, Ide-cel) hat das Therapiespektrum des multiplen Myeloms wesentlich erweitert. Die wichtigsten Studien dabei sind CARTITUDE-1 und CARTITUDE-4.
CARTITUDE-1 war eine Phase-Ib/II-Studie und untersuchte Cilta-cel bei stark vorbehandelten Patient:innen. Die Langzeitergebnisse zeigten ein medianes OS von 60,7 Monaten, etwa ein Drittel der Patient:innen war progressionsfrei (PFS) ohne Erhaltungstherapie.
In der Phase-III-Studie CARTITUDE-4 wurde Cilta-cel randomisiert gegen zwei etablierte Standardtherapien untersucht. Dabei konnte ein 12-Monats-PFS von 75,9% erreicht werden, eine ORR von 84,6%, eine CR-Rate von 73% und eine beeindruckende MRD-Negativität von 60,6% (vs. 15,6% im Vergleichsarm). Die MRD-Negativität etabliert sich auch beim multiplen Myelom zunehmend als klinisch relevanter Meilenstein.
Nebenwirkungsmanagement
Das Nebenwirkungsmanagement ist ein zentraler Bestandteil der CAR-T-Zell-Therapie und erfordert eine strukturierte, interdisziplinäre Betreuung sowohl in der Akutphase als auch im Langzeitverlauf.
Akuttoxizitäten
Zu den häufigsten und klinisch relevantesten Akuttoxizitäten zählt das „cytokine release syndrome“ (CRS). Dieses ist Ausdruck einer systemischen Inflammation infolge der massiven Aktivierung von Immunzellen und tritt typischerweise innerhalb weniger Stunden bis Tage nach der CAR-T-Zell-Re-Infusion auf. Das CRS wird in vier Schweregrade (Grad 1–4) eingeteilt. Die Therapie umfasst zunächst supportive Maßnahmen wie Flüssigkeitssubstitution und Antipyretika. Bei klinischer Verschlechterung oder höhergradigem CRS ist ein frühzeitiger Einsatz immunmodulatorischer Substanzen erforderlich, vor allem des IL-6-Rezeptorantagonisten Tocilizumab sowie von systemischen Kortikosteroiden. In ausgewählten Fällen kann zusätzlich der IL-1-Rezeptorantagonist Anakinra eingesetzt werden. Zur frühzeitigen Identifikation von Hochrisikopatient:innen wird eine Risikostratifizierung mittels etablierter CRS-Scores empfohlen.
Eine weitere charakteristische Akuttoxizität ist das immuneffektorzellassoziierte Neurotoxizitätssyndrom (ICANS). Dieses kann ein breites Spektrum neurologischer Symptome umfassen, darunter Benommenheit, Sprach- und Wortfindungsstörungen, Tremor, Kopfschmerzen, epileptische Anfälle bis hin zu schweren Bewusstseinsstörungen. Das Monitoring erfolgt standardisiert mittels des ICE-Scores, wobei besonders Veränderungen im Schriftbild als frühes Warnzeichen gelten. Ab einem ICANS-Grad ≥2 wird der Einsatz von Dexamethason empfohlen, auch wenn der klinische Nutzen nicht eindeutig belegt ist.
Darüber hinaus können im Rahmen der CAR-T-Zell-Therapie Organtoxizitäten auftreten, insbesondere mit kardialer, hepatischer, renaler oder kutaner Beteiligung. Diese erfordern eine engmaschige klinische und laborchemische Überwachung sowie eine organspezifische supportive Therapie.
Spättoxizitäten
Auch die Spättoxizitäten spielen eine wesentliche Rolle für die Langzeitprognose der Patient:innen. Infektionen sind hierbei die häufigste Ursache der Non-relapse-Mortalität. Entsprechend sind strukturierte Infektprophylaxen, regelmäßiges Monitoring sowie Impfstrategien essenziell (siehe auch Impfempfehlungen Onkopedia). Ferner sind eine Immunsurveillance und die Überwachung der immunologischen Rekonstitution der CD4-positiven T-Zellen und B-Zellen erforderlich und auch prognostisch relevant. Persistierende Zytopenien sind ebenfalls häufig und können den Einsatz von Wachstumsfaktoren wie G-CSF oder Thrombopoetin-Rezeptoragonisten erforderlich machen. Aufgrund der Expression der Targetantigene auch auf gesunden Plasmazellen kommt es häufig zu einer B-Zell-Aplasie mit konsekutiver Hypogammaglobulinämie, was eine Substitution von Immunglobulinen notwendig machen kann. Das Risiko für Sekundärmalignome nach CAR-T-Zell-Therapie ist derzeit noch nicht abschließend geklärt. Aufgrund der limitierten Langzeitdaten wird eine strukturierte und langfristige Nachsorge empfohlen.
Insgesamt ist eine konsequente Langzeitnachsorge unerlässlich, um therapieassoziierte Komplikationen frühzeitig zu erkennen und adäquat zu behandeln.
Epidemiologie und Versorgungsrealität in Europa und Österreich
Die Versorgungsrealität in Hinsicht auf zelluläre Therapien in Europa befindet sich in einem dynamischen Wandel. Der EBMT Activity Survey dokumentiert seit 2020 einen Rückgang der autologen Stammzelltransplantation (ASZT), der parallel zum zunehmenden Einsatz von CAR-T-Zell-Therapien verläuft. Dieser Trend spiegelt den wachsenden Stellenwert immuntherapeutischer Ansätze bei lymphatischen Neoplasien wider. Im Jahr 2023 wurden in Europa insgesamt 47731 hämatopoetische Stammzelltransplantationen durchgeführt, davon 27246 ASZT und 20485 allogene Transplantationen. Den größten Anteil der ASZT machten Patient:innen mit multiplem Myelom aus: 13803. Im gleichen Zeitraum wurden bei dieser Indikation 736 CAR-T-Zell-Therapien vorgenommen, was den zunehmenden, jedoch noch ausbaufähigen Einsatz von CAR-T-Zellen im Therapiekonzept des multiplen Myeloms verdeutlicht.
Auch bei B-Zell-Lymphomen zeigt sich eine deutliche Verschiebung hin zu CAR-T-Zell-Therapien. So wurden 2023 4826 Patient:innen mit B-Zell-Lymphomen einer Stammzelltransplantation zugeführt, während 3437 Patient:innen eine CAR-T-Zell-Therapie erhielten. Diese Zahlen unterstreichen, dass die CAR-T-Zell-Therapie besonders in dieser Indikation zunehmend etablierte Therapieformen ersetzt oder ergänzt.
In Österreich ist eine ähnliche Entwicklung zu beobachten. Die Anzahl der durchgeführten CAR-T-Zell-Therapien stieg von 84 Behandlungen im Jahr 2023 auf rund 150 Therapien im Jahr 2024 deutlich an. Dass sich die Zahl innerhalb eines Jahres nahezu verdoppelt hat, reflektiert sowohl die Erweiterung der zugelassenen Indikationen als auch den verbesserten Zugang zu spezialisierten Behandlungszentren.
Insgesamt verdeutlichen diese epidemiologischen Daten, dass CAR-T-Zell-Therapien in Europa und Österreich zunehmend in die klinische Routine integriert werden und einen wesentlichen Beitrag zur Weiterentwicklung der hämatologischen Versorgung leisten.
Ausblick
CAR-T-Zell-Therapien haben die Prognose zahlreicher lymphatischer Neoplasien nachhaltig verbessert und sind ein Meilenstein der modernen Immuntherapie. Trotz dieser Erfolge bestehen weiterhin relevante Herausforderungen, vor allem betreffend den komplexen und zeitintensiven Herstellungsprozess, das spezifische Akut- und Spättoxizitätsspektrum sowie offene Fragen hinsichtlich der langfristigen Finanzierung und breiten Zugänglichkeit dieser Therapien. Zukünftige Entwicklungen fokussieren sich auf die Optimierung der biologischen Eigenschaften von CAR-T-Zellen, insbesondere auf eine verbesserte Persistenz. Darüber hinaus werden Strategien zum Umgehen oder Vermeiden von Resistenzmechanismen intensiv erforscht, etwa durch duale Antigen-Targeting-Ansätze oder „armored“ CAR-Konstrukte mit zusätzlicher immunmodulatorischer Aktivität.
Ein weiterer zentraler Entwicklungsschwerpunkt ist die Erweiterung der Indikationen über hämatologische Neoplasien hinaus. Erste präklinische und klinische Studien untersuchen den Einsatz von CAR-T-Zellen bei soliden Tumoren sowie bei ausgewählten Autoimmunerkrankungen, was das therapeutische Potenzial dieser Technologie erheblich erweitern könnte. Insgesamt wird die Weiterentwicklung der CAR-T-Zell-Therapie maßgeblich davon abhängen, wie erfolgreich biologische Innovationen, klinische Sicherheit und ökonomische Rahmenbedingungen in Einklang gebracht werden können.
Literatur:
● Berdeja JG et al.: Lancet 2021; 398(10297): 314-24 ● Kamdar M et al.: Lancet 2022; 399(10343): 2294-308 ● Locke FL et al.: NEJM 2022; 386(7): 640-54 ● Neelapu SS et al.: NEJM 2017; 377(26): 2531-44 ● Onkopedia-Leitlinie „CAR-T Zellen: Management von Nebenwirkungen“, Stand 5/2025 ( www.onkopedia.com/de/onkopedia/guidelines ) ● Onkopedia-Leitlinie „Diffuses großzelliges B-Zell-Lymphom“, Stand 12/2025 ( www.onkopedia.com/de/onkopedia/guidelines ) ● Passweg JR et al.: BMT 2025; 60(4): 519-28 ● Wang M et al.: NEJM 2020; 382(14): 1331-42
Das könnte Sie auch interessieren:
Akute myeloische Leukämie (AML) – State of the Art 2025
Die aktuellen Therapiestandards der akuten myeloischen Leukämie ermöglichen eine spezifisch auf die Patient:innen abgestimmte Therapie, je nach Eignung für Chemotherapie und genetischem ...
Highlights on myeloproliferative neoplasms from the EHA2025 Congress
The Swiss Cancer Institute’s Young Oncology Academy (YOA) is a support and mentorship program for young oncologists. Academy participants are supervised by a renowned faculty member for ...
Anamnese oder präoperatives Gerinnungsscreening?
Blutgerinnungsstörungen können zu intra- wie auch postoperativen Blutungen führen, die abhängig von Lokalisation und Schweregrad ernste Folgen nach sich ziehen können. Ziel einer ...