Therapieneuerungen: FL, CLL und LBCL
Autoren:
PD Dr. med. et Dr. phil. nat. Marc Wehrli1
Prof. Dr. med. Urban Novak2
1 Oberarzt, FMH medizinische Onkologie
Inselspital, Universitätsspital Bern
Klinik und Poliklinik für Medizinische Onkologie
2 Chefarzt & Leiter der Poliklinik der Medizinischen Onkologie
Inselspital, Universitätsspital Bern
Korrespondenz:
E-Mail: urban.novak@insel.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Am Jahreskongress der American Society of Hematology (ASH) wurden zahlreiche relevante Neuerungen in der Lymphomtherapie vorgestellt. Wir präsentieren drei ausgewählte Studien zur chronischen lymphatischen Leukämie (CLL) und zum follikulären Lymphom sowie einen Real-World-Vergleich der drei zugelassenen CAR-T-Zell-Produkte zur Behandlung des «large B-cell lymphoma» (LBCL).
Keypoints
-
Zeitlich limitierte Therapie beim CLL – Studie CLL17:Zeitlich limitierte Kombinationstherapien können in CLL17 vergleichbar tiefe Remissionen mit hoher MRD-Negativität wie kontinuierliche BTK-Inhibition erreichen und eröffnen damit für ausgewählte Patient:innen eine klinisch attraktive Option mit definiertem Therapieende.
-
Epcoritamab + R-Quadrat (R2) – Studie EPCORE FL1:Die EPCORE-FL1-Daten zeigen, dass Epcoritamab in Kombination mit R-Quadrat beim follikulären Lymphom im (rezidivierenden oder refraktären) Zweitlinien-Setting hohe Raten kompletter und MRD-negativer Remissionen bei kontrollierbarer CRS und Neurotoxizität erzielt und damit ein potenziell neuer immuntherapeutischer Standard diskutiert wird.
-
Real-World-Vergleich der drei CAR-T-Produkte bei LBCL:Die grosse Real-World-Analyse bestätigt die hohe Wirksamkeit aller drei zugelassenen CAR-T-Zell-Produkte beim LBCL, zeigt jedoch produkt- und zentrumsspezifische Unterschiede in Ansprechkinetik und Toxizität, die eine individualisierte CAR-T-Auswahl im klinischen Alltag unterstützen.
Zeitlich limitierte Therapie beim CLL – die CLL17-Studie
Am ASH-Kongress 2025 rückte die CLL17-Studie den Stellenwert zeitlich limitierter Therapieansätze bei der chronischen lymphatischen Leukämie (CLL) erneut in den Fokus. Während sich in den vergangenen Jahren die kontinuierliche Behandlung mit BTK-Inhibitoren als Standard etabliert hat, adressiert CLL17 die Frage, ob fixe, zeitlich begrenzte Therapiestrategien eine vergleichbare Krankheitskontrolle erzielen können – und dies bei gleichzeitig verbesserter Lebensqualität und reduzierter Therapielast.
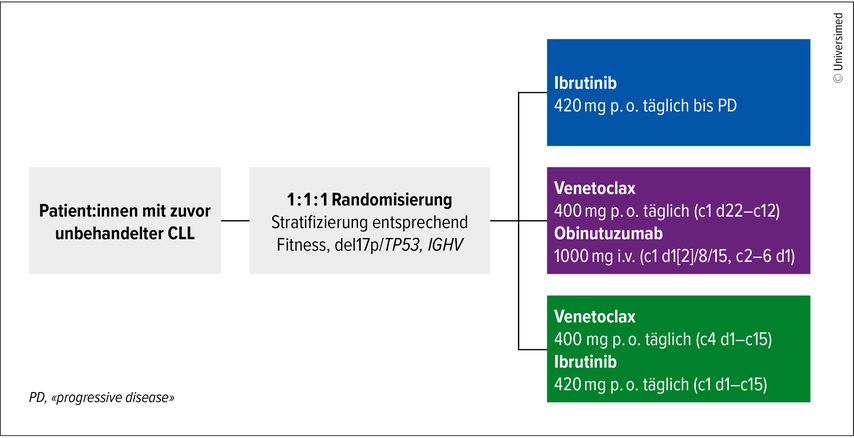
Präsentiert wurden aktualisierte Wirksamkeits- und Sicherheitsdaten der dreiarmigen Phase-III-Studie, in der eine kontinuierliche, rein zielgerichtete Therapie mit zeitlich limitierten Kombinationen verglichen wurde. Konkret wurde Ibrutinib (zeitlich unlimitiert) gegen Venetoclax+Obinutuzumab (zeitlich für ein Jahr limitiert) gegen Venetoclax+Obinutuzumab (zeitlich für ein Jahr limitiert) verglichen, entsprechend 1:1:1 randomisiert sowie nach Fitness, Deletion17p/TP53 sowie IGHV stratifiziert (Abb.1).
Zeitgleich mit der Präsentation wurde die Studie von Al Sawaf et al. im New England Journal of Medicine publiziert. Ein zentrales Augenmerk lag auf der Rate an MRD-Negativität sowie der Dauer der therapiefreien Intervalle nach Behandlungsende.
Die am Kongress vorgestellten Ergebnisse zeigen, dass ein relevanter Anteil der Patient:innen unter zeitlich limitierter Kombinationstherapie tiefe Remissionen erreicht, die ein Absetzen der Behandlung erlauben, ohne dass kurzfristig ein Verlust der Krankheitskontrolle zu beobachten ist.
Besonders interessant ist, dass die MRD-negativen Raten in einigen Armen im Bereich jener oder sogar oberhalb jener liegen, die man aus Studien mit kontinuierlicher Monotherapie kennt. Dies hat unmittelbare Implikationen für die klinische Praxis: Für geeignete Patient:innen – insbesondere solche mit grossem Wunsch nach Therapiefreiheit oder mit kumulierter Toxizität unter Langzeittherapie – könnte ein zeitlich begrenztes Regime künftig eine attraktive Alternative darstellen.
Kontrovers diskutiert wurden am ASH-Kongress die noch begrenzte Nachbeobachtungsdauer und die offenen Fragen zur Resistenzentwicklung nach Absetzen der Therapie. Unklar bleibt zudem, ob sich langfristig Unterschiede im Gesamtüberleben oder im Sequenzmanagement späterer Therapielinien zeigen werden (Abb. 2).
Abb. 2: Gesamtüberleben (OS) in der Studie CLL17 (modifiziert nach Al-Sawaf et al., N Engl J Med 2025)
Gleichwohl positioniert CLL17 zeitlich limitierte Konzepte als ernst zu nehmende Option neben der etablierten Dauertherapie und liefert essenzielle Daten für eine echte partizipative Entscheidungsfindung im Arzt-Patienten-Gespräch. Für die DACH-Region, in der Kosten, Toxizität und Patient:innenpräferenzen zunehmend an Bedeutung gewinnen, könnte CLL17 künftig massgeblich die Diskussion über die optimale Erstlinientherapie der CLL prägen.
EPCORE FL1: bispezifischer CD20/CD3-Antikörper Epcoritamab in Kombination mit R-Quadrat (R2)
Das follikuläre Lymphom bleibt trotz generell guter Prognose eine chronische Erkrankung mit wiederkehrenden Rezidiven, insbesondere bei Hochrisikopatient:innen.
Am ASH-Kongress 2025 rückte die Studie EPCORE FL1 Epcoritamab – einen subkutan applizierbaren, bispezifischen CD20/CD3-Antikörper – in Kombination mit Rituximab und Lenalidomid (R2) in den Mittelpunkt der Diskussion zur Rezidivtherapie. Ziel ist es, durch den zusätzlichen bispezifischen CD20/CD3-Antikörper die Tiefe und Dauer der Remissionen über das etablierte R2-Regime hinaus zu steigern, ohne die Toxizität inakzeptabel zu erhöhen.
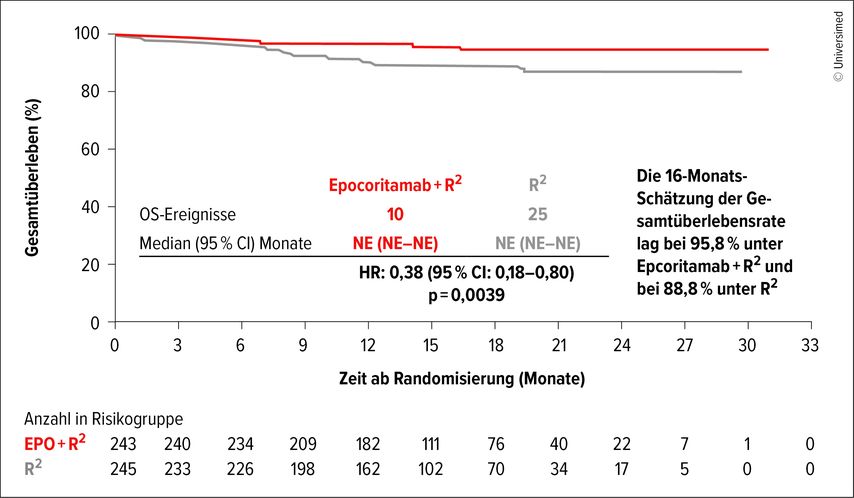
Die am Kongress präsentierten Daten dokumentieren die Überlegenheit von Epcoritamab+R2 bezüglich Gesamtüberleben (OS) mit einer Hazard-Ratio von 0,38 und einem signifikanten p-Wert von 0,0039 (Abb.3). Weiter zeigen die Daten hohe Gesamtansprechraten (ORR) mit einem bemerkenswerten Anteil kompletter Remissionen, die über den historischen Vergleichswerten für R2 alleine liegen.
Abb. 3: Positiver Trend im Gesamtüberleben bei Therapie mit Epcoritamab+R2 in der Studie EPCORE FL1 (modifiziert nach Falchi et al. 2025)
Die Sicherheitsanalyse zeigte das für bispezifische Antikörper typische Profil mit Zytokinfreisetzungssyndromen (CRS) und neurotoxischen Ereignissen, überwiegend im niedrigen Schweregrad. Durch ein gestuftes Dosierungsschema, stationäre Überwachung in der frühen Phase sowie etablierte Managementprotokolle konnten schwerwiegende Komplikationen meist verhindert oder rasch kontrolliert werden.
Aus Sicht der klinischen Praxis stellt sich die Frage, für welche Patient:innengruppen dieser intensivierte Ansatz in der rezidivierten oder refraktären Situation einen Mehrwert bietet. Subgruppenanalysen deuten darauf hin, dass insbesondere Patient:innen mit grossem Tumorbulk, frühem Progress (POD24-Risiko) oder ungünstigen klinischen und biologischen Risikofaktoren profitieren könnten. Gleichzeitig muss die Rolle von Epcoritamab im Gesamtkonzept berücksichtigt werden: Wie lässt sich diese Therapie mit zukünftigen Sequenzen – etwa anderen bispezifischen Antikörpern oder CAR-T-Zell-Therapie – sinnvoll verknüpfen, ohne potenzielle Resistenzmechanismen zu verstärken?
Für das deutschsprachige hämatologisch-onkologische Setting ist EPCORE FL1 vor allem als Signalstudie zu verstehen, die den Weg zu immunmodulatorisch verstärkten Rezidivtherapien ebnet. Ob und in welcher Form dieser Ansatz den Standard verändern wird, bleibt Gegenstand weiterer Phase-III-Studien und gesundheitsökonomischer Bewertungen, auch im Vergleich zu den Daten der inMIND-Studie.
Die drei zugelassenen CAR-T-Zell-Produkte im Real-World- Vergleich – CAR-T bei LBCL
CAR-T-Zell-Therapien haben die Behandlung des refraktären oder mehrfach rezidivierten «large B-cell lymphoma» (LBCL) grundlegend verändert. Während Zulassungsstudien klare Evidenz für Wirksamkeit und Machbarkeit geliefert haben, bleiben wichtige Fragen zur Übertragbarkeit in den klinischen Alltag offen.
Am ASH-Kongress 2025 erregte daher eine grosse Real-World-Analyse Aufmerksamkeit, in der die drei kommerziell verfügbaren CAR-T-Produkte systematisch miteinander verglichen wurden. Eingeschlossen waren 925 Patient:innen aus zahlreichen Zentren mit hoher Heterogenität hinsichtlich Alter, Komorbiditäten, Vortherapien und Krankheitsbiologie – damit war die Analyse deutlich näher an der Versorgungsrealität als die selektionierten Studienpopulationen.
Die präsentierten Daten bestätigten die insgesamt hohe antitumorale Aktivität aller drei Produkte mit relevanten Gesamtansprech- und Komplettremissionsraten (CRR), auch bei stark vorbehandelten und biologisch ungünstigen Verläufen. Gleichzeitig traten Unterschiede in der Kinetik und der Dauer des Ansprechens sowie im Sicherheitsprofil zutage.
Schweregrad und Management hinsichtlich Toxizität hingen neben dem Produkt selbst wesentlich von Zentrenexpertise, Supportivkonzept und Patient:innenselektion ab. Mit Liso-cel (Breyanzi®) behandelte Patient:innen waren im Median älter und erhielten häufiger eine Überbrückungstherapie. Die Anwendung von Axi-cel (Yescarta®) war mit einer kürzeren Zeitspanne zwischen Leukapherese und Reinfusion sowie mit einer geringeren Häufigkeit von Produkten ausserhalb der Spezifikationen assoziiert. Axi-cel zeigte die höchste Rate an hochgradigem CRS und ICANS, war jedoch nicht mit einer erhöhten 30- oder 90-Tage-Mortalität verbunden.
Zwischen Axi-cel und Liso-cel bestanden keine Unterschiede hinsichtlich der Ansprechrate, des Gesamtüberlebens (OS) oder des progressionsfreien Überlebens (PFS). Dabei wurden «confounding factors» wie ECOG, Histologie, Double Hit, Krankheitsstadium sowie primär refraktäre Erkrankungen mitberücksichtigt.
Tisa-cel (Kymriah®) war mit einer geringeren ORR, einer niedrigeren CRR, einem kürzeren OS und einem kürzeren PFS sowie mit einer höheren 90-Tage-Mortalität assoziiert.
Besonders relevant ist die Beobachtung, dass auch ältere Patient:innen und solche mit moderaten Organfunktionsstörungen substanziell profitieren können, sofern ein strukturiertes Assessment sowie ein engmaschiges periinterventionelles Monitoring etabliert sind.
Diskutiert wurden am ASH-Kongress zudem logistische Faktoren wie Produktionszeiten, Notwendigkeit und Art der Bridging-Therapie, Bettensituation und interdisziplinäre Zusammenarbeit, die sich in den Real-World-Outcomes messbar niederschlagen.
Insgesamt unterstreichen die Daten, dass die Wahl des CAR-T-Produkts zunehmend individualisiert erfolgen sollte – basierend auf Patient:innencharakteristika, Risikoprofil, Zentrumserfahrung und organisatorischen Rahmenbedingungen. Für die klinische Routine liefern diese Real-World-Ergebnisse eine wichtige Orientierungshilfe, um CAR-T-Therapien künftig früher und breiter in die Behandlungspfade von LBCL-Patient:innen zu integrieren.
Fazit und Ausblick
Die am ASH-Kongress 2025 präsentierten Daten unterstreichen eindrücklich, wie dynamisch sich das therapeutische Spektrum in der Lymphombehandlung weiterentwickelt.
Für die CLL illustriert CLL17, dass zeitlich limitierte, hochwirksame Kombinationstherapien mit definiertem Therapieende eine realistische Alternative zur Dauertherapie darstellen und damit sowohl medizinische als auch patient:innenrelevante Bedürfnisse adressieren.
Beim follikulären Lymphom deutet EPCORE FL1 darauf hin, dass bispezifische Antikörper wie Epcoritamab in Kombination mit R-Quadrat das Konzept der Rezidivtherapie grundlegend erweitern und eine neue Qualität der Remissionstiefe ermöglichen könnten.
Im Bereich der aggressiven Lymphome liefern die umfangreichen Real-World-Daten zu CAR-T-Zell-Therapien eine wertvolle Orientierung für die individualisierte Produktwahl und die strukturelle Weiterentwicklung der Versorgungslandschaft.
Für die klinische Praxis in der DACH-Region entsteht daraus ein klarer Auftrag: Die Integration dieser innovativen Ansätze erfordert eine Integration von akademischer Evidenz, multidisziplinärer Expertise und individuellen Patient:innenpräferenzen. Gleichzeitig gewinnen Fragen der Langzeitnachsorge, der Sequenzierung zielgerichteter und zellulärer Therapien sowie gesundheitsökonomische Überlegungen weiter an Bedeutung.
Die kommenden Jahre werden zeigen, in welchem Ausmass zeitlich limitierte Regime, bispezifische Antikörper und CAR-T-Zell-Strategien nicht nur bestehende Standards ergänzen, sondern diese in ausgewählten Subgruppen auch ablösen.
Schon jetzt ist absehbar, dass eine präzise Risikostratifizierung und echte partizipative Entscheidungsfindung entscheidend sein werden, um das Potenzial dieser neuen Therapien voll auszuschöpfen und den individuell bestmöglichen Nutzen für unsere Patient:innen zu realisieren.
Literatur:
bei den Verfassern
Das könnte Sie auch interessieren:
„Die Lebensqualität ist sehr variabel, auch innerhalb der Subtypen“
Im Rahmen eines JATROS-Interviews mit Ao. Univ.-Prof. Dr. Wolfgang Reinhard Sperr, MedUni Wien, wollten wir einen Einblick in den Umgang mit der seltenen Erkrankung „systemische ...
Therapie im Wandel: zeitlich begrenzt und Sequenzierung
Die therapeutische Landschaft der chronischen lymphatischen Leukämie (CLL) hat sich in den vergangenen Jahren fundamental gewandelt. Die klassische Chemoimmun-therapie ist weitgehend ...
Chronische myeloische Leukämie (CML)
Die Prognose der CML-Patient:innen unterscheidet sich durch die Entwicklung der Tyrosinkinaseinhibitoren (TKI) kaum mehr von der Normalbevölkerung. Dennoch gibt es neue Erkenntnisse, die ...
%20in%20der%20Studie%20CLL17.jpg)