La transplantation d’îlots de Langerhans à l’ère de l’insulinothérapie moderne
Compte-rendu:
Dre méd. Anna Maria Roll
Journaliste médicale
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Le traitement du diabète de type 1 (DT1) a fait d’énormes progrès au cours des cent dernières années. Cependant, les technologies modernes telles que la mesure du glucose en continu, les pompes à insuline et les systèmes de délivrance automatisée d’insuline (p.ex. systèmes «closed loop») ne sont pas adaptées à tou·tes les patient·es. La transplantation d’îlots de Langerhans constitue une alternative importante, surtout chez les patient·es souffrant d’hypoglycémies sévères. Le PD Dr méd. Karim Gariani des Hôpitaux Universitaires Genève a expliqué son importance à l’ère de l’insulinothérapie moderne lors de la conférence annuelle de la Société Suisse d’Endocrinologie et de Diabétologie (SSED).
Les systèmes «closed loop» sont considérés aujourd’hui comme la meilleure option thérapeutiques chez les personnes atteintes de DT1, à condition bien sûr que la mise en place soit possible et que les patient·es arrivent à les utiliser», a expliqué l’expert. Ces systèmes mesurent la glycémie toutes les trois à cinq minutes environ et délivrent de l’insuline pour la corriger. «Seules les cellules bêta de l’organisme fonctionnent de manière encore plus précise, car elles sont capables de mesurer le taux de glucose pratiquement en continu et de réagir en conséquence», explique K. Gariani.
L’insulinothérapie moderne permet de contrôler très efficacement la glycémie. En cas de DT1, le «time in range» (TIR), c’est-à-dire le temps pendant lequel la glycémie se situe dans la cible, augmente de plus de 10%.1 L’expert a souligné qu’il n’était toutefois pas possible de résoudre tous les problèmes avec ces technologies, car des hypoglycémies sévères continuent de survenir malgré les progrès techniques réalisés.2 On constate également des effets secondaires tels que des réactions cutanées locales et d’autres limitations. Par exemple, certain·es patient·es ne veulent pas porter d’appareil, refusent les alarmes fréquentes ou ont des difficultés à utiliser les systèmes.
Prévention des hypoglycémies et amélioration de la qualité de vie
«L’objectif de la transplantation d’îlots de Langerhans est de prévenir les hypoglycémies sévères et d’améliorer ainsi la qualité de vie. Elle ne vise pas en premier lieu à obtenir une indépendance vis-à-vis de l’insuline. Les patient·es doivent en être conscient·es», a souligné l’intervenant.
La transplantation d’îlots de Langerhans est particulièrement adaptée chez les patient·es atteint·es de DT1 et souffrant d’hypoglycémies sévères. Le critère est la survenue de deux épisodes ou plus d’hypoglycémie sévère au cours des deux dernières années. De plus, une altération de la perception de l’hypoglycémie joue également un rôle. Pour les patient·es qui nécessitent également une transplantation rénale, les critères sont généralement moins stricts. En revanche, les patient·es ayant un besoin élevé en insuline (>0,7U/kgPC/j) ne sont pas éligibles pour une transplantation d’îlots de Langerhans, car cela réduit considérablement les chances de succès. L’obésité diminue également les chances de succès.
Histoire et développement de la transplantation d’îlots de Langerhans
L’idée d’un traitement de remplacement des cellules bêta remonte à plus d’un siècle. La première transplantation du pancréas a été réalisée avec succès en 1966 et la première méthode automatique d’isolement des îlots de Langerhans a été développée dans les années 1980. En 2000, le protocole d’Edmonton a constitué une percée décisive: pour la première fois, des patient·es ont montré une indépendance temporaire vis-à-vis de l’insuline après une transplantation d’îlots de Langerhans, et ce sous traitement immunosuppresseur sans corticoïdes. Ce protocole constitue la base des stratégies de transplantation modernes qui ont été développées depuis.3 Au cours des deux dernières décennies, plus de 4000 transplantation d’îlots de Langerhans ont été réalisées dans le monde, principalement en Europe et en Amérique du Nord.4
Comment se déroule une transplantation d’îlots de Langerhans?
Dans la transplantation d’îlots de Langerhans conventionnelle, le pancréas est prélevé sur un donneur décédé, puis est soumis à une phase de digestion enzymatique en laboratoire à l’aide de collagénase afin de séparer les îlots endocrines du tissu exocrine. Il s’ensuit plusieurs étapes de préparation visant à obtenir des îlots de Langerhans aussi purs et fonctionnels que possible. La transplantation réelle est réalisée dans le cadre d’une radiologie interventionnelle. Les îlots de Langerhans sont perfusés dans la veine porte à l’aide d’un cathéter guidé par échographie.5 «Cette perfusion ne dure généralement qu’une trentaine de minutes. Deux ou trois perfusions sont en principe nécessaires pour transplanter suffisamment d’îlots de Langerhans, mais elles ne sont pas réalisées le même jour», a expliqué K. Gariani. Une transplantation d’îlots de Langerhans peut être réalisée après ou simultanément à une transplantation rénale.
Pour éviter un rejet immunologique, les patient·es reçoivent un traitement immunosuppresseur. Il consiste en général en un traitement d’induction par la globuline antithymocyte ou des anticorps anti-IL-2R, ainsi qu’en un traitement d’entretien par le tacrolimus et le mycophénolate. «Les complications de l’intervention sont rares, mais nous ne devons pas les négliger», a averti K. Gariani. Des saignements au niveau du site d’injection ou une thrombose de la veine porte peuvent survenir. À long terme, l’immunosuppression peut poser des problèmes (risque d’infection, de tumeurs malignes).
Transplantation d’îlots de Langerhans par rapport à transplantation du pancréas
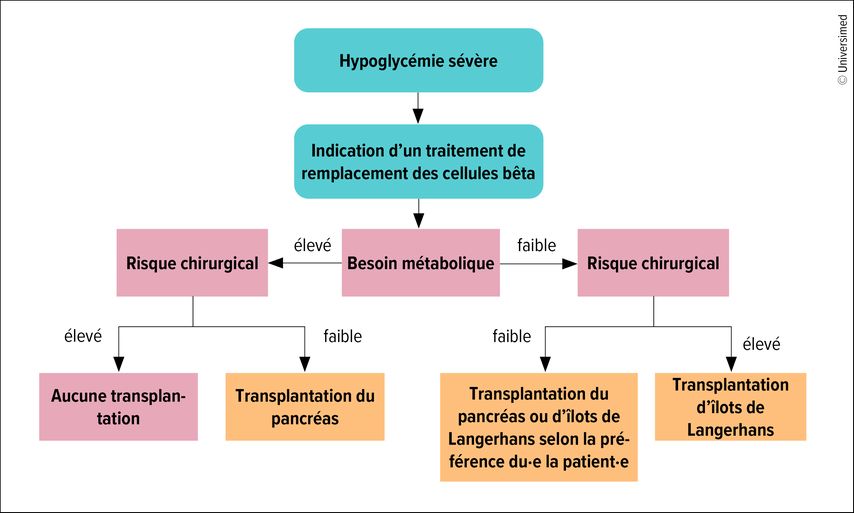
La question de savoir si une transplantation d’îlots de Langerhans ou du pancréas entier est le traitement le plus approprié pour les patient·es souffrant d’hypoglycémies sévères dépend principalement du besoin métabolique (Fig.1). «Différents algorithmes thérapeutiques sont disponibles pour prendre cette décision», a déclaré l’intervenant. Si le besoin en insuline est élevé, les chances de succès d’une transplantation d’îlots de Langerhans sont limitées. Une transplantation du pancréas peut, le cas échéant, être envisagée chez les patient·es âgé·es de moins de 55 ans présentant une bonne situation vasculaire. Bien qu’elle soit plus invasive et comporte davantage de risques, cette intervention permet souvent d’obtenir de meilleurs résultats métaboliques à long terme par rapport à la transplantation d’îlots de Langerhans. En cas de besoin en insuline faible, la transplantation d’îlots de Langerhans peut en revanche constituer une option appropriée, surtout si les patient·es présentent un risque chirurgical élevé.
Fig. 1: Transplantation d’îlots de Langerhans ou du pancréas? Algorithme thérapeutique chez les patient·es atteint·es de DT1 et souffrant d’hypoglycémies sévères (adaptée selon Wojtusciszyn A et al. 2019)5
La transplantation rénale est la première indication en présence d’une insuffisance rénale chronique terminale. La pertinence d’une stratégie combinant transplantation rénale et d’îlots de Langerhans ou du pancréas dépend également du besoin métabolique ou du risque chirurgical.5 Une transplantation du pancréas seule, sans transplantation rénale simultanée, est aujourd’hui rarement réalisée.
Bénéfices manifestes de la transplantation d’îlots de Langerhans
Plusieurs études révèlent que la transplantation d’îlots de Langerhans améliore nettement le contrôle glycémique: l’HbA1c, le glucose à jeun et, particulièrement important, le nombre d’hypoglycémies sévères diminuent.6 On observe parallèlement une réduction nette du besoin en insuline, même s’il peut à nouveau augmenter légèrement à long terme. Nombre de patient·es font en outre état d’une nette amélioration de leur qualité de vie, notamment en ce qui concerne le stress lié au diabète.7 Cela se manifeste aussi bien après une transplantation d’îlots de Langerhans seule qu’en combinaison avec une transplantation rénale.8
Des données à long terme portant sur plus de 250 patient·es ayant subi une transplantation montrent que le greffon fonctionne encore chez plus de la moitié après dix ans. Environ 20% des patient·es n’ont toujours pas besoin d’insuline après dix ans. «La réduction durable du nombre d’hypoglycémies sévères est cependant bien plus importante que l’indépendance vis-à-vis de l’insuline», a souligné l’expert. En effet, les patient·es dont le greffon fonctionnait encore après 20 ans ne présentaient plus d’hypoglycémies sévères.9
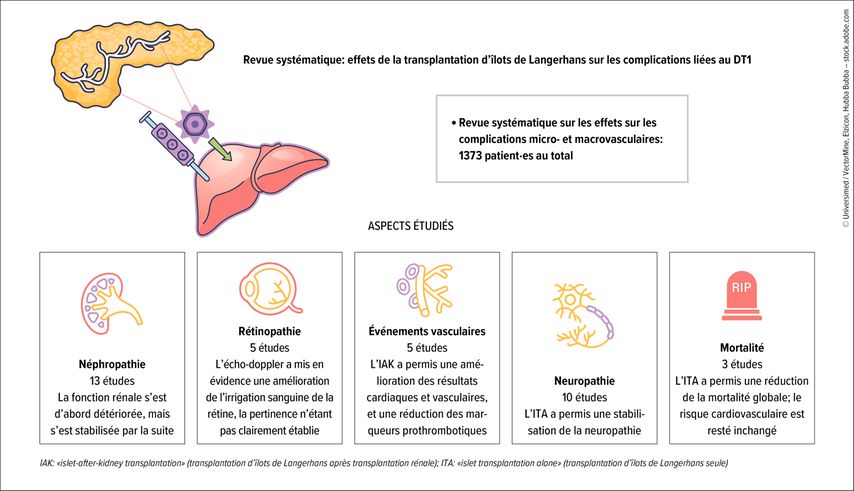
Outre l’amélioration du contrôle glycémique, la transplantation d’îlots de Langerhans semble également ralentir la progression des complications liées au diabète.10 Des études ont par exemple mis en évidence que la progression de la rétinopathie diabétique et de la neuropathie pouvait être ralentie, voire stoppée (Fig.2).11 Les patient·es ayant subi une transplantation rénale présentaient en outre un risque nettement plus faible de nouvelle dialyse s’il·elles avaient subi simultanément une transplantation d’îlots de Langerhans que ceux·elles qui ne l’avaient pas subi.12
Fig. 2: Effets de la transplantation d’îlots de Langerhans sur les complications micro- et macrovasculaires du diabète (adaptée selon Gariani K et al. 2025)11
Nouveaux développements: cellules souches et édition génomique
Les recherches actuelles se concentrent sur l’utilisation de cellules souches pour produire des cellules productrices d’insuline.13 Les résultats semblent prometteurs: la production d’insuline a repris et le contrôle glycémique s’est amélioré. De plus, le risque d’hypoglycémie et le besoin en insuline ont diminué. Les avantages de cette méthode sont l’indépendance potentielle par rapport aux organes de donneur·ses et l’administration unique sous forme de perfusion. Toutefois, des questions restent en suspens concernant les aspects éthiques, les coûts et l’efficacité à long terme.
D’autres stratégies comprennent la transplantation de cellules encapsulées qui doivent empêcher une réaction immunitaire et peuvent ainsi rendre le traitement immunosuppresseur superflu. Les études menées jusqu’à présent n’ont cependant pas donné de résultats convaincants. Parallèlement, il existe d’autres approches très innovantes: chez une patiente chinoise, des cellules autologues ont par exemple été reprogrammées en laboratoire en cellules d’îlots de Langerhans productrices d’insuline, puis transplantées de manière autologue dans le muscle abdominal.14 En Suède, des chercheur·ses ont tenté de modifier génétiquement et d’adapter immunologiquement des cellules de donneur·ses de tissu pancréatique à l’aide de technologies modernes (entre autres CRISPR-Cas9).15 «Il pourrait donc être possible de développer des stratégies de transplantation sans traitement immunosuppresseur à long terme», conclut K. Gariani.
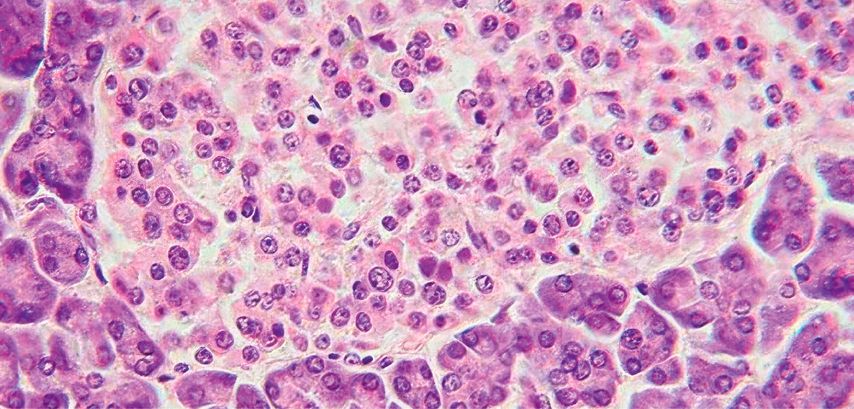
Fig. 3: Îlots de Langerhans, coloration à l’HE
Source:
Congrès annuel de la Société Suisse d’Endocrinologie et de Diabétologie (SSED), du 13 au 14 novembre 2025, à Lucerne
Littérature:
1 Fan W et al.: Efficacy and safety of automated insulin delivery systems in patients with type 1 diabetes mellitus: a systematic review and meta-analysis. Diabetes Metab J 2025; 49: 235-51 2 Sherr JL et al.: Severe hypoglycemia and impaired awareness of hypoglycemia persist in people with type 1 diabetes despite use of diabetes technology: results from a cross-sectional survey. Diabetes Care 2024; 47: 941-7 3 Berney T et al.: Allogeneic islet transplantation: chronicle of a death foretold? Transpl Int 2025; 38: 14598 4 Berney T et al.: A worldwide survey of activities and practices in clinical islet of Langerhans transplantation. Transpl Int 2022; 35: 10507 5 Wojtusciszyn A et al.: Indications for islet or pancreatic transplantation: statement of the TREPID working group on behalf of the Société francophone du diabète (SFD), Société francaise d’endocrinologie (SFE), Société francophone de transplantation (SFT) and Société française de néphrologie – dialyse – transplantation (SFNDT). Diabetes Metab 2019; 45: 224-37 6 Lablanche S et al.: Ten-year outcomes of islet transplantation in patients with type 1 diabetes: Data from the Swiss-French GRAGIL network. Am J Transplant 2021; 21: 3725-33 7 Markmann JF et al.: Phase 3 trial of human islet-after-kidney transplantation in type 1 diabetes. Am J Transplant 2021; 21: 1477-92 8 Gariani K et al.: Effect of islet alone or islets after kidney transplantation on quality of life in type 1 diabetes: A systematic review. Transplant Rev 2024; 38: 100870 9 Marfil-Garza BA et al.: Pancreatic islet transplantation in type 1 diabetes: 20-year experience from a single-centre cohort in Canada. Lancet Diabetes Endocrinol 2022; 10: 519-32 10 Perrier Q et al.: Impact of islet transplantation on diabetes complications and mortality in patients living with type 1 diabetes. Diabetes Care 2025; 48: 1007-15 11 Gariani K et al.: Impact of islet transplantation on type 1 diabetes-related complication: a systematic review. Transpl Int 2025; 38: 15091 12 Maanaoui M et al.: Islet-after-kidney transplantation versus kidney alone in kidney transplant recipients with type 1 diabetes (KAIAK): a population-based target trial emulation in France. Lancet Diabetes Endocrinol 2024; 12: 716-24 13 Reichman TW et al.: Stem cell-derived, fully differentiated islets for type 1 diabetes. N Engl J Med 2025; 393: 858-68 14 Wang S et al.: Transplantation of chemically induced pluripotent stem-cell-derived islets under abdominal anterior rectus sheath in a type 1 diabetes patient. Cell 2024; 187: 6152-6164.e18 15 Carlsson PO et al.: Survival of transplanted allogeneic beta cells with no immunosuppression. N Engl J Med 2025; 393: 887-94
Das könnte Sie auch interessieren:
L’obésité et ses conséquences sur les reins
L’obésité est devenue l’un des principaux problèmes de santé dans le monde. Elle a des conséquences directes et indirectes sur les reins. Outre le risque de glomérulopathie et l’ ...
Une perte de poids précoce peut favoriser la rémission du diabète de type 2
De nouveaux concepts physiopathologiques remettent en question la compréhension actuelle du diabète de type 2 (DT2). L’accent n’est plus mis sur l’augmentation de la glycémie, mais sur ...
Suivi à long terme après un cancer de l’enfant ou de l’adolescent: points pertinents pour les internistes et les médecins de famille
En raison de l’augmentation de la survie globale après un cancer de l’enfant ou de l’adolescent, la population de patients ayant survécu à un cancer de l’enfant ne cesse de croître et de ...