Potentiel thérapeutique des ARN non codants dans le diabète
Auteur:
Pr Romano Regazzi, PhD
Département des Sciences Biomédicales
Faculté de Biologie et Médecine
Université de Lausanne
E-mail: romano.regazzi@unil.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Nos cellules produisent des milliers d’ARN qui ne codent pas pour des protéines. L’étude du rôle de ces molécules a permis de mieux comprendre les mécanismes impliqués dans de nombreuses pathologies, dont le diabète sucré. Le développement d’approches visant à moduler leur activité ainsi que l’identification d’ARN non codants dans le sang et dans d’autres fluides corporels, pourraient, dans un avenir proche, fournir de nouveaux outils thérapeutiques pour la prise en charge des patients diabétiques.
Keypoints
-
Nos cellules contiennent des dizaines de milliers d’ARN non codants qui, bien qu’ils ne produisent pas de protéines, jouent un rôle central dans la régulation des fonctions cellulaires.
-
Le profil d’expression de ces ARN non codants est altéré, tant dans les îlots de Langerhans que dans les tissus cibles de l’insuline, au cours du développement du diabète de type 1 et de type 2.
-
Diverses approches thérapeutiques visant à moduler l’expression des ARN non codants afin de prévenir ou de traiter le diabète sont actuellement à l’étude.
-
Les cellules libèrent dans la circulation des vésicules extracellulaires contenant une partie de leurs ARN non codants. Ces derniers peuvent servir de biomarqueurs pour prédire la réponse des patients diabétiques à certains traitements et ainsi améliorer leur prise en charge.
Le génome humain est constitué d’environ 3 milliards de paires de bases, mais moins de 2% de ces séquences codent pour des protéines. Nous savons aujourd’hui que les régions non codantes du génome donnent naissance à des dizaines de milliers d’ARN jouant un rôle essentiel dans la régulation des fonctions cellulaires. Les ARN non codants présentent des longueurs et des modes d’action très variés.1,2 Les microARNs sont les plus connus et les mieux étudiés: composé de 21 à 23 nucléotides, ils inhibent la traduction de nombreux ARN messagers cibles et régulent ainsi l’expression d’une grande partie des protéines cellulaires. Le développement de nouvelles techniques de séquençage a permis d’identifier d’autres classes d’ARN non codants, telles que les piARNs, les longs ARN non codants et les ARN circulaires.1 Certains ARN non codants sont également générés par clivage d’autres ARN, comme les tsARNs issus de la fragmentation d’ARN de transfert ou les sinARNs dérivés de séquences introniques des ARN messagers.2
Contribution des ARN non codants au développement du diabète
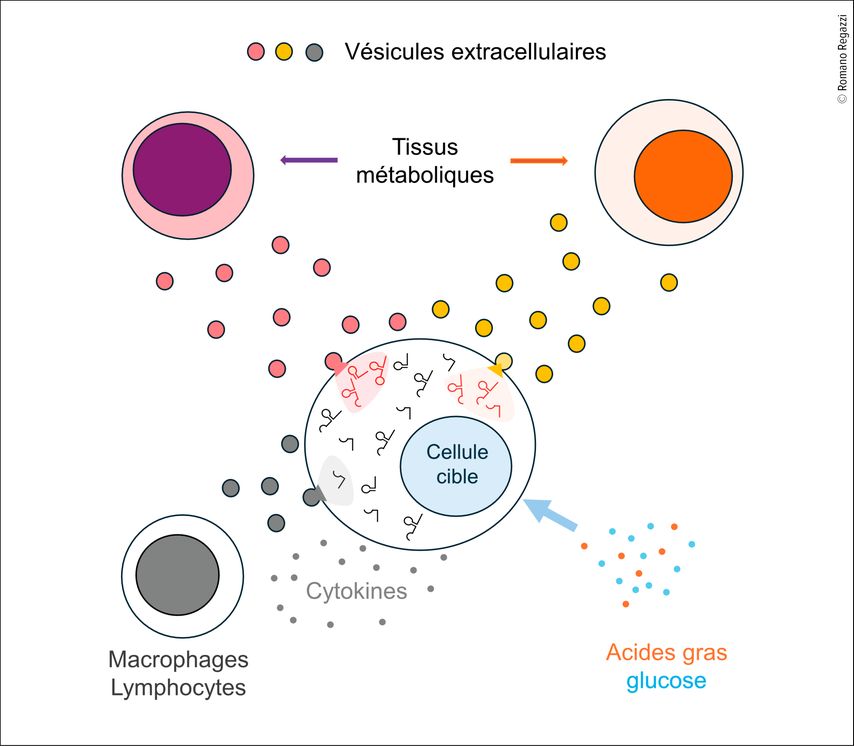
Plusieurs études ont mis en évidence des variations du niveau d’ARN non codants, associées au développement du diabète, aussi bien dans des modèles animaux que chez l’homme.3–5 Des modifications du profil d’expression des microARNs, mais aussi d’autres classes d’ARN non codants (longs ARN non codants, ARN circulaires, tsARNs) ont été observées.6–8 Ces altérations surviennent pendant les phases précoces du diabète de type 1 et sont également associées au diabète de type 2. Elles concernent non seulement les cellules bêta pancréatiques, mais aussi les cellules cibles de l’insuline, telles que les hépatocytes, les cellules musculaires et les adipocytes. Une partie de ces changements résulte d’une exposition prolongée à des cytokines pro-inflammatoires ou à des concentrations élevées d’acides gras saturés et de glucose (Fig. 1). D’autres modifications peuvent être dues au transfert d’ARN non codants entre cellules. En effet, la plupart des cellules libèrent des vésicules extracellulaires contenant des ARN non codants, notamment des microARNs et des tsARNs, capables de fusionner avec des cellules cibles et d’y transférer leur contenu.2 La composition de ces vésicules varie selon le type cellulaire et les conditions physiopathologiques. Ainsi, les hépatocytes, les adipocytes, les cellules musculaires et les îlots pancréatiques échangent des ARN non codants afin de coordonner leur activité et de réguler le métabolisme corporel.9 Ces échanges peuvent être altérés en conditions pathologiques et contribuer à la résistance à l’insuline. Un transfert d’ARN non codants a également lieu lors des phases initiales du diabète de type 1 entre les cellules immunitaires infiltrant les îlots de Langerhans et les cellules bêta, contribuant au dysfonctionnement et à l’élimination des cellules insulino-sécrétrices.10,11
Fig. 1: Mécanismes qui règlent le niveau des ARN non codants. Les cellules impliquées dans le contrôle du métabolisme corporel contiennent plusieurs milliers d’ARN non codants. Leur expression peut être altérée par une exposition prolongée à des cytokines pro-inflammatoires, ainsi qu’à des concentrations élevées d’acides gras saturés ou de glucose. Le niveau de ces ARN peut également être modifié par le transfert d’ARN non codants via des vésicules extracellulaires provenant d’autres tissus métaboliques ou de cellules immunitaires
Compte tenu de leur rôle central dans la régulation cellulaire, des altérations du profil d’expression des ARN non codants peuvent entraîner un dysfonctionnement, voire la mort des cellules. Par exemple, une augmentation de certains microARNs peut perturber la sécrétion d’insuline dans les cellules bêta ou induire une insulino-résistance dans le foie et le tissu adipeux. Des stratégies thérapeutiques visant à corriger ces anomalies pourraient permettre de prévenir, voire traiter le diabète. Des études chez la souris ont montré que l’inhibition de certains microARNs surexprimés dans la cellule bêta au cours du diabète de type 2 peut empêcher le développement de la maladie.12 Bien que ces travaux constituent une preuve de concept, ils ne sont pas directement transposables chez l’homme, ce qui nécessite le développement d’approches alternatives.
Stratégies thérapeutiques pour moduler l’activité des ARN non codants
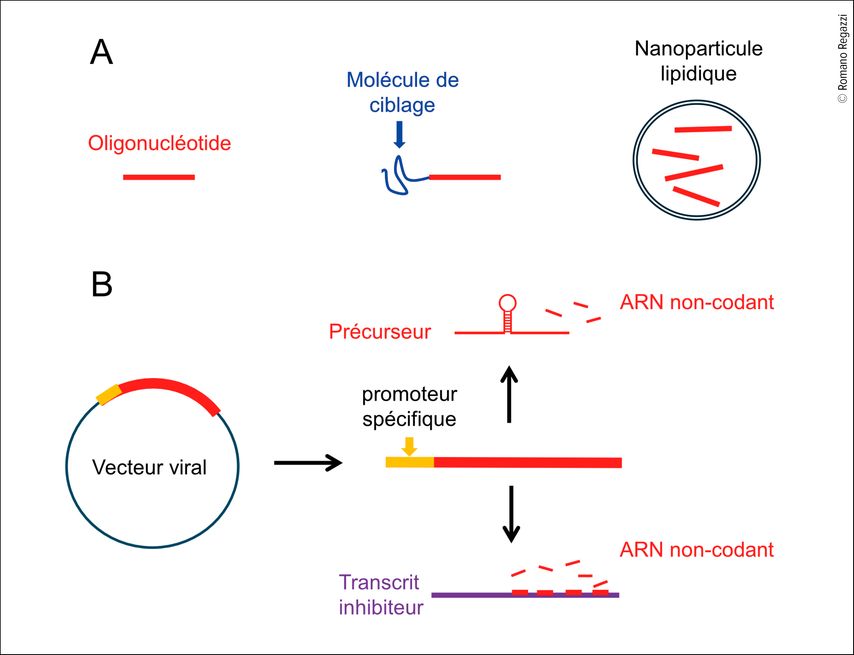
Deux approches principales peuvent être envisagées pour moduler spécifiquement le niveau d’un ARN non codants: l’introduction d’oligonucléotides synthétiques mimant ou bloquant spécifiquement ces ARN, ou bien l’utilisation de vecteur viraux capables de produire ou d’inhiber l’action des ARN non codants (Fig. 2). Chacune de ces approches présente des avantages et des obstacles.
Fig. 2: Approches pour moduler spécifiquement le niveau ou l’activité des ARN non codants dans des cellules cibles. A) Des oligonucléotides de synthèse mimant les séquences des ARN non codants ou capables de bloquer leur action sont couplés à des molécules permettant de les délivrer spécifiquement dans les cellules cibles. Ces molécules de ciblage peuvent être des peptides ou des aptamères (séquences d’ARN ou d’ADN adoptant des structures tridimensionnelles permettant une liaison spécifique à un ligand). Les oligonucléotides de synthèse peuvent aussi être encapsulés dans des nanoparticules lipidiques conçues pour cibler des types cellulaires spécifiques. B) Une approche alternative repose sur l’utilisation de vecteurs viraux permettant l’expression de précurseurs d’ARN non codants ou de transcrits inhibiteurs capables de les lier et de les séquestrer. L’expression de ces transcrits est contrôlée par des promoteurs spécifiques, actifs uniquement dans les cellules cibles
Les oligonucléotides de synthèse permettent déjà d’augmenter ou de diminuer de manière efficace et spécifique le niveau des microARNs et des tsARNs. La stabilité et l’affinité de ces molécules sont améliorées grâce à l’introduction de nucléotides modifiés. De nombreuse études chez les rongeurs ont démontré l’efficacité de ces oligonucléotides aussi bien in vitro qu’in vivo. Toutefois, le principal obstacle à leur utilisation en clinique réside dans le manque de spécificité tissulaire, car ces molécules pénètrent dans toutes les cellules. Étant donné l’implication des ARN non codants dans de multiples processus physiologiques et pathologiques, l’utilisation de ces molécules chez l’homme n’est pas envisageable à ce jour. Des recherches sont en cours pour développer des stratégies permettant de délivrer spécifiquement ces oligonucléotides dans les cellules cibles (Fig. 2). Ces approches incluent le couplage des oligonucléotides à des ligands spécifiques (peptides ou aptamères) capables de cibler des molécules présentes à la surface des cellules13 ou l’encapsulation dans des nanoparticules lipidiques conçues pour cibler des organe particuliers.14
Une approche alternative consiste à utiliser des virus modifiés, non pathogènes, pour délivrer les ARN non codants dans les cellules cibles (Fig. 2). Dans ce cas, la production de l’ARN par le vecteur viral est contrôlée par un promoteur spécifique uniquement actif dans la cellule cible. Par exemple, le promoteur du gène de l’insuline permet de cibler la cellule bêta et celui de l’albumine les hépatocytes. Cette stratégie peut également être utilisée pour bloquer l’activité d’un ARN non codant (Fig. 2). Dans ce cas, le vecteur viral est conçu pour exprimer un transcrit capable de séquestrer l’ARN non codant et l’empêcher d’interagir avec ces cibles naturelles. Dans un modèle de souris qui développe spontanément la maladie, le blocage des microARNs transférés des cellules immunitaires aux cellules bêta au cours des phases précoces du diabète de type 1 a permis de prévenir l’apparition du diabète.11
Les ARN non codants circulants comme biomarqueurs
Une fraction des ARN non codants produits par les cellules est libérée au sein de vésicules extracellulaires et peut être détectée dans divers fluides corporels. Leur libération étant influencée par l’état physiologique, leur mesure dans le sang ou l’urine constitue une source d’information précieuse sur l’apparition et la progression des maladies.15 Une étude récente a permis de développer un algorithme capable d’identifier des patients diabétiques et de prédire leur réponse à certains traitements en fonction du profil des microARNs circulants.16 L’analyse de ces ARN non codants pourrait ainsi devenir un outil important pour guider les décisions thérapeutiques.
Conclusion et perspectives
La découverte des ARN non codants a profondément transformé notre compréhension des mécanismes impliqués dans l’apparition de nombreuses maladies, y compris le diabète sucré. Le développement de stratégies visant à corriger les altérations de leur expression ou de leur activité ouvre des perspectives prometteuses pour de nouveaux traitements. Par ailleurs, l’analyse des ARN non codants circulants permet de mieux comprendre la communication intercellulaire et pourrait faciliter une médecine plus personnalisée. Si ces avancées se confirment, les ARN non codants pourraient devenir, dans un avenir proche, des outils essentiels pour améliorer la prise en charge des patients diabétiques.
Littérature:
1 Guay C et al.: Roles of Noncoding RNAs in Islet Biology. Compr Physiol 2020; 10(3): 893-932 2 Jacovetti C et al.: Emerging Classes of Small Non-Coding RNAs With Potential Implications in Diabetes and Associated Metabolic Disorders. Front Endocrinol (Lausanne) 2021; 12: 670719 3 Trajkovski M et al.: MicroRNAs 103 and 107 regulate insulin sensitivity. Nature 2011; 474(7353): 649-53 4 Kornfeld JW et al.: Obesity-induced overexpression of miR-802 impairs glucose metabolism through silencing of Hnf1b. Nature 2013; 494(7435): 111-5 5 Nesca V et al.: Identification of particular groups of microRNAs that positively or negatively impact on beta cell function in obese models of type 2 diabetes. Diabetologia 2013; 56(10): 2203-12 6 Stoll L et al.: A circular RNA generated from an intron of the insulin gene controls insulin secretion. Nat Commun 2020; 11(1): 5611 7 Motterle A et al.: Identification of islet-enriched long non-coding RNAs contributing to beta-cell failure in type 2 diabetes. Mol Metab 2017; 6(11): 1407-18 8 Jacovetti C et al.: The mitochondrial tRNA-derived fragment, mt-tRF-Leu(TAA), couples mitochondrial metabolism to insulin secretion. Mol Metab 2024; 84: 101955 9 Xourafa G et al.: Inter-organ crosstalk during development and progression of type 2 diabetes mellitus. Nat Rev Endocrinol 2024; 20(1): 27-49 10 Brozzi F et al.: tRNA-derived fragments in T lymphocyte-beta cell crosstalk and in type 1 diabetes pathogenesis in NOD mice. Diabetologia 2024; 67(10): 2260-74 11 Guay C et al.: Lymphocyte-Derived Exosomal MicroRNAs Promote Pancreatic beta Cell Death and May Contribute to Type 1 Diabetes Development. Cell Metab 2019; 29(2): 348-61e6 12 Belgardt BF et al.: The microRNA-200 family regulates pancreatic beta cell survival in type 2 diabetes. Nat Med 2015; 21(6): 619-27 13 Regazzi R: MicroRNAs as therapeutic targets for the treatment of diabetes mellitus and its complications. Expert Opin Ther Targets 2018; 22(2): 153-60 14 Miyamoto N et al.: Advanced Nanotechnology-Based Nucleic Acid Medicines. Pharmaceutics 2024; 16(11): 1367 15 Guay C et al.: Circulating microRNAs as novel biomarkers for diabetes mellitus. Nat Rev Endocrinol 2013; 9(9): 513-21 16 Joglekar MV et al.: A microRNA-based dynamic risk score for type 1 diabetes. Nat Med 2025; 31(8): 2622-31
Das könnte Sie auch interessieren:
Études actuelles sur le traitement de l’ILD
Le terme pneumopathie interstitielle (ILD) est un terme générique désignant un groupe important et hétérogène de maladies qui se manifestent principalement dans l’espace broncho- ...
Mise à jour 2026: vers la modification de la maladie
Un grand nombre de médicaments biologiques immunomodulateurs et de «small molecules» ont considérablement élargi l’éventail des options thérapeutiques dans les maladies inflammatoires ...
Schémas thérapeutiques de référence plus courts dans la tuberculose
La tuberculose (TB) constitue toujours un défi majeur à l’échelle mondiale. Malgré les progrès, le besoin de schémas thérapeutiques plus efficaces, plus courts et mieux tolérés reste ...