Controverses en matière de diagnostic
Compte-rendu:
Dre Corina Ringsell
Rédactrice
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Les pneumopathies interstitielles (ILD) constituent un groupe hétérogène de maladies différentes. C’est pourquoi le diagnostic est complexe et comprend des aspects cliniques, radiologiques et histopathologiques qui doivent ensuite faire l’objet de discussions multidisciplinaires.1
Les ILD sont caractérisées par une atteinte de l’interstitium et/ou des alvéoles et/ou des bronchioles, et se distinguent par des critères cliniques, radiologiques et histopathologiques spécifiques. Une discussion d’experts a porté sur les examens pertinents.
Importance de l’imagerie
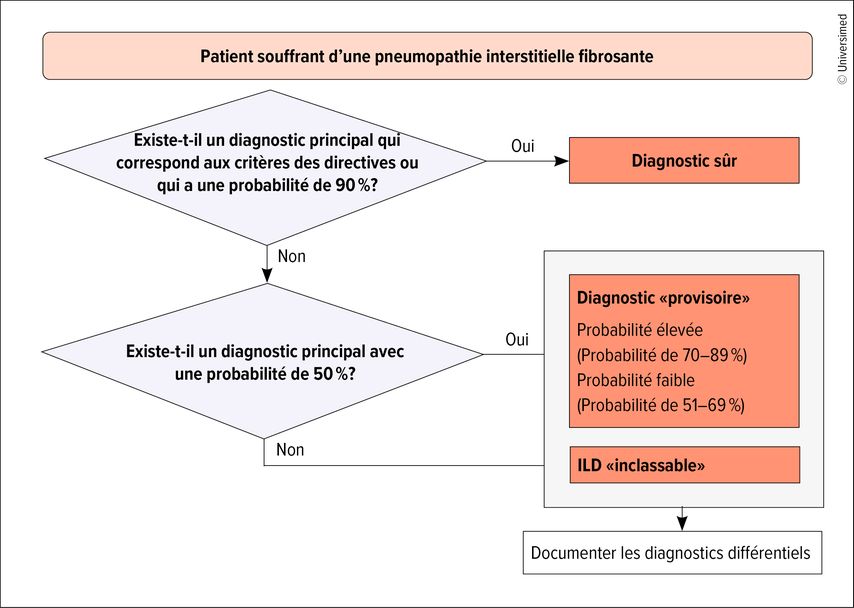
La Figure 1 montre un algorithme de sécurité diagnostique en cas d’«ILD», développé par un groupe de travail international.1Un diagnostic est considéré comme sûr en cas de probabilité de plus de 90%. Entre 50% et 90%, le diagnostic est provisoire; en dessous de 50%, on parle d’une ILD inclassable.
Fig.1: Sécurité diagnostique en cas de suspicion de pneumopathie interstitielle (ILD) (modifiée selon Ryerson CJ et al. 2017)1
La question est de savoir comment gérer un diagnostic provisoire et si l’imagerie peut confirmer le diagnostic. Le facteur limitant est l’interprétation par les évaluateurs. Pour une étude, 112 radiologues, dont 96 spécialistes en imagerie thoracique, ont examiné les tomodensitométries de 150 patients atteints de fibrose pulmonaire idiopathique (IPF) selon les critères des principales sociétés savantes. La concordance parfaite a été définie comme coefficient kappa κ=1, une concordance encore acceptable sur le plan clinique comme κ=0,4, ce qui n’a donné qu’une concordance modérée de 0,48 pour les radiologues en général et de 0,52 pour les spécialistes en imagerie thoracique ayant 10 à 20 ans d’expérience. Chez les radiologues ayant plus de 25 ans d’expérience, le coefficient κ était de 0,37 seulement.2 Une étude menée auprès de plus de 1100 pneumologues et 34 spécialistes de l’IPF dans plus de 100 pays a abouti à un résultat similaire. Ils ont évalué 60 cas d’ILD sur la base de résultats cliniques et d’images detomodensitométrie haute résolution (HRCT). Une fois encore, seule une concordance modérée a été observée, légèrement plus importante parmi les spécialistes de l’IPF que parmi les autres participants (κ=0,53 par rapport à 0,4).3 Les directives actuelles recommandent une biopsie pulmonaire dans les cas équivoques.4Une étude publiée en 2019 montre toutefois que, même lorsque le diagnostic n’est pas clair, on renonce souvent à la biopsie et on instaure un traitement antifibrotique dès lors que la probabilité d’une IPF est évaluée à au moins 70%.5
Un meilleur diagnostic grâce à la TBLC?
Un groupe de travail dirigé par Jürgen Hetzel, de Bâle, a cherché à savoir si la cryobiopsie transbronchique (TBLC) pouvait constituer une alternative à la biopsie chirurgicale. Les données de 128 patients chez lesquels un comité multidisciplinaire (cliniciens, radiologues, pathologistes) a suspecté une pneumonie interstitielle idiopathique ont été analysées. L’évaluation s’est déroulée en quatre étapes: (1) résultats cliniques et radiologiques, (2) plus lavage bronchoalvéolaire (BAL), (3) plus résultats de TBLC et, si disponibles, (4) résultats de biopsie pulmonaire. La TBLC a augmenté significativement le pourcentage de diagnostics fiables (c.-à-d. ≥70% de probabilité) de 60 jusqu’à 81%.6 Reste à savoir à partir de quel seuil une biopsie doit être prescrite: en dessous de 70 ou de 90%. Cela dépend notamment de l’âge et de l’état de santé des patients, ainsi que du risque de complications associé.5 En outre, la technique de biopsie joue un rôle. Le risque le plus élevé est celui de la biopsie chirurgicale, avec un taux de mortalité de 1,7 par rapport à environ 0,2% pour la TBLC. Chez les hommes âgés de plus de 74 ans présentant des comorbidités, le risque de décès à la suite d’une biopsie chirurgicale augmente même jusqu’à 10%.7 La TBLC est supérieure à la biopsie chirurgicale en termes de risque, mais pas en termes de résultats pathologiques et histologiques. C’est là que la biopsie chirurgicale est supérieure. Une étude australienne a révélé qu’il n’y avait toutefois plus de différence significative si l’on combinait la TBLC avec d’autres données cliniques et radiologiques.8 Une TBLC et une biopsie chirurgicale ont été réalisées chez des patients chez qui une discussion au sein d’un comité multidisciplinaire avait laissé supposer le bénéfice d’une biopsie. Les résultats ont été concordants dans environ 70% des cas. Le problème est que les prélèvements de TBLC sont plus petits que ceux de biopsie chirurgicale. Par conséquent, les résultats peuvent être moins clairs et la sécurité diagnostique inférieure.8 Les directives communes de l’American Thoracic Society, de l’European Respiratory Society, de la Japanese Respiratory Society et de l’Asociación Latinoamericana de Tórax stipulent que la TBLC peut être privilégiée à la biopsie chirurgicale dans certaines conditions. Elle doit toutefois uniquement être réalisée dans des centres expérimentés et chez des patients appropriés. Dans les cas équivoques, une biopsie chirurgicale doit être effectuée.9,10
Quand une biopsie est-elle pertinente et nécessaire?
La biopsie n’est pas pertinente si la cause de l’ILD fibrosante est connue ou en cas de maladie concomitante, par exemple une maladie du tissu conjonctif ou une polyarthrite rhumatoïde confirmée. Il n’est pas non plus nécessaire de pratiquer une biopsie en cas de modèle clair ou probable de pneumonie interstitielle commune (UIP) à l’HRCT.9 Inversement, seuls environ 50% des cas diagnostiqués histologiquement comme une UPI présentent un modèle clair d’UIP à l’HRCT. Avant de prescrire une biopsie, il est toutefois important de prendre en compte la sécurité diagnostique et d’évaluer dans quelle mesure une biopsie peut l’améliorer. Il faut aussi tenir compte du risque de l’intervention. S’il est très élevé, la biopsie ne doit pas être réalisée.11 Cela est particulièrement vrai pour les patients en soins intensifs et en présence de facteurs de risque tels qu’un âge avancé, une multimorbidité, une oxygénothérapie en cours, une faible capacité de diffusion et une hypertension pulmonaire.7
Bien qu’elle présente globalement un risque plus faible, la TBLC n’est pas sans risque. Ainsi, le risque d’hémorragie est d’environ 30%, bien que les hémorragies sévères soient rares. Un pneumothorax se produit dans moins de 10% des cas. D’autre part, les risques d’exacerbation aiguë et de mortalité à 30 jours sont moins élevés en cas de TBLC que de biopsie chirurgicale.12,13
Alternatives à la biopsie
Avant de prescrire une biopsie, il faut avoir épuisé toutes les autres options diagnostiques, en particulier les méthodes non invasives comme l’auscultation pulmonaire. La collaboration avec le service de rhumatologie peut fournir de précieuses indications, par exemple la détermination des anticorps antinucléaires (ANA) par coloration. La capillaroscopie peut indiquer une sclérose systémique et d’autres maladies du tissu conjonctif. En cas de suspicion de myosite, une IRM permet de clarifier les résultats incertains.14
Biomarqueurs de la sarcoïdose
Bien que la pathogenèse de la sarcoïdose soit bien définie, le traitement des antigènes joue un rôle qui déclenche la réponse immunitaire à médiation cellulaire, entraînant une inflammation, la formation de granulomes, puis finalement la fibrose. Le diagnostic est posé à l’aide de l’imagerie, de la biopsie et de l’exclusion d’autres maladies granulomateuses. En raison de la pathogenèse, différents biomarqueurs sont également proposés. Il s’agit notamment du récepteur de l’IL-2 comme marqueur de l’activation des lymphocytes T, des marqueurs de l’activation des macrophages comme la chitotriosidase (CHIT1) et de nouveaux candidats comme l’activation de la voie JAK-STAT.15 La CHIT1 est en corrélation avec l’activité de la maladie, la sévérité et la dissémination multi-organes. Les taux sont réduits par l’administration de corticoïdes, mais augmentent à nouveau en cas de récidive. Des taux élevés sont également associés à une progression de la maladie dans les deux à cinq ans.16 Lors de l’interprétation, il faut toutefois tenir compte du fait qu’il existe un polymorphisme génétique. Environ 5% de la population présentent un taux de CHIT1 nul, car ces personnes sont homozygotes pour cette mutation, les autres présentant des taux différents. Pour interpréter correctement les taux de CHIT1, les patients doivent donc subir un génotypage.17En dehors de cela, il existe des biomarqueurs de l’atteinte et des lésions organiques, comme l’interleukine 6 (IL-6) pour les lésions externes diffuses ou la troponine et le NT-proBNP pour le cœur.15
Aucun marqueur, même en combinaison avec d’autres, ne permet cependant de poser un diagnostic clair de sarcoïdose. Il en va de même pour la détection des granulomes. Là encore, plusieurs diagnostics différentiels sont possibles.18 Autre problème avec les biomarqueurs proposés: l’absence quasi totale de validation externe des études publiées à ce sujet. Tous ces biomarqueurs sont des éléments normaux de la réponse inflammatoire et immunitaire dans la sarcoïdose, mais ils ne sont pas spécifiques à la sarcoïdose. Ils sont également détectables dans d’autres réactions inflammatoires. C’est pourquoi les directives européennes et américaines actuellement en vigueur ne recommandent aucun biomarqueur.19
Il existe donc un besoin de biomarqueurs pour le diagnostic tout comme le traitement afin d’éviter un surtraitement ainsi que la morbidité liée aux médicaments qui en découle.20
Source:
Controversies in the diagnosis & classification of Interstitial Lung Disease – Pro-Con Debate: «Interstitial Lung Disease – to (cryo)biopsy or not to biopsy? – Pro», exposé du Pr Jürgen Hetzel, Bâle; «Interstitial Lung Disease – to (cryo)biopsy or not to biopsy? – Contra», exposé de la Pre Sabina Guler, Berne; «Sarcoidosis – are lab biomarkers any good? – Pro», exposé du Pr Martin H. Brutsche, Saint-Gall; «Sarcoidosis – are lab biomarkers any good? – Contra», exposé du Dr Romain Lazor, Lausanne. Congrès annuel de la Société Suisse de Pneumologie, du 15 au 16 mai 2025, à Genève
Littérature:
1 Ryerson CJ et al: Am J Respir Crit Care Med 2017; 196: 1249-54 2 Walsh SLF et al.: Thorax 2016; 71: 45-51 3 Walsh SLF et al.: Eur Respir J 2017; 50: 1700936 4 Raghu G et al.: Am J Respir Crit Care Med 2018; 198: e44-68 5 Walsh SLF et al.: Am J Respir Crit Care Med 2019; 200: 1146-53 6 Hetzel J et al.: Eur Respir J 2020; 56: 1901520 7 Hutchinson JP et al.: Am J Respir Crit Care Med 2016; 193: 1161-7 8 Troy LK et al.: Lancet Respir Med 2020; 8: 171-81 9 Raghu G et al.: Am J Respir Crit Care Med 2022; 205: e18-47 10 Korevaar DA et al.: Eur Respir J 2022; 60: 2200425 11 Guler SA, Ryerson CJ: Minerva Pneu 2017; 56: 25-32 12 Rodrigues I et al.: Eur Respir Rev 2022; 31: 210280 13 Kheir F et al.: Ann Am Thorac Soc 2022; 19: 1193-202 14 Guler SA et al.: Chest 2024; 166: 352-61 15 Drent M et al.: N Engl J Med 2021; 385: 1018-32 16 Bennett D et al.: Respir Res 2020; 21: 617 Csongrádi A et al.: Clin Chim Acta 2021; 513: 50-6 18 Judson MA: F1000Prime Rep 2014; 6: 89 19 Kraaijvanger R et al.: Front Immunol 2020; 11: 1443 20 Pohle S et al.: PLoS One 2016; 11: e0151940
Das könnte Sie auch interessieren:
Études actuelles sur le traitement de l’ILD
Le terme pneumopathie interstitielle (ILD) est un terme générique désignant un groupe important et hétérogène de maladies qui se manifestent principalement dans l’espace broncho- ...
Mise à jour 2026: vers la modification de la maladie
Un grand nombre de médicaments biologiques immunomodulateurs et de «small molecules» ont considérablement élargi l’éventail des options thérapeutiques dans les maladies inflammatoires ...
Schémas thérapeutiques de référence plus courts dans la tuberculose
La tuberculose (TB) constitue toujours un défi majeur à l’échelle mondiale. Malgré les progrès, le besoin de schémas thérapeutiques plus efficaces, plus courts et mieux tolérés reste ...