Oxygénothérapie à haut débit: quand et quelle durée?
Compte-rendu:
Dre Corina Ringsell
Rédactrice
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
L’oxygénothérapie à haut débit (OHD) peut améliorer la fraction inspirée en oxygène (FiO2). Elle a un effet dynamique sur la pression expiratoire positive (PEP), réduit le travail respiratoire ainsi que l’espace mort, et améliore la clairance mucociliaire, ce qui est l’effet le plus important pour le traitement à domicile.1–3 Mais pour quels patients cetraitement est-il approprié?
L’OHD à domicile convient à tous les patients pour lesquels une indication a été démontrée dans des études correspondantes. La plupart des preuves concernent la bronchopneumopathie chronique obstructive (BPCO), mais il existe également des études portant sur la bronchectasie et la pneumopathie interstitielle (ILD).
Oxygénothérapie à long terme en cas de BPCO
Une étude danoise menée en 2018 sur 200 patients atteints de BPCO stable et recevant une oxygénothérapie à long terme (OLT) à domicile. Ils présentaient une PaCO2 médiane de 6,5kPa et une médiane de trois exacerbations par an. Ils ont été randomisés pour recevoir l’oxygénothérapie de référence ou l’oxygénothérapie plus OHD par canule nasale à haut débit (CNHD). L’étude a duré un an. L’OHD a été administrée environ six heures par jour, le plus souvent la nuit. Le débit de 20l/min pour l’OHD était inférieur aux débits observés à l’hôpital, mais comparable à d’autres études portant sur l’OHD à domicile. Il en va de même pour le débit d’oxygène de 1,8l/min.
Il s’est avéré que les exacerbations de la BPCO ont considérablement diminué dans le groupe utilisant une CNHD par rapport au groupe de contrôle (3/an par rapport à 5/an; p<0,001). Le score de dyspnée s’est amélioré, tout comme la PaCO2 (–0,4kPa; p=0,005) et la distance parcourue au test de marche de 6 minutes (+30m; p=0,005), ce qui a également amélioré la qualité de vie liée à la santé d’une manière générale. En revanche, le nombre d’hospitalisations était identique dans les deux groupes.4
Une méta-analyse des études comparatives antérieures menées sur un total de 440 patients atteints de BPCO avec/sans OHD montre que l’OHD réduit le nombre d’exacerbations aiguës par rapport à l’OLT de référence (RR: 0,77; IC à 95%: 0,66–0,89) et peut diminuer la fréquence des hospitalisations (RR: 0,87; IC à 95%: 0,69–1,09).5 Le mécanisme sous-jacent est probablement l’amélioration de la clairance mucociliaire. Sur la base de ces données, les exacerbations fréquentes de la BPCO sont désormais de plus en plus reconnues comme une indication pour l’OHD à domicile. Quatre essais randomisés contrôlés portant sur l’OHD à domicile sont actuellement en cours, ce qui nous permettra d’obtenir des données supplémentaires à ce sujet.
CNHD par rapport à VNI: les résultats des études
De nombreuses études ont examiné l’utilisation de la CNHD en cas d’exacerbation aiguë de la BPCO (EA-BPCO) et si, et selon quels critères, elle peut être utilisée comme alternative à la ventilation non invasive (VNI).
Une étude italienne a porté sur 79 patients présentant une EA-BPCO légère à modérée (pH sanguin: 7,25–7,35; PaCO2: ≥55mmHg avant assistance respiratoire). Le critère d’évaluation primaire de cette étude de non-infériorité était la réduction de la PaCO2 dans les deux heures, les principaux critères d’évaluation secondaires étant la réduction de la PaCO2 dans les six heures et le taux de changement de traitement. Le volume d’air a été réglé à 60l/min et la température de l’air à 37 degrés. Avec des valeurs initiales de PaCO2 >70mmHg en moyenne dans les deux groupes, la CNHD a permis de réduire la PaCO2 de 6,8mmHg (+/-8,7) après deux heures, par rapport à9,5mmHg (+/-8,5) pour la VNI. La différence n’était pas statistiquement significative (p=0,404). Cependant, après six heures, 32% des patients du groupe utilisant une CNHD étaient passés à la VNI et une personne était passée sous ventilation invasive.6
Plusieurs méta-analyses n’ont trouvé aucune différence significative entre la VNI et la CNHD en termes de mortalité, de nécessité d’intubation ou de durée de séjour en soins intensifs.7–9
L’une des rares études dont le résultat était négatif incluait 225 patients souffrant d’hypercapnie sévère (PaCO2: 63mmHg ou 61mmHg). Le critère d’évaluation primaire était le taux d’échec thérapeutique, défini comme l’intubation endotrachéale ou le passage à une autre méthode de traitement à l’étude. Les critères d’évaluation secondaires étaient les taux d’intubation ou de changement de traitement, les valeurs de l’analyse des gaz du sang, les signes vitaux à 1, 12 et 48 heures, la mortalité à 28 jours ainsi que la durée de séjour en soins intensifs et la durée d’hospitalisation. Un échec thérapeutique a été observé chez 25,7% des patients du groupe utilisant une CNHD et 14,3% des patients du groupe sous VNI. Le taux d’intubation était également plus élevé dans le groupe utilisant une CNHD (14,2 par rapport à 5,4%, p=0,026). Aucune différence statistiquement significative n’a été observée pour les autres critères d’évaluation.10
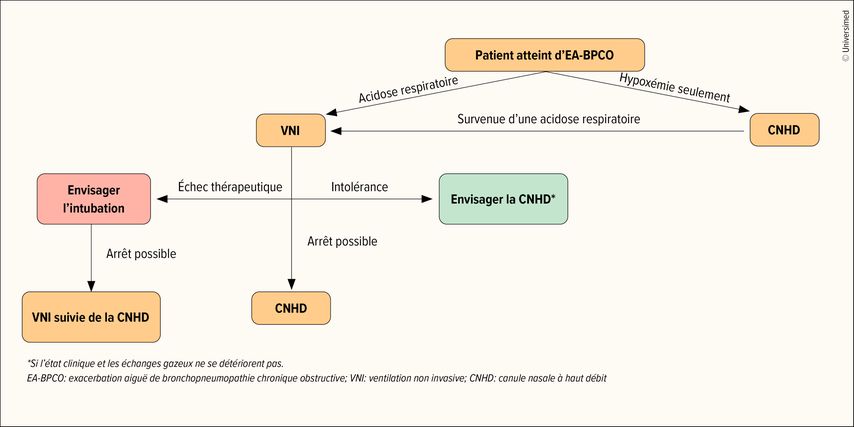
Une recommandation de 2022 stipule que la VNI reste le traitement de référence en cas d’acidose respiratoire. La CNHD est le traitement de référence en l’absence d’acidose respiratoire. Elle peut en outre être envisagée si la VNI n’est pas tolérée. En cas d’échec de la VNI, l’intubation doit être envisagée. Dès que l’intubation et la VNI ne sont plus nécessaires, il est également possible de passer à une CNHD (Fig.1).11
Fig.1: Algorithme pour l’utilisation potentielle de la CNHD chez les patients atteints d’EA-BPCO (modifiée selon Bruni A et al. 2022)11
OHD en cas de bronchectasies
Les preuves sont limitées à ce sujet, car il n’existe qu’un seul essai randomisé contrôlé. Il a inclus 108 patients stables, dont deux tiers étaient atteints de BPCO et un tiers de bronchectasie. Ils devaient présenter plus de deux exacerbations par an et ont été randomisés pour recevoir le traitement de référence ou le traitement à haut débit utilisant une CNHD. Le traitement par CNHD n’a été utilisé que la journée et pendant environ deux heures seulement. Le résultat portait sur l’ensemble de la population atteinte de BPCO et de bronchectasie. Dans le groupe utilisant une CNHD, on a constaté un allongement significatif du délai jusqu’à la première exacerbation (52 par rapport à 27 jours; p=0,05), une réduction du taux d’exacerbation (2,97 par rapport à 3,63; p=0,067) et une diminution du nombre de jours d’exacerbation par an (18,2 par rapport à 33,5; p=0,045). Si l’on considère uniquement la population atteinte de bronchectasie (n=45), une réduction du taux d’exacerbation et une amélioration significative de la qualité de vie associée ont également été décrites.12
Une étude cas-témoins rétrospective portant sur la bronchiectasie et menée en Italie auprès de 40 patients atteints de bronchiectasie a révélé une diminution significative du nombre d’exacerbations en l’espace d’un an et d’hospitalisations. De plus, une légère amélioration de la fonction pulmonaire a été constatée.13
OHD en cas d’ILD
Les données sont encore plus limitées pour l’ILD. Actuellement, il n’existe qu’une très petite étude crossover randomisée, contrôlée portant sur neuf patients atteints d’ILD. Elle a mis en évidence que l’OHD avait entraîné un allongement statistiquement et cliniquement significatif de la distance parcourue au test de marche de 6 minutes ainsi qu’une réduction du temps de récupération de la saturation après le test de marche. Cependant, aucune amélioration de la qualité de vie liée à la santé n’a été constatée en ce qui concerne la dyspnée ou la qualité du sommeil.14
Durée de l’oxygénothérapie
Les objectifs de l’oxygénothérapie sont de corriger l’hypoxémie et d’améliorer les paramètres physiologiques afin d’augmenter les performances physiques, d’améliorer les fonctions cognitives, de réduire les comorbidités cardiovasculaires et le taux d’hospitalisation. L’objectif principal est toutefois d’améliorer la qualité de vie liée à la santé et de diminuer la mortalité.
L’OLT est uniquement indiquée en cas d’hypoxémie sévère, définie par une PaO2 <56mmHg ou une PaO2 <60mmHg associée à une polycythémie (Ht >54%) ou à un cœur pulmonaire. En cas d’hypoxémie modérée, elle ne réduit ni le taux d’hospitalisation ni le taux de mortalité. La qualité de vie liée à la santé n’est pas améliorée et la progression vers une hypoxémie sévère n’est pas empêchée.15
Les directives européennes et américaines actuellement en vigueur recommandent une utilisation d’au moins 15 heures par jour.16–18
Défis
Le suivi du traitement constitue l’un des défis principaux. Les données du registre danois de l’oxygénothérapie montrent que seuls environ 40% des patients ont été suivis après l’initiation de l’oxygénothérapie. Ce suivi était principalement effectué lorsque le traitement avait été initié par un pneumologue et qu’il existait une prescription très claire de la durée nécessaire de l’oxygénothérapie. Cette étude a également révélé que la moitié des patients ne recevaient aucune prescription concernant la durée de l’oxygénothérapie.19 L’observance est un autre défi: dans une étude canadienne, seuls 60% des patients ont déclaré utiliser l’oxygénothérapie plus de 15 heures par jour. Dans ce contexte, l’observance est notamment liée à la mobilité. Les patients plus âgés sont plus susceptibles d’observer le traitement, car ils ne quittent pas leur domicile. Les dispositifs d’oxygénothérapie de déambulation améliorent également l’observance du traitement.20 De plus, le traitement s’accompagne de contraintes pour les patients, par exemple de troubles locaux comme la sécheresse des muqueuses, les saignements de nez et les inflammations de la peau. Ils font face à des désagréments en contexte social du fait que les dispositifs sont souvent très bruyants. Une étude coréenne a examiné ces barrières sociales et a conclu que 50% des patients avaient peur de devoir utiliser les dispositifs à long terme, 40% craignaient d’attirer involontairement l’attention ou pensaient ne pas avoir besoin d’oxygène. 20% des patients pensaient que l’oxygène était nocif pour eux.
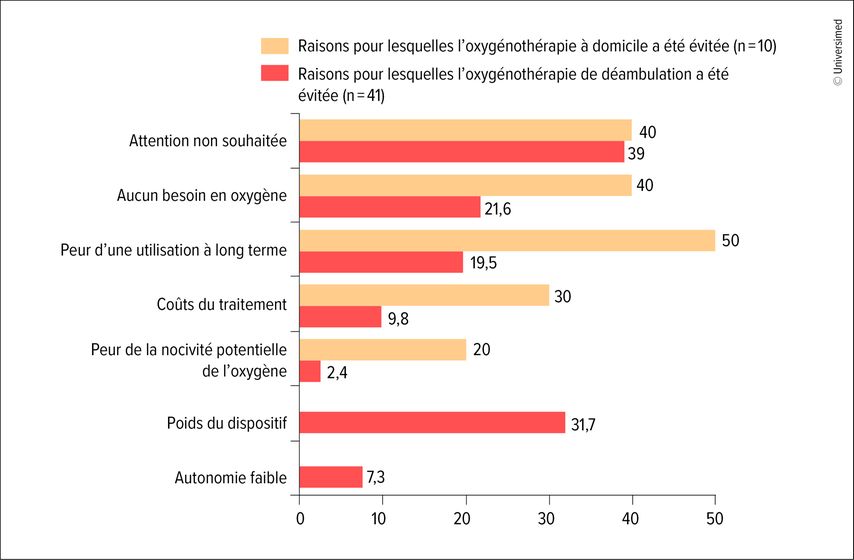
Parmi les patients qui utilisaient des dispositifs mobiles, beaucoup se sont plaints que les dispositifs étaient trop lourds, que l’autonomie était trop faible et que le débit ne pouvait pas être adapté à leurs besoins (Fig.2). Il est donc important d’expliquer aux patients pourquoi l’oxygénothérapie est nécessaire et à quoi elle sert.21Un aspect essentiel est le coût. Environ 30% des patients sont préoccupés par le coût de leur traitement. Une analyse de la base de données de santé française montre que les coûts de prise en charge des patients présentant une oxygénodépendance sont principalement liés aux hospitalisations et non pas tant au coût de l’oxygène même. Le taux de survie des patients ayant un dispositif mobile est plus élevé que celui des patients ayant un concentrateur fixe.22
Fig.2: Raisons pour lesquelles les patients n’ont pas observé l’oxygénothérapie selon la prescription, en% (modifiée selon Kim HJ et al. 2024)21
En fin de compte, la technologie doit être adaptée aux besoins des patients en termes de mobilité et de débit d’oxygène. Il convient de vérifier régulièrement si le traitement est réellement observé et s’il améliore la qualité de vie des patients.
Source:
«Optimal duration of oxygen therapy», exposé de la Dre méd. Maura Prella, Lausanne; «HFOT in AE-BPCO, according to which criteria should it be used alternately with NIV?», exposé du Pr Dr méd. Jean-Paul Janssens, Genève; «HF(O)T at home - for which patients and how can we implement it in Switzerland?», exposé du Dr méd. Grégoire Gex, Sion. Congrès annuel de la Société Suisse de Pneumologie, du 15 au 16 mai 2025, à Genève
Littérature:
1 Mündel T et al.: J Appl Physiol 2013; 114(8): 1058-65 2 Möller W et al.: J Appl Physiol 2017; 122(1): 191-7 3 Hasani A et al.: Chron Respir Dis 2008; 5(2): 81-6 4 Storgaard LH et al.: Int J Chron Obstruct Pulmon Dis 2018; 13: 1195-205 5 Pitre T et al.: Respir Med 2023; 219: 107420 6 Cortegiani A et al.: Crit Care 2020; 24(1): 692 7 Yang PL et al.: Heart Lung 2021; 50(2): 252-61 8 Feng Z et al.: Int J Chron Obstruct Pulmon Dis 2022: 17: 1987-99 9 Du Y et al.: Can Respir J 2023; doi: 10.1155/2023/7707010 10 Tan D et al.: Crit Care 2024; 28(1): 250 11 Bruni A et al.: Healthcare (Basel) 2022; 10(3): 536 12 Rea H et al.: Respir Med 2010; 104(4): 525-33 13 Crimi C et al.: J Clin Med 2022; 11(24): 7323 14 Weinreich UM et al: Chron Respir Dis 2022; 19: 14799731221137085 15 Lacasse Y et al.: Lancet Respir Med 2022; 10(11): 1029-37 16 Haidl P et al.: S2k-Leitlinie Langzeit-Sauerstofftherapie. AWMF-Registernummer 020-002 17 Jacobs SS et al.: Am J Respir Crit Care Med 2020; 202(10): e121-41 18 Hardinge M et al.: Thorax 2015; 70(6): 589-91 19 Ringbaek TJ et al.: J Intern Med 2001; 250(2): 131-6 20 Gauthier A et al.: Chron Respir Dis 2019; 16: 1479972318767724 21 Kim HJ et al.: Tuberc Respir Dis (Seoul) 2024; 87(1): 100-14 22 Glezer S et al.: Pulm Ther 2024; 10(2): 237-62; Correction: 263-5
Das könnte Sie auch interessieren:
Études actuelles sur le traitement de l’ILD
Le terme pneumopathie interstitielle (ILD) est un terme générique désignant un groupe important et hétérogène de maladies qui se manifestent principalement dans l’espace broncho- ...
Mise à jour 2026: vers la modification de la maladie
Un grand nombre de médicaments biologiques immunomodulateurs et de «small molecules» ont considérablement élargi l’éventail des options thérapeutiques dans les maladies inflammatoires ...
Schémas thérapeutiques de référence plus courts dans la tuberculose
La tuberculose (TB) constitue toujours un défi majeur à l’échelle mondiale. Malgré les progrès, le besoin de schémas thérapeutiques plus efficaces, plus courts et mieux tolérés reste ...