La nouvelle directive KDIGO sur l’ADPKD
Compte-rendu:
Dre Corina Ringsell
Rédactrice
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
En janvier 2025, l’organisation KDIGO (Kidney Disease: Improving Global Outcomes) a publié pour la première fois une directive claire sur le diagnostic et le traitement de la polykystose rénale autosomique dominante («autosomal dominant polycystic kidney disease», ADPKD).1 Lors du forum d’expert·es FOMF Update Nephrologie, le Dr méd. Christian Kuhn, médecin chef de clinique mbF, Hôpital cantonal de St-Gall, HOCH Health Ostschweiz, a expliqué les principales recommandations.
L’ADPKD est la maladie rénale monogénique la plus fréquente, qui peut entraîner une insuffisance rénale. La prévalence est d’environ 1:1000. Selon C. Kuhn, environ 10000 personnes sont concernées en Suisse et environ 12 millions dans le monde. L’ADPKD est due à des mutations génétiques, des gènes PKD1 et PKD2 dans 90% des cas. Si l’un des parents est atteint, les enfants ont une probabilité de 50% de développer la maladie en raison du mode de transmission autosomique dominant. De plus, l’ADPKD a une très forte pénétrance, ce qui signifie qu’elle se déclarera presque à coup sûr en cas de transmission. Environ 20% des personnes concernées présentent une nouvelle mutation sans anamnèse familiale positive.1
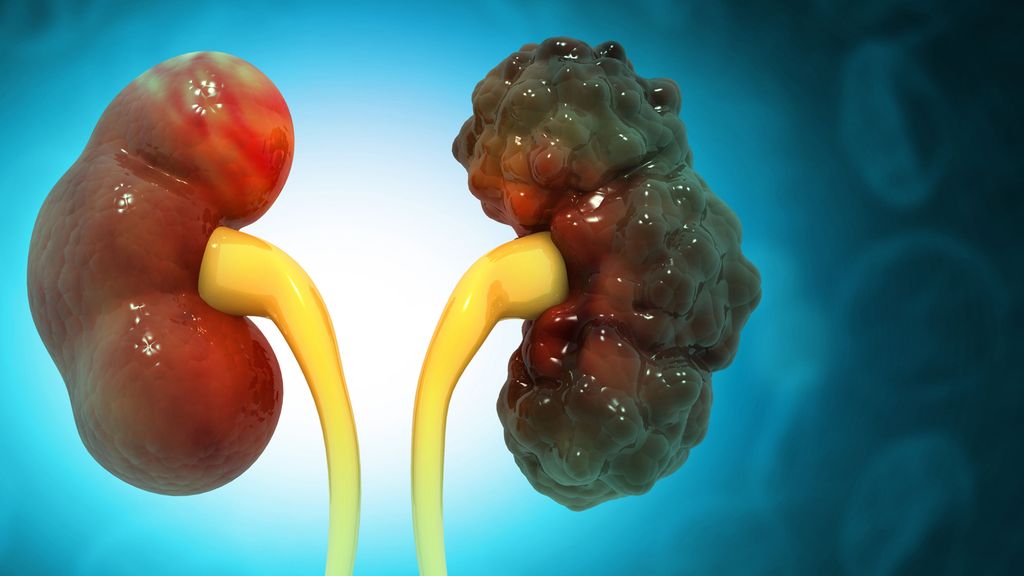
L’ADPKD entraîne le développement progressif de multiples kystes dans les deux reins, qui prennent la place du tissu rénal normal (Fig.1). Il en résulte une perte de fonction progressive, qui peut aller jusqu’à la nécessité d’une suppléance rénale. L’ADPKD peut également avoir des manifestations extrarénales, par exemple les kystes hépatiques et les anévrismes cérébraux sont fréquents.1
Procédure diagnostique
En ce qui concerne le diagnostic, la question se pose de savoir si une personne ayant des antécédents familiaux d’ADPKD souhaite réellement savoir si elle est atteinte, a déclaré C. Kuhn. Si un dépistage est souhaité, la première étape diagnostique est l’échographie. Il s’agit d’évaluer le nombre de kystes rénaux en fonction de critères diagnostiques liés à l’âge afin de confirmer l’ADPKD.1
Si les résultats de l’échographie ne sont pas clairs, il est possible de recourir à l’imagerie par résonance magnétique (IRM), qui permet également de visualiser de très petits kystes. Si la mutation familiale est connue, il est également possible de procéder à une analyse de ségrégation ciblée de cette mutation spécifique.1 Des examens complémentaires sont recommandés chez les adultes chez qui des kystes rénaux ou hépatiques sont détectés par hasard lors d’une échographie, mais qui n’ont pas d’antécédents familiaux ou pas d’antécédents familiaux connus.1
C. Kuhn a souligné que, en cas de présentation clinique typique d’une ADPKD, une analyse génétique négative ou peu claire n’exclut pas une forme héréditaire de la maladie. Les personnes à risque doivent être traitées de la même manière que les personnes atteintes d’ADPKD confirmée.
Facteurs pronostiques
Les mutations PKD1 et PKD2 sont défavorables en termes de pronostic.1 La première est associée à des évolutions plus sévères de la maladie et conduit à la nécessité d’une suppléance rénale en moyenne environ 20 ans plus tôt par rapport à la deuxième, a expliqué C. Kuhn. D’autres facteurs pronostiques défavorables sont le sexe masculin, l’obésité, un apport calorique et un apport en sel élevés, ainsi qu’une fonction rénale déjà réduite ou un volume rénal total élevé.1
Afin de prédire la détérioration de la fonction rénale et la survenue d’une insuffisance rénale, la directive recommande d’utiliser la classification de Mayo pour l’imagerie. Pour ce faire, il faut déterminer le volume rénal total, qui doit être saisi dans un outil en ligne ( www.mayo.edu/research/documents/pkdcenter-adpkd-classification/doc-20094754 ), avec la taille et l’âge de la personne. Ce dernier calcule le volume rénal total ajusté en fonction de la taille (htTKV), qui indique le volume rénal en millilitres par mètre d’une personne. Le résultat est classé en fonction de l'âge de 1A à 1E selon la classification de Mayo, une classe supérieure indiquant une détérioration plus rapide de la fonction rénale et une insuffisance rénale plus précoce. La classification de Mayo n’est validée que pour l’ADPKD «typique» (classe 1) ainsi que pour les mutations PKD1 et PKD2.1 Sont considérés comme «typiques» les kystes rénaux bilatéraux et diffus qui traversent complètement les deux reins; les formes atypiques (classe 2) sont par exemple une atteinte unilatérale, segmentaire ou très asymétrique.
Manifestations de l’ADPKD
Hypertension artérielle
La manifestation clinique la plus fréquente et la plus précoce de l’ADPKD est l’hypertension artérielle, qui survient généralement avant 30 ans. Chez les patient·es âgés de 18 à 49 ans atteint·es de maladie rénale chronique (MRC) aux stades 1 et 2 (DFGe >60ml/min/1,73m2) et de pression artérielle élevée (>130/85mmHg), il convient de viser un objectif de pression artérielle <110/75mmHg (en automesure à domicile), à condition qu’il soit toléré.1 Pour les patient·es de ce groupe d’âge dont la pression artérielle se situe entre 110/75mmHg et 130/85mmHg, la directive ne fait pas de recommandation, car les données disponibles sont insuffisantes. Il existe toutefois un point pratique qui conseille une approche individualisée basée sur une prise de décision partagée avec les patient·es.1 Pour les personnes âgées de plus de 50 ans, une pression artérielle systolique cible moyenne <120mmHg est proposée, indépendamment du stade de la MRC (mesure standardisée de la pression artérielle). Si un traitement médicamenteux est indiqué, un inhibiteur de l’ECA ou un sartan est recommandé en premier lieu.1
Douleurs rénales chroniques et infections urinaires
Des douleurs chroniques au niveau du flanc, de l’abdomen et des lombaires surviennent fréquemment. Dans ce cas, il faut exclure des diagnostics différentiels tels qu’une sténose du canal rachidien. Si les douleurs sont liées à l’ADPKD, il est toutefois préférable qu’elles soient traitées par une équipe inter-/multidisciplinaire. Les traitements vont de mesures non invasives, telles que des applications de chaleur, à des mesures de plus en plus invasives, jusqu’à la néphrectomie, lorsque toutes les autres options ont échoué.1
Les calculs rénaux sont également une complication fréquente, qui se traite de la même manière que pour la population en bonne santé: il faut conseiller aux personnes concernées d’augmenter leur consommation d’eau et les informer des facteurs de risque tels que l’obésité et le diabète. Si possible, une analyse des calculs et des facteurs prolithogènes doit être effectuée.1
Les infections urinaires sont généralement traitées de la même manière que pour la population en bonne santé. Si un·e patient·e atteint·e d’ADPKD présente de la fièvre, des douleurs au niveau de l’abdomen ou du flanc et des taux élevés de CRP, il faut toutefois envisager une infection du kyste.1 En général, une forte suspicion suffit pour initier un traitement antibiotique, a déclaré C. Kuhn. Selon les directives, il doit de préférence comprendre un antibiotique soluble dans les lipides comme la ciprofloxacine ou le sulfaméthoxazole/triméthoprime et être pris pendant quatre à six semaines.1
Insuffisance rénale progressive et suppléance rénale
En général, la prise en charge de la MRC dans l’ADPKD ne diffère pas de celle des autres maladies rénales, a expliqué l’intervenant. Seule exception importante: les inhibiteurs du SGLT2 ne sont pas recommandés – du moins pour le moment – en cas d’ADPKD, car la maladie était un critère d’exclusion dans les études de grande envergure portant sur ces substances, a souligné C. Kuhn. La méthode de suppléance rénale de référence est la transplantation rénale.1 Un point nouveau et passionnant est que le poids estimé des kystes rénaux et du foie kystique doit être déduit du poids de la personne, surtout si le centre de transplantation a une limite d’IMC pour la transplantation, a déclaré l’intervenant.
Retarder la progression de la maladie
Pour retarder la progression de la maladie, il est possible d’inhiber l’action de l’hormone antidiurétique sur le récepteur de l’ADH dans les reins. Le médicament le plus étudié à cet effet et recommandé dans la directive est le tolvaptan.1 Il a une influence positive sur la diminution du DFG et retarde l’augmentation du volume rénal total (VRT). Dans les études, il a également réduit significativement l’incidence des infections urinaires, des calculs rénaux, de l’hématurie et des douleurs rénales par rapport au placebo.2,3 Les principaux effets secondaires sont des conséquences de l’inhibition de la réabsorption d’eau dans les tubules rénaux, entre autres la soif, la polyurie et la nycturie. En outre, une atteinte hépatique peut survenir, raison pour laquelle les transaminases et la bilirubine doivent être surveillées tous les mois avant et pendant les 18 premiers mois du traitement, puis tous les trois mois. En cas de signes d’atteinte hépatique, le traitement doit être interrompu.1 Selon les directives, le tolvaptan est indiqué en cas de DFGe ≥25ml/min/1,73m2 et de risque élevé de progression rapide de la maladie, défini par la classe de Mayo ou la documentation d’une diminution rapide du DFG ≥3ml/min/1,73m2 par an.1
Conditions préalables en Suisse
C. Kuhn a souligné qu’une garantie de prise en charge des coûts doit toujours être demandée avant le début du traitement en Suisse. Les coûts sont uniquement pris en charge pour les adultes atteints d’ADPKD «typique» (classe 1), qui présentent une MRC de stade 1–3 (DFGe ≥30ml/min/1,73m2). Le volume rénal total (VRT) doit être d’au moins 750ml et, si le DFGe est ≥90ml/min/1,73m2, la classe Mayo 1D ou 1E pour que le traitement soit remboursé.4 Si le DFGe est compris entre 30 et 90ml/min/1,73m2, la classe Mayo 1C est suffisante, a précisé l’intervenant. La prescription et la surveillance du traitement doivent en outre être effectuées par des néphrologues exerçant dans un hôpital défini par l’OFSP.4
Autres interventions
La directive KDIGO déconseille actuellement les autres mesures visant à retarder la progression de la maladie, comme les inhibiteurs de mTOR, la metformine, les inhibiteurs du SGLT2 ou un régime cétogène. Une mesure proposée, avec un faible niveau de preuve, est d’augmenter l’apport quotidien en eau à au moins deux ou trois litres.1 Cela doit permettre de réduire la libération d’ADH et donc de freiner la croissance des kystes. Les données disponibles sont toutefois limitées, a expliqué C. Kuhn.
Source:
Forum d’expert·es FOMF Update Nephrologie, 6 mars 2025, en ligne
Littérature:
1 KDIGO ADPKD Work Group: KDIGO 2025 Clinical Practice Guideline for the Evaluation, Management, and Treatment of Autosomal Dominant Polycystic Kidney Disease (ADPKD). Kidney Int 2025; 107(2S): S1-239 2 Casteleijn NF et al.: Tolvaptan and Kidney Pain in Patients With Autosomal Dominant Polycystic Kidney Disease: Secondary Analysis From a Randomized Controlled Trial. Am J Kidney Dis 2017; 69: 210-9 3 Casteleijn NF et al.: Novel treatment protocol for ameliorating refractory, chronic pain in patients with autosomal dominant polycystic kidney disease. Kidney Int 2017; 91: 972-81 4Office fédérale de la santé publique OFSP: https://www.bag.admin.ch/dam/bag/de/dokumente/kuv-leistungen/arzneimittel/beurteilungen-bag-von-arzneimitteln-der-spezialitaetenliste/beurteilungen-01.11.2016/jinarc-neuaufnahme-01.11.2016.pdf.download.pdf/Jinarc%20Neuaufnahme%2001.11.2016.pdf
Das könnte Sie auch interessieren:
Études actuelles sur le traitement de l’ILD
Le terme pneumopathie interstitielle (ILD) est un terme générique désignant un groupe important et hétérogène de maladies qui se manifestent principalement dans l’espace broncho- ...
Mise à jour 2026: vers la modification de la maladie
Un grand nombre de médicaments biologiques immunomodulateurs et de «small molecules» ont considérablement élargi l’éventail des options thérapeutiques dans les maladies inflammatoires ...
Schémas thérapeutiques de référence plus courts dans la tuberculose
La tuberculose (TB) constitue toujours un défi majeur à l’échelle mondiale. Malgré les progrès, le besoin de schémas thérapeutiques plus efficaces, plus courts et mieux tolérés reste ...