State of the Art der interventionellen Therapie bei Herzrhythmusstörungen
Autorin:
OÄ Dr. Alexandra Schratter
Abteilung für Kardiologie
Klinik Floridsdorf, Wien
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die katheterbasierte Therapie von Herzrhythmusstörungen ist aufgrund der geringen Invasivität und der hochspezialisierten Verfahren eine etablierte Behandlungsoption mit klarer Verankerung in den Leitlinien der europäischen und internationalen Fachgesellschaften. Im Folgenden werden interventionelle Therapiestandards bei häufigen Herzrhythmusstörungen präsentiert.
Keypoints
-
Katheterablation bei symptomatischem paroxysmalem Vorhofflimmern bzw. bei Tachykardie-induzierter Kardiomyopathie als First-Line-Therapie, bei persistierendem Vorhofflimmern nach vorangegangener medikamentöser Therapie
-
Ausgezeichnetes Effizienz- und Sicherheitsprofil der Ablationstherapie aufgrund von hochauflösenden 3D-Mapping-Systemen, multipolaren Mapping-Kathetern und zusätzlichen Features
-
Katheterablation bei ventrikulärer Extrasystolie zur Symptomreduktion und/oder Verbesserung der systolischen Linksventrikelfunktion
-
Baldige Katheterablation bei monomorphen ventrikulären Tachykardien bei ischämischer Kardiomyopathie zur Vermeidung von ICD-Therapien und Verbesserung der Prognose
-
„Leadless pacemaker implantation“ bei hohem Infektionsrisiko oder fehlenden venösen Zugängen der oberen Körperhälfte bzw. nach operativem oder interventionellem Trikuspidalklappenersatz – nunmehr auch atriale „leadless stimulation“ möglich
Katheterablation von Vorhofflimmern und komplexen atrialen Rhythmusstörungen
Vorhofflimmern ist die häufigste Herzrhythmusstörung im Erwachsenenalter. Eine von drei bis fünf Personen über 45 Jahre entwickelt im Laufe ihres weiteren Lebens Vorhofflimmern.1 Laut den aktuellen Leitlinien der European Society of Cardiology2 ist die Katheterablation bei paroxysmalem Vorhofflimmern als Erstlinientherapie oder bei persistierendem Vorhofflimmern nach frustraner medikamentöser Therapie indiziert (jeweils Klasse-IA-Indikation). Auch bei Patient:innen mit manifester Herzinsuffizienz oder Tachykardie-induzierter Kardiomyopathie hat die Katheterablationstherapie von Vorhofflimmern einen großen Stellenwert in den aktuellen Leitlinien.2
Ablationsverfahren mit thermischer Energie (Punkt-für-Punkt-Ablation mittels Hochfrequenzstrom oder Kryoablation mittels Ballonkatheter als Single-Shot- Verfahren) sind in zahlreichen Studien hinsichtlich Effizienz und Sicherheit hinlänglich untersucht worden und weisen mittlerweile jahrzehntelange Erfahrungswerte auf.3
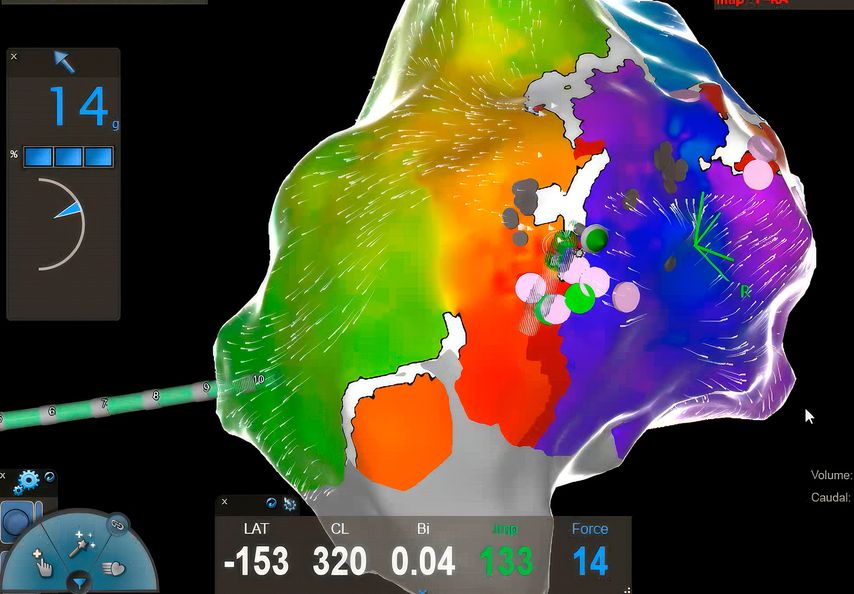
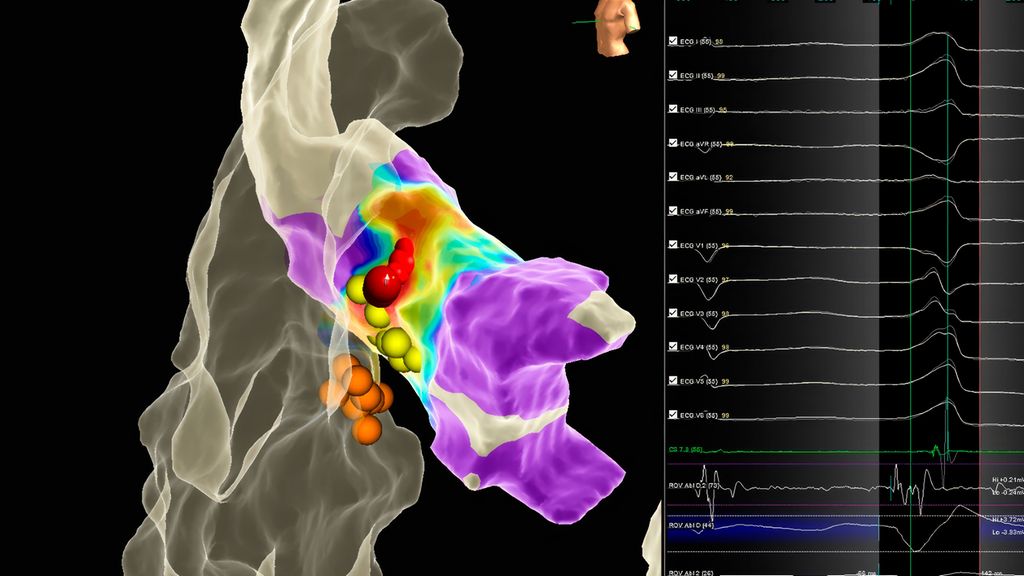
Der große Vorteil von Punkt-für-Punkt-Ablationsverfahren mittels Hochfrequenzstrom ist die Möglichkeit, auch komplexe atriale Rhythmusstörungen abseits der Pulmonalvenenisolation – wie z.B. atypisches rechts- oder linksatriales Vorhofflattern nach vorangegangenen Ablationen oder Herzoperationen – behandeln zu können. Hierbei kommen 3D-Mapping-Systeme sowie hochauflösende multipolare Mappingkatheter zum Einsatz, welche es ermöglichen, innerhalb weniger Minuten zehntausende Mappingpunkte zu erfassen und somit eine extrem akkurate Diagnostik und Therapie der Rhythmusstörung zu gewährleisten (Abb. 1).
Abb. 1: Hochauflösendes 3D-Map des rechten Vorhofs mit farbcodierter Visualisierung der atrialen Tachykardie und Darstellung der undichten Stelle (rosa Punkte) im Bereich der vorbestehenden Ablationsläsion (weiße Linie). Erfolgreiche Ablation an der mittels Map genau definierten Stelle anhand eines Contact-Force-Katheters (14 Gramm Anpressdruck)
In den letzten Jahren hat eine neue Energieform zur Behandlung von Vorhofflimmern zunehmend an Bedeutung gewonnen: die sogenannte „pulsed field ablation“, welche mittels Elektroporation Myokardzellen zerstört.4 Diese Energieform soll sehr selektiv Myozyten schädigen und umliegende Strukturen (Ösophagus, Nervus phrenicus) schonen. Nachdem initial nur multipolare Single-Shot-Devices verfügbar waren, gibt es nunmehr auch die Möglichkeit, mit dieser Energieform eine Punkt-für-Punkt-Ablation vorzunehmen und somit auch Rhythmusstörungen abseits der Pulmonalvenenisolation zu behandeln.5
Katheterablation von ventrikulären Rhythmusstörungen
Die Ablationstherapie bei ventrikulären Rhythmusstörungen ist laut aktuellen ESC-Leitlinien insbesondere bei idiopathischen ventrikulären Tachykardien bei strukturell Herz-gesunden Patient:innen sowie bei anhaltenden ventrikulären Tachykardien bei myokardialen Narben bei ischämischer Kardiomyopathie zur Vermeidung von ICD-Therapieabgaben und Verbesserung der Lebensqualität und des Outcomes indiziert.6
Auch nicht anhaltende ventrikuläre Arrhythmien im Sinne von isolierten Extrasystolen oder kurzen ventrikulären „runs“, wie sie insbesondere bei Ausflusstrakt-Extrasystolie auftreten, können die Lebensqualität der Betroffenen aufgrund der ausgeprägten Symptomatik (Palpitationen, Bradykardie und Schwindel bei Pulsdefizit) stark beeinträchtigen beziehungsweise bei hoher Arrhythmielast zu einer Extrasystolie-induzierten Kardiomyopathie führen.
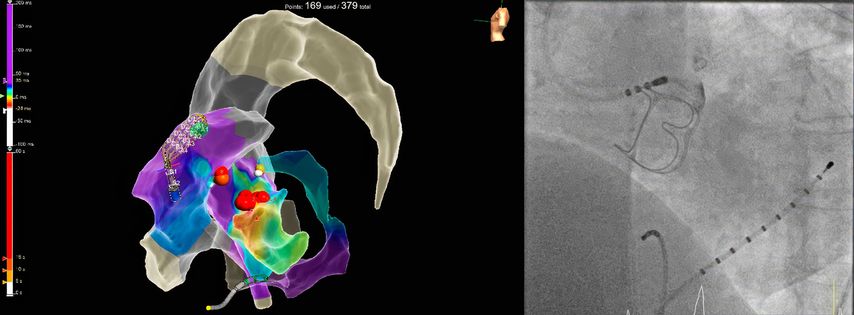
Die Katheterablation von symptomatischen ventrikulären Extrasystolen (VES) oder monomorphen ventrikulären Tachykardien (VT) ohne zugrunde liegende strukturelle Herzerkrankung stellt laut aktuellen ESC-Leitlinien6 im Falle von aus dem rechtsventrikulären Ausflusstrakt (RVOT) kommenden Arrhythmien oder faszikulären Tachykardien eine Klasse-I-Indikation dar. Bei anderen idiopathischen VES/VT-Lokalisationen, z.B. aus dem linksventrikulären Ausflusstrakt (LVOT) entspringenden ventrikulären Arrhyth-mien, ist zunächst ein medikamentöser Therapieversuch mittels Betablockern oder Kalziumkanalblockern indiziert (Klasse-I-Empfehlung), bevor eine Katheterablation in Erwägung gezogen wird (Klasse-IIa-Empfehlung). Dies ist durch die doch komplexere Ablationsprozedur bedingt, da insbesondere LVOT-Arrhythmien oftmals einer Katheterablation schwerer zugänglich sind (Fokus im Aortensinus, im distalen Koronarsinus/„great cardiac vein“). Gegebenenfalls kann ein Ablationsverfahren von mehreren Herzhöhlen ausgehend notwendig sein, entweder konsekutiv (Abb. 2) oder mittels bipolarer Ablation, wo mithilfe eines speziellen Generators die gleichzeitige Energieabgabe über zwei Katheter simultan erfolgen kann.7
Abb. 2: Links: 3D-Rekonstruktion und Aktivierungsmapping mittels multipolaren Mapping-Katheters und erfolgreiche Ablation einer ventrikulären Extrasystolie vom „left ventricular summit“ mittels konsekutiver Energieabgabe im rechtsventrikulären Ausflusstrakt (links im Bild) und linksventrikulären Ausflusstrakt/Aortensinus (mittig – rote Punkte) sowie im distalen Koronarsinus am Übergang zur „great cardiac vein“ (gelber Punkt). Rechts: Kontrastmitteldarstellung des linkskoronaren Aortensinus mittels Kontrastmittelgabe über den Ablationskatheter vor Ablation (unmittelbare Nähe zum Abgang des linken Hauptstamms und zum biologischen Aortenklappenersatz)
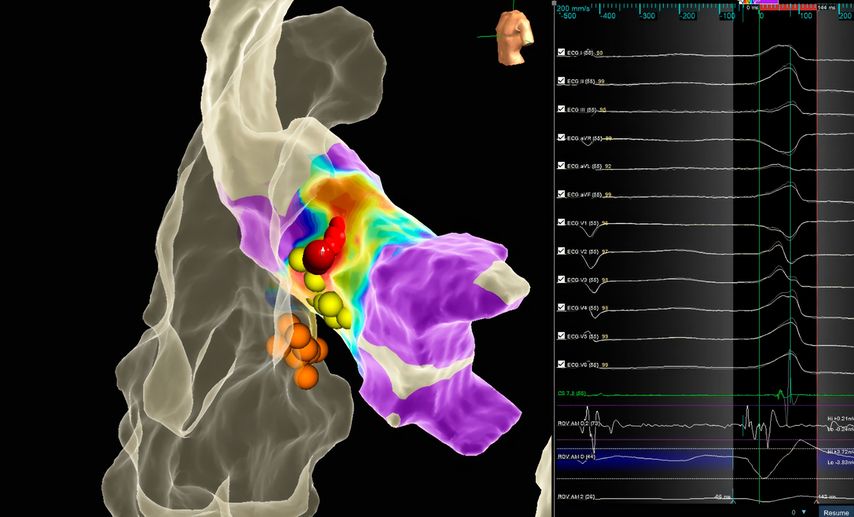
Die hochauflösenden 3D-Mapping-Systeme sind insbesondere dann von kritischer Bedeutung, wenn sehr sensible Strukturen im Rahmen der Ablation geschont werden sollen. In Abbildung 3 ist die erfolgreiche Ablation einer Ausflusstraktextrasystolie im Bereich der Aortenwurzel in unmittelbarer Nähe zum intrinsischen Reizleitungssystem (HIS-Signale) dargestellt.
Abb. 3: Elektroanatomische Rekonstruktion mit Aktivierungsmapping des linksventrikulären Ausflusstrakts/Aortenwurzel mit Ursprung der Extrasystolie in unmittelbarer Nähe zum intrinsischen Reizleitungssystem (HIS-Signal, gelbe Punkte). Erfolgreiche Ablation (rote Punkte) mit vorsichtiger Annäherung an die HIS-Punkte ohne Verlängerung der PQ-Zeit
Die im Rahmen der Katheterablation von monomorphen Kammertachykardien bei struktureller Herzerkrankung gewählte Behandlungsstrategie richtet sich nach der zugrunde liegenden Pathologie. Bei ventrikulären Tachykardien bei ischämischer Kardiomyopathie zeigt sich meistens ein klar begrenztes überwiegend endokardiales Narbenareal, das der Ausdehnung des stattgehabten vorangegangenen Myokardinfarkts entspricht. Das Ventrikelendokard wird im Rahmen der Ablationsprozedur mittels hochauflösender multipolarer Mappingkatheter in Zusammenhang mit einem 3D-Mapping-System kartografiert und es wird ein 3D-Modell des Herzens erstellt, das die vorhandenen Narbenareale in Bezug auf das Gesamtendokard visualisiert. Innerhalb der Low-Voltage-Zone des Narbenareals können zudem stark fraktionierte und Spätpotenziale identifiziert werden, welche noch leitfähigen Myokardstraßen entsprechen, die zumeist kritische Isthmen der klinischen ventrikulären Tachykardien darstellen. Ein Aktivierungsmapping im Sinusrhythmus oder während Stimulation vom rechten oder linken Ventrikel kann Dezelerationszonen der Erregungsfront identifizieren, die für die Entstehung und Aufrechterhaltung von ventrikulären Reentrykreisen verantwortlich sind.8,9 Bei der ischämischen Kardiomyopathie werden dann substratgesteuert wenn möglich alle abnormalen Potenziale an der Narbengrenze und innerhalb der Narbe sowie gegebenenfalls etwaige kritische Dezelerationszonen abliert. Ein Aktivierungsmapping der intraprozedural auslösbaren ventrikulären Tachykardien oder Stimulationsmanöver zur Lokalisation des laufenden Reentry-Kreises sind oft bei hämodynamischer Instabilität nur zeitlich sehr begrenzt oder nicht möglich bzw. muss auf die Kreislaufunterstützung mittels temporären Assist-Devices (Impella, ECMO) zurückgegriffen werden.
Bei nichtischämischer Kardiomyopathie (z.B. nach Myokarditis, bei dilatativer Kardiomyopathie, arrhythmogener rechts- und/oder linksventrikulärer Kardiomyopathie, Sarkoidose oder anderen Systemerkrankungen mit myokardialer Beteiligung) gehen die Narbenareale oft nicht von endokardial aus, sondern es zeigt sich häufig eine mittmyokardiale bzw. epikardiale Beteiligung. Zur Prozedurplanung ist daher insbesondere bei nichtischämischer Kardiomyopathie eine vorangehende kardiale Magnetresonanztomografie empfehlenswert, um das Ablationstarget im Vorfeld zu definieren. Manche der bei nichtischämischer struktureller Herzerkrankung auftretenden klinischen Tachykardien können von endokardial abliert werden, bei anderen ist ein epikardialer Zugang (z.B. von subxiphoidal oder mittels kardiochirurgischen endoskopischen Eingriffs) notwendig. Hierbei werden die Mapping- und Ablationskatheter direkt in den Perikardraum eingebracht, wo Mapping und in weiterer Folge Ablation des epikardialen Substrats erfolgen.
Interventionelle sondenlose Herzschrittmacherimplantation
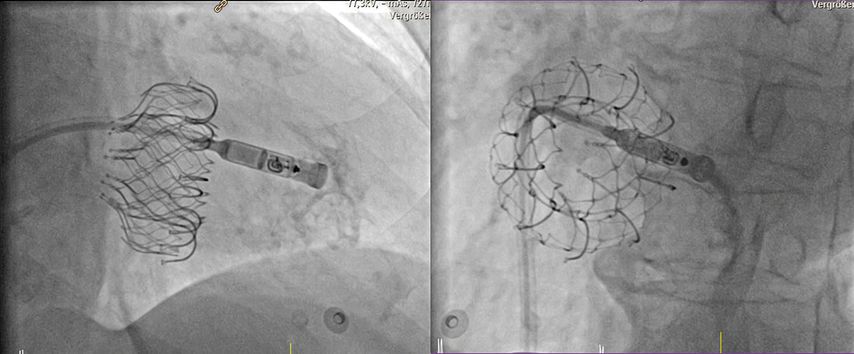
Bei bradykarden Herzrhythmusstörungen gibt es seit 2013 die Möglichkeit, einen sondenlosen Herzschrittmacher mittels Katheterverfahren in den rechten Ventrikel zu implantieren.10,11 Dies kann über die Femoralvene oder über die Jugularvene erfolgen. So können Patient:innen mit bradykardem Vorhofflimmern, aber auch bei z.B. seltenen Reflexsynkopen aufgrund von langen Pausen zwischen den Herzschlägen im VVI-Modus (VVI = ventrikulär, ventrikulär, inhibiert), sowie Betroffene mit höhergradigen AV-Blockierungen im VDD-Modus (VDD = Ventricular-DrivenDual-Chamber) des Herzschrittmachers, interventionell behandelt werden – allerdings mit nur bedingter atrioventrikulärer Synchronität. Der große Vorteil der sondenlosen Herzschrittmachertherapie ist die Tatsache, dass auch Patient:innen mit fehlendem venösem Zugang der oberen Körperhälfte oder bei deutlich erhöhtem Infektionsrisiko (z.B. vorangegangene Schrittmachersysteminfektion, chronische Hämodialyse) einer Schrittmachertherapie zugeführt werden können (Klasse-IIa-Indikation laut aktuellen ESC-Leitlinien).12 Außerdem sind sondenlose Systeme zu favorisieren, wenn ein Zustand nach Trikuspidalklappenersatz besteht (Abb. 4).
Abb. 4: Implantation eines sondenlosen Herzschrittmachers (Medtronic MicraTM) in den rechten Ventrikel bei vorbestehendem interventionellem Trikuspidalklappenersatz (EvoqueTM). Zur optimalen Positionierung wird über den Delivery-Katheter Kontrastmittel verabreicht. Die sondenlose Schrittmacherkapsel ist noch mit dem Delivery-Katheter verbunden. Links: Ansicht von schräg rechts vorne (RAO), rechts: Ansicht von schräg links vorne (LAO)
Seit einigen Jahren kann auch eine Schrittmacherkapsel in den Vorhof implantiert werden.13 Dies ermöglicht zusätzlich zur VVI/VDD-Stimulation nunmehr eine rein atriale bzw. eine DDD-Stimulation. Die sondenlose Herzschrittmachertherapie stellt somit für eine deutlich größere Bandbreite an zugrunde liegenden bradykarden Rhythmusstörungen eine therapeutische Option dar.
Literatur:
1 Linz D et al.: Atrial fibrillation: epidemiology, screening and digital health. Lancet Reg Health Eur 2024; 37: 100786 2 Van Gelder IC et al.: 2024 ESC Guidelines for the management of atrial fibrillation developed in collaboration with the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J 2024; 45(36): 3314-414 3 Parameswaran R et al.: Catheter ablation for atrial fibrillation: current indications and evolving technologies. Nat Rev Cardiol 2021; 18(3): 210-25 4 Verma A et al.: Pulsed field ablation for the treatment of atrial fibrillation: PULSED AF Pivotal Trial. Circulation 2023; 147(19): 1422-32 5 Wenzel JP et al.: Nonthermal point-by-point pulmonary vein isolation using a novel pulsed field ablation system. Circ Arrhythm Electrophysiol 2023; 16(9): e012093 6 Zeppenfeld K et al.: 2022 ESC Guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death. Eur Heart J 2022; 43(40): 3997-4126 7 Futyma P et al.: Bipolar ablation of ventricular arrhythmias: Step-by-step. J Cardiovasc Electrophysiol 2023; 34(12): 2599-606 8 Irie T et al.: Relationship between sinus rhythm late activation zones and critical sites for scar-related ventricular tachycardia: systematic analysis of isochronal late activation mapping. Circ Arrhythm Electrophysiol 2015; 8(2): 390-9 9 Anter E et al.: Ablation of reentry-vulnerable zones determined by left ventricular activation from multiple directions: A novel approach for ventricular tachycardia ablation: A multicenter study (PHYSIO-VT). Circ Arrhythm Electrophysiol 2020; 13(6): e008625 10 Ritter P et al.: Early performance of a miniaturized leadless cardiac pacemaker: the Micra Transcatheter Pacing Study. Eur Heart J 2015; 36(37): 2510-9 11 Reynolds D et al.: A leadless intracardiac transcatheter pacing system. N Engl J Med 2016; 374(6): 533-41 12 Glikson M et al.: 2021 ESC Guidelines on cardiac pacing and cardiac resynchronization therapy. Eur Heart J 2021; 42(35): 3427-520 13 Knops RE et al.: A dual-chamber leadless pacemaker. N Engl J Med 2023; 388(25): 2360-70
Das könnte Sie auch interessieren:
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
Inclisiran bei Patienten mit Statinintoleranz wirksam und sicher
Eine Analyse statinintoleranter Patienten aus dem Phase III Studienprogramm ORION zeigt, dass Inclisiran die LDL-Cholesterinspiegel kardiovaskulärer Hochrisikopatienten, die kein Statin ...