Pathogenese der akuten Myokarditis und der inflammatorischen Kardiomyopathie
Autor:
Prof. Dr. Carsten Tschöpe1–4
1 Klinik für Kardiologie, Angiologie & Intensivmedizin, Deutsches Herzzentrum d. Charité, Berlin
2Charité – Universitätsmedizin Berlin, corporate member of Freie Universität Berlin and Humboldt-Universität zu Berlin
3 DZHK (German Centre for Cardiovascular Research), partner site Berlin
4Berlin Institute of Health at Charité(BIH)–BCRT – Universitätsmedizin Berlin
E-Mail: carsten.tschoepe@dhzc-charite.de
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Akute Myokarditiden und inflammatorische Kardiomyopathien sind immunvermittelte Erkrankungen mit komplexer Pathogenese. Fulminante Verläufe erfordern eine sofortige Diagnostik inklusive endomyokardialer Biopsie (EMB) – innerhalb von 24 Stunden. Die Magnetresonanztomografie (MRT) ist ein wichtiges Frühdiagnostikum, ersetzt aber nicht immer die EMB.
Keypoints
-
Die Pathogenese umfasst infektiöse, autoimmunvermittelte, toxische und genetisch prädisponierte Mechanismen.
-
Ein Virusnachweis muss im klinischen Kontext interpretiert werden – entscheidend sind Entzündungsaktivität und Replikation.
-
Bestimmte vererbbare Mutationen (wie z.B. Desmoplakin) sind mit rezidivierenden inflammatorischen Phasen und arrhythmogener Progression verknüpft.
-
Fulminante Verläufe erfordern rasche Diagnostik, frühzeitige Biopsie und intensivmedizinische Unterstützung.
-
Die MRT ist in der Frühphase sensitiv, verliert aber im Verlauf an Aussagekraft und liefert keine ätiologische Differenzierung.
-
Die biopsiegestützte Differenzierung bleibt Grundlage zielgerichteter Therapien.
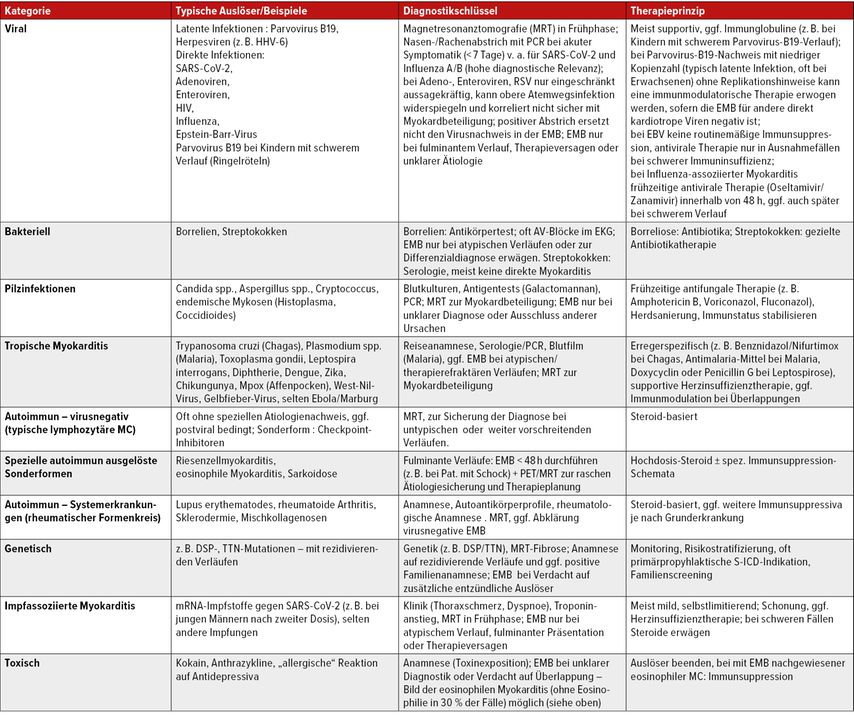
Virale Trigger, bakterielle oder durch Parasiten ausgelöste Infektionen, Autoimmunprozesse, genetische Prädisposition, toxische Substanzen und seltene immunonkologische Nebenwirkungen greifen komplex ineinander in der vielfältigen Pathogenese von Myokarditiden und inflammatorischen Kardiomyopathien.
Die differenzierte Einordnung inflammatorischer Myokarderkrankungen erfordert ein Zusammenspiel aus Klinik, Bildgebung, Histopathologie, Virologie und Genetik. Die MRT ist dabei ein wichtiges Frühinstrument,ersetzt aber nicht die rechts- oder linksventrikulär entnommene EMB, wenn es um die Entscheidung betreffend die spezifische Therapie geht.1,2 Genetische Konstellationen mit inflammatorischen Schüben müssen erkannt und gezielt überwacht werden. Insbesondere fulminante Verläufe bedürfen einer frühen EMB und gezielter, teils intensivmedizinischer Therapie. Die EMB bleibt hierfür der zentrale Schlüssel zur richtigen Weichenstellung.
Immunologische Vielfalt und diagnostische Konsequenz
Myokarditiden sind eine immunologisch heterogene Krankheitsgruppe. Von transienten, postinfektiösen Formen bis hin zu persistierenden Entzündungsreaktionen mit struktureller Progression reichen die klinischen Ausprägungen. Inflammatorische Kardiomyopathien markieren dabei das Übergangsspektrum zur chronischen Herzinsuffizienz. In den meisten Fällen heilen sie unter temporärer körperlicher Schonung und einer leitlinien-gerechten Herzinsuffizienztherapie unkompliziert aus. Komplizierte Fälle benötigen jedoch eine spezielle Diagnostik und spezifische Therapieansätze.
Auslöserspektrum und deren Überlagerung
Klassische virale Auslöser sind beispielsweise Adenoviren, Enteroviren, SARS-CoV-2, Parvovirus B19 oder humane Herpesviren (z.B. HHV-6). Parvovirus B19, der „Ringelröteln-Virus“, kann bei Kindern mitunter schwere Verläufe auslösen; hier kommt in Einzelfällen eine Therapie mit Immunglobulinen infrage. Bei Erwachsenen ist der Nachweis von Parvovirusgenomen im Myokard häufig, jedoch meist mit niedriger Kopienzahl und ohne Krankheitswert eher Ausdruck einer früheren Exposition. Eine komplette Eliminierung durch das Immunsystem gelingt, ähnlich wie bei Herpesviren, hier nicht. Serologische Antikörperbestimmungen sind diagnostisch meist unbrauchbar, insbesondere gegen direkt kardiotrope Viren wie Adeno- oder Enteroviren, für die es zudem keine etablierten antiviralen Behandlungsstrategien gibt. Eine Immunsuppression wird in diesen Fällen ausdrücklich nicht empfohlen.2 Eine Ausnahme stellt die Hepatitis-C-assoziierte Myokarditis dar: Hier kann ein immunvermittelter Zytokinstress auftreten, bei dem eine gezielte antivirale Therapie indiziert ist – etwa mit einer Tripeltherapie aus Sofosbuvir, Velpatasvir und Ribavirin. Entscheidend für die klinische Relevanz sind der direkte Virusnachweis und ggf. die Replikationsaktivität in der EMB. Bakterielle Infekte oder die Borreliose-vermittelte myokardiale Reaktion können durch Antibiotika gut behandelt werden. Auch toxische Substanzen wie Kokain, Anthrazykline oder exzessiv konsumierter Alkohol können inflammatorische oder nekrotisierende Veränderungen induzieren. Zudem können entsprechende familiäre Prädispositionen zugrunde liegen.3 Autoimmunvermittelte Myokarditiden, die endomyokardial virusnegativ sind, profitieren von einer meist auf Cortison basierenden immunsuppressiven Therapie.4 Ähnliches gilt für die Begleitmyokarditiden aus dem rheumatischen Formenkreis.
Genetik als Wegbereiter für rezidivierende Myokarditiden
Genetische Varianten – insbesondere Mutationen im Desmoplakin(DSP)-Gen – führen nicht primär zur Myokarditis, sondern prädisponieren im Sinne eines „Second hit“-Modells zu inflammatorischen Schüben mit potenzieller myokarditischer Symptomatik. Im MRT zeigt sich häufig ein typisches Muster subepikardialer oder transmural betonter Fibrosierung, wie es bei der arrhythmogenen rechts- oder linksventrikulären Kardiomyopathie (ARVC) bekannt ist. Diese Formen gehen häufig mit arrhythmogener Progression einher. Die genetische Diagnostik ist essenziell zur Risikostratifikation. Bei Nachweis einer DSP- oder TTN-Mutation sollte ein frühzeitiges rhythmologisches Monitoring erfolgen, ggf. ergänzt durch eine primärprophylaktische ICD-Implantation. Ein kardiologisches Screening von Familienangehörigen ist dringend erforderlich.3
Diagnostik: Bildgebung und Biopsie gezielt kombinieren
Die kardiale MRT spielt eine zentrale Rolle bei der initialen Abklärung. Sie erlaubt die nichtinvasive Darstellung entzündlicher Veränderungen, Ödeme (in T2-Sequenz) und Narbenmuster („late gadolinium enhancement“; LGE). Ihre Sensitivität ist in der Frühphase hoch, nimmt aber mit zunehmender Chronifizierung ab. Zudem liefert sie keine Hinweise auf Ätiologie oder immunhistologische Differenzierung. In Fällen mit schwerem Verlauf, Therapieresistenz oder unklarer Ätiologie ist daher die EMB essenziell – insbesondere zum Ausschluss spezifischer Entitäten wie Riesenzellmyokarditis, Sarkoidose oder eosinophiler Myokarditis.2
Fulminante Verläufe – rasches Handeln ist entscheidend
Die fulminante (FM) Myokarditis ist eine Sonderform mit plötzlichem Pumpversagen, häufig biventrikulär, oft mit kardiogenem Schock. Sie erfordert sofortige intensivmedizinische Stabilisierung, inklusive mechanischer Kreislaufunterstützung (z.B. Impella®-Pumpe, venoarterielle extrakorporale Membranoxygenierung; auch VA-ECMO). Die FULLMOON-Studie konnte zeigen, dass ein standardisierter und früher Biopsieansatz bei Verdacht auf fulminante Myokarditis umsetzbar und prognostisch hilfreich ist – entscheidend dabei ist eine Durchführung der EMB innerhalb der ersten 24 Stunden.5 Bei FM-Verlauf ohne gezielte Therapie bleibt die Prognose ungünstig. Dies stellt eine logistische und organisatorische Herausforderung dar, da nur spezialisierte Zentren in der Lage sind, diese Diagnostik und Versorgung in diesem Zeitfenster sicherzustellen.
Sonderform: immunver-mittelte Myokarditis unter Checkpoint-Inhibition
Auch wenn selten, können Immuncheckpoint-Inhibitoren (ICI) wie PD-1- oder CTLA-4-Blocker eine rasch progrediente lymphozytäre Myokarditis induzieren – oft in Kombination mit Myositis oder neurologischen Autoimmunreaktionen. Frühdiagnose, Steroidgabe und ggf. zusätzliche Immunsuppression sind hier entscheidend.6
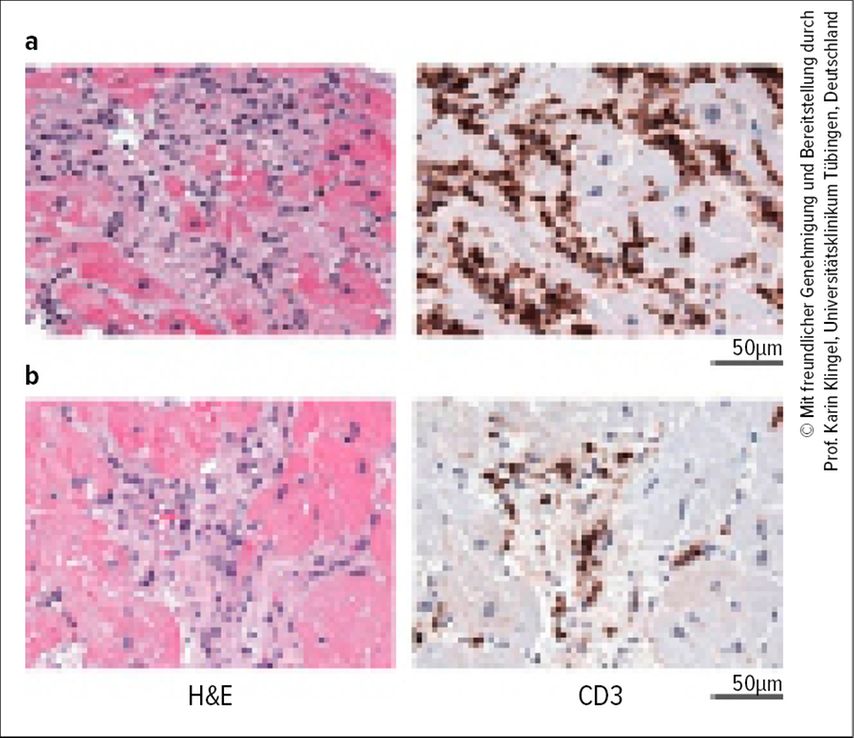
Abb. 1:Akute und abheilende lymphozytäre Myokarditis wird durch Histologie und Immunhistologie von Endomyokardbiopsien diagnostiziert: a) Akute lymphozytäre Myokarditis verursacht durch eine Enterovirus-A71-Infektion. Histologisches Bild mit Nachweis einer Kardiomyozytennekrose (erkennbar in der Hämatoxylin-Eosin(H&E)-Färbung im linken Panel) und immunhistologisches Bild mit diffuser Infiltration von CD3+-T-Zellen (nachgewiesen durch Anti-CD3-Antikörper-Färbung (braun) im rechten Panel). b) Abheilende lymphozytäre immunvermittelte Myokarditis. Histologisches Bild mit Nachweis von Fibrose, jedoch ohne Kardiomyozytennekrose (linkes Panel), immunhistologisches Bild mit Nachweis von infiltrierten CD3+-T-Zellen (rechtes Panel; aus Tschöpe C et al. 2021)2
Impfungen und immunvermittelte Reaktionen
Impfungen, welcher Art auch immer, können in seltenen Fällen Begleitmyokarditiden auslösen. Im Zusammenhang z.B. mit SARS-CoV-2-Impfungen wurden auch Fälle von Myokarditis beobachtet, insbesondere bei jungen Männern nach der zweiten Dosis mRNA-Impfstoff. Diese verlaufen meist mild und selbstlimitierend. Eine generelle Impfskepsis ist daraus nicht abzuleiten.7 Vielmehr schützen Impfungen – gerade gegen respiratorische Viren – vulnerable kardiovaskuläre Patienten indirekt vor infektiösen Myokarditiden.
Therapie nach immunologischer Einordnung
Die Therapie richtet sich nach der Schwere des Krankheitsbildes und der Ätiologie (nach Ergebnissen der histologischen kardialen Biopsie und Inflammationsnachweisen, wie bei fulminanten oder therapieresistenten Verläufen):
-
Autoimmun-/Checkpoint-Inhibitoren(Steroid-basierte Immunsuppression)
-
fulminante Verläufe: intensivmedizinisch, frühzeitige EMB, gezielte Immunmodulation
-
viruspositive EMB mit Replikation: supportive Therapie, fraglich Immunglobuline, antivirale Therapie meist nicht etabliert (Ausnahme: z.B. bei HepatitisC)
-
eosinophile Myokarditis in EMB: Hochdosis-Steroide, ggf. Reslizumab/Mepolizumab
-
Riesenzellmyokarditis in EMB: mit Steroiden, Ciclosporin, ggf. „anti-T-lymphocyte globulin“ (ATG)
-
MRT/Positronen-Emissions-Tomografie mit Fluordesoxyglukose und EMB bei kardialer Sarkoidose: Steroide, ggf. Methotrexat oder TNF-Blocker
-
genetisch assoziiert: supportive Therapie, Risikostratifizierung, Rhythmusüberwachung, ggf. ICD-Implantation, familiäres Screening
-
toxisch: Auslöser beenden, symptomatisch, ggf. Immunsuppression bei Überlappung
Fazit
Die differenzierte Einordnung inflammatorischer Myokarderkrankungen erfordert ein Zusammenspiel aus Klinik, Bildgebung, Histopathologie, Virologie und Genetik. Die MRT ist dabei ein wichtiges Frühinstrument, ersetzt aber nicht die EMB, wenn es um die Frage spezifischer Therapieentscheidungen geht. Genetische Konstellationen mit inflammatorischen Schüben müssen erkannt und gezielt überwacht werden. Insbesondere fulminante Verläufe bedürfen rascher Diagnostik, einer frühen EMB und gezielter, teils intensivmedizinischer Therapie. Die EMB bleibt dann hierfür der zentrale Schlüssel zur richtigen Weichenstellung.
Literatur:
1 Friedrich MG et al.: Cardiovascular magnetic resonance in myocarditis: A JACC White Paper. J Am Coll Cardiol 2009; 53(17): 1475-87 2 Tschöpe C et al.: Myocarditis and inflammatory cardiomyopathy: current evidence and future directions. Nat Rev Cardiol 2021; 18(3): 169-93 3 Drazner MH et al.: ACC expert consensus decision pathway on strategies and criteria for the diagnosis and management of myocarditis: a report of the American College of Cardiology Solution Set Oversight Committee. J Am Coll Cardiol 2025; 4;85(4): 391-431 4 Frustaci A et al.: Randomized study on the efficacy of immunosuppressive therapy in patients with virus-negative inflammatory cardiomyopathy: the TIMIC study. Eur Heart J 2009; 30(16): 1995-2002 5 Huang F et al.: Fulminant myocarditis proven by early biopsy and outcomes. Eur Heart J 2023; 44(48): 5110-24 6 Heemelaar JC et al.: Treatment of immune checkpoint inhibitorassociated myocarditis. J Cardiovasc Pharmacol 2024; 83(5): 384-91 7 Imazio M et al.: Myopericardial complications following Covid-19 disease and vaccination: a clinical consensus statement of the European Society of Cardiology Working Group on Myocardial and Pericardial Diseases. Eur Heart J 2025; doi: 10.1093/eurheartj/ehaf222
Das könnte Sie auch interessieren:
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
Inclisiran bei Patienten mit Statinintoleranz wirksam und sicher
Eine Analyse statinintoleranter Patienten aus dem Phase III Studienprogramm ORION zeigt, dass Inclisiran die LDL-Cholesterinspiegel kardiovaskulärer Hochrisikopatienten, die kein Statin ...