Myokarditis und Perikarditis: Was bringen die neuen ESC-Leitlinien?
Autor:innen:
Ap. Prof. Priv.-Doz. Dipl.-Ing. Dr. Noemi Pavo, PhD
Priv.-Doz. Dr. Max Lenz, PhD
Abteilung für Kardiologie
Universitätsklinik für Innere Medizin II
Medizinische Universität Wien
E-Mail: noemi.pavo@meduniwien.ac.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die neuen ESC-Leitlinien im Bereich Myokarditis und Perikarditis 2025 bringen vor allem drei wesentliche Veränderungen: Die Myokarditis und Perikarditis werden erstmals als gemeinsames Spektrum verstanden und unter dem neuen Oberbegriff inflammatorisches myoperikardiales Syndrom (IMPS) zusammengefasst. Weiters rückt die kardiovaskuläre Magnetresonanztomografie (CMR) klar in den Mittelpunkt der nichtinvasiven Diagnostik. Das Management wird zusätzlich stärker risikobasiert und phänotyporientiert strukturiert, also abhängig davon, ob Brustschmerz, Herzinsuffizienz, Rhythmusstörung, Erguss, Tamponade oder Rezidivneigung im Vordergrund stehen.1
Keypoints
-
Das IMPS-Konzept betrachtet Myokarditis und Perikarditis nicht mehr isoliert, sondern als Spektrum entzündlicher myoperikardialer Syndrome.
-
Die Diagnostik der Myokarditis sollte frühzeitig und strukturiert erfolgen, wobei der CMR eine zentrale Rolle zukommt.
-
Bei klinisch schweren oder unklaren Verläufen sollte die Indikation zur Endomyokardbiopsie großzügig gestellt werden.
-
Patienten mit hämodynamischer Instabilität, ventrikulären Arrhythmien oder hochgradig eingeschränkter LVEF sollten frühzeitig als Hochrisikopatienten erkannt werden.
-
Die Myokarditis wird supportiv und ätiologiegeleitet behandelt, während die Perikarditis primär mit ASS/NSAID plus Colchicin therapiert wird.
-
Kortikosteroide sollten nur selektiv eingesetzt werden, und Anti-IL-1-Therapien haben bei rezidivierender Perikarditis klar an Bedeutung gewonnen.
Eine der wichtigsten Neuerungen ist die Einführung des Begriffs IMPS. Dahinter steckt die klinisch sinnvolle Beobachtung, dass Myokard und Perikard anatomisch benachbart sind sowie dass damit verbundene Krankheitsbilder oft ähnliche infektiöse oder nichtinfektiöse Ursachen haben und sich nicht selten überlappen. Die Leitlinie denkt daher nicht mehr nur in den Kategorien der isolierten Myokarditis oder der isolierten Perikarditis. Vielmehr geht sie von einem Kontinuum von Perikarditis über Myoperikarditis/Perimyokarditis bis zur Myokarditis aus. Dies stellt sich für die Praxis besonders hilfreich heraus, da die frühe Erstbeurteilung oft noch keine endgültige Zuordnung erlaubt. Die Stadieneinteilung wurde klarer definiert:
-
akut bis 4 Wochen,
-
subakut bzw. persistierend von >4 Wochen bis 3 Monate,
-
chronisch >3 Monate,
-
Unterscheidung des Rezidivs, der Remission ohne Residuen und der Remission mit Residuen
Gerade die Remission mit Residuen ist klinisch bedeutsam, da Patienten symptomfrei sein können, aber weiterhin „late gadolinium enhancement“ (LGE), Funktionsstörungen oder Biomarkerauffälligkeiten aufweisen können. Das hat direkte Konsequenzen für Sportfreigabe, Nachsorge und Prognose.
Diagnostik: CMR jetzt zentral und Endomyokardbiopsie gezielter eingesetzt
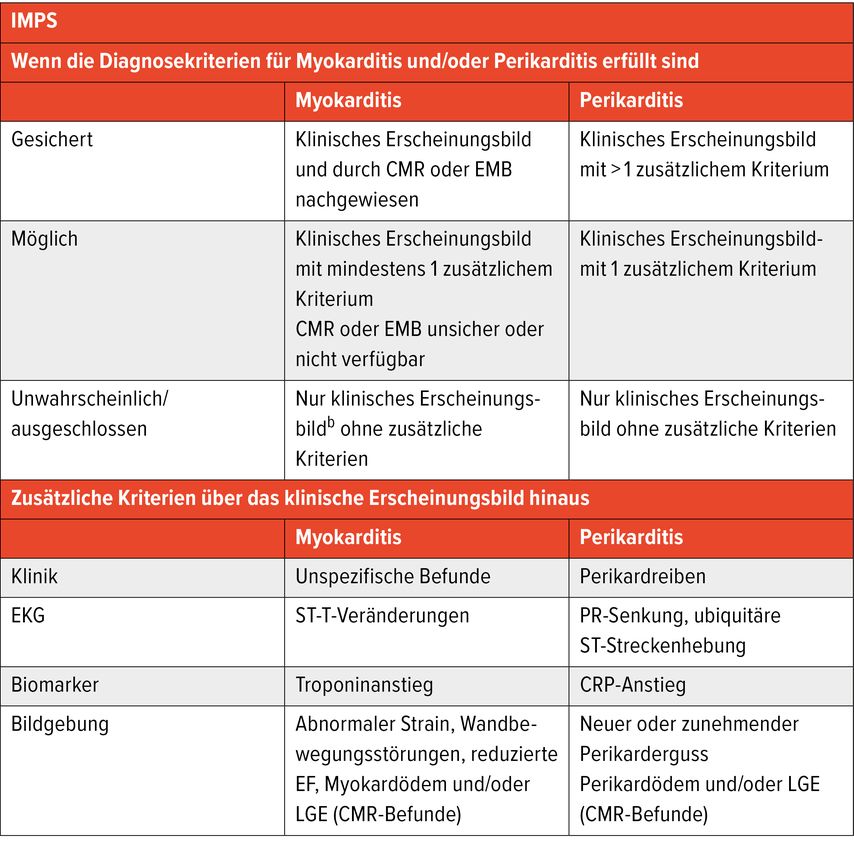
Der vielleicht wichtigste Paradigmenwechsel betrifft die Diagnostik der Myokarditis (Tab.1). Während früher die Endomyokardbiopsie (EMB) im Zentrum der definitiven Diagnose stand, betont die Leitlinie nun, dass sowohl CMR als auch EMB eine definitive klinische Diagnose liefern können — allerdings mit unterschiedlichen Indikationen. Die CMR hat die Rolle eines Schlüsselverfahrens eingenommen.
Für die Myokarditis gilt: Eine gesicherte Diagnose liegt bei passendem klinischem Bild vor, wenn CMR oder EMB positiv sind. Die Leitlinie nutzt dafür die aktualisierten Lake-Louise-Kriterien. Praktisch bedeutet das: Für eine mit CMR nachgewiesene Myokarditis müssen beide Hauptkriterien erfüllt sein: ein T2-basiertes Kriterium für Myokardödem und ein T1-basiertes Kriterium für nichtischämische Myokardschädigung etwa über T1-Mapping“, elektrische Kardioversion (ECV) oder LGE. Ist nur eines der beiden Hauptkriterien erfüllt, bleibt die Myokarditis CMR-seitig unsicher.
Die Diagnose der Perikarditis ist klinischer: Dazu zählen ein passendes klinisches Bild plus mindestens ein zusätzliches Kriterium, etwa Perikardreiben, typische EKG-Veränderungen, CRP-Anstieg oder ein neuer/zunehmender Perikarderguss. Neu ist aber auch hier die stärkere Rolle der CMR, weil sie Perikardödem, perikardiales LGE und Überlappungsformen sichtbar machen kann. Damit gewinnt die Bildgebung besonders bei unklaren, protrahierten oder rezidivierenden Verläufen an Wert.
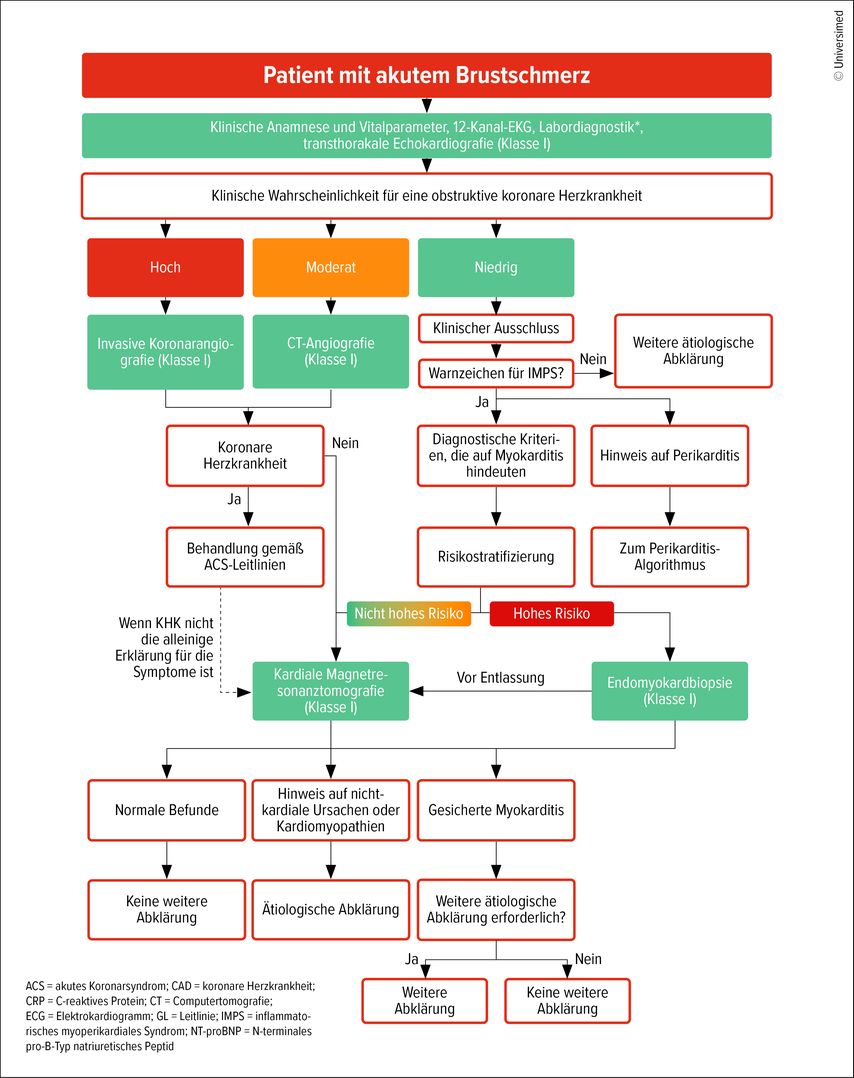
Die neuen Leitlinien betonen eine frühzeitige und standardisierte Diagnostik bei klinischem Verdacht auf IMPS. Ein entsprechender diagnostischer Algorithmus wird in den Leitlinien klar dargestellt (Abb.1). Differenzialdiagnostisch ist dabei stets an ein akutes Koronarsyndrom zu denken, das primär ausgeschlossen werden muss. Bei typischer Symptomkonstellation, insbesondere bei Thoraxschmerz, Dyspnoe oder neu aufgetretenen Arrhythmien in Kombination mit erhöhten kardialen Biomarkern, sollte eine weiterführende Abklärung ohne Verzögerung und konsequent, insbesondere mittels kardialer MRT, erfolgen.
Abb. 1: Diagnostischer Algorithmus bei akutem Thoraxschmerz: Die Labordiagnostik umfasst Troponin, NT-proBNP, C-reaktives Protein sowie ein Differenzialblutbild (nach Schulz-Menger J et al. 2025)1
Der Nachweis von Myokardschädigung und Entzündung sowie das Vorliegen von LGE haben nicht nur diagnostische, sondern auch prognostische Relevanz.2 Darüber hinaus ermöglicht die CMR zunehmend eine differenziertere Einschätzung des Krankheitsverlaufs und kann in der Verlaufskontrolle zur Beurteilung der Remission oder Persistenz entzündlicher Aktivität herangezogen werden.
Die Rolle der EMB bei einer Myokarditis ist in den neuen Leitlinien genauer definiert und insgesamt früher im Krankheitsverlauf empfohlen. Dies gilt insbesondere für Patienten mit fulminanter Präsentation, therapierefraktärer Herzinsuffizienz oder Verdacht auf spezifische Entitäten wie die Riesenzellmyokarditis. Die EMB ermöglicht nicht nur eine histologische Sicherung der Diagnose, sondern auch eine differenzierte immunhistologische und molekularbiologische Charakterisierung, die für therapeutische Entscheidungen wegweisend sein kann. Insbesondere bei schweren Verläufen ist eine frühe Biopsie mit einem längeren Überleben assoziiert.3
Risikostratifizierung essenziell für das weitere Management
Die Leitlinie betont sehr klar, dass der erste diagnostische Schritt nicht die Feindiagnose, sondern die Risikoeinschätzung ist. Typische Red Flags für Myokarditis sind etwa infarktähnliche Brustschmerzen, Arrhythmien, Synkopen, hämodynamische Instabilität, erhöhte Troponine, erhöhte NT-proBNP-Werte sowie Bildgebungshinweise auf Funktionsstörung oder LGE. Für die Perikarditis sind Fieber, Perikardreiben, CRP-Anstieg, Perikarderguss, Polyserositis oder CMR-Hinweise auf Perikardödem/LGE wichtig.
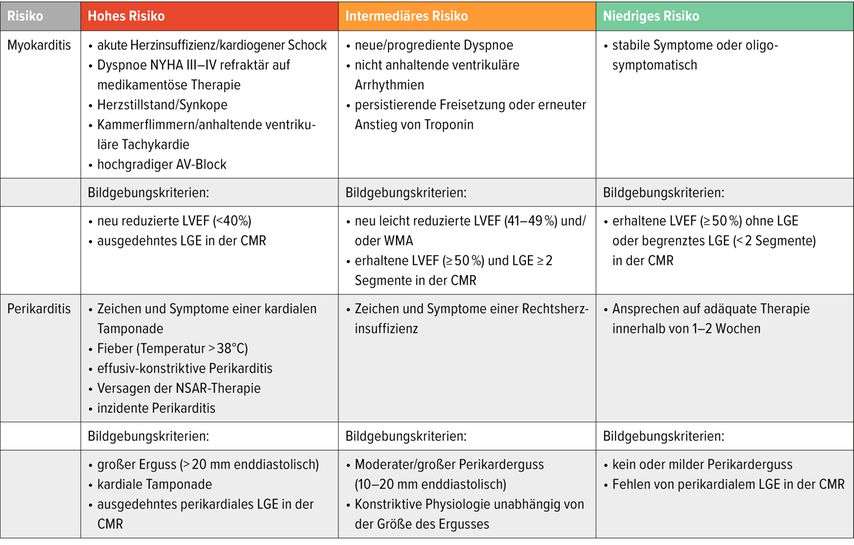
Darauf aufbauend erfolgt die Einteilung in niedriges, mittleres und hohes Risiko (Tab.2). Bei der Myokarditis gelten akute Herzinsuffizienz, kardiogener Schock, Herzstillstand, anhaltende ventrikuläre Tachykardien, hochgradiger AV-Block, LVEF <40% oder ausgedehntes LGE als Hochrisikokriterien. Bei der Perikarditis sprechen Tamponadezeichen, Fieber >38°C, große Ergüsse, exsudativ-konstriktive Verläufe, fehlendes Ansprechen auf NSAID-Therapie oder persistierende Perikarditis für höheres Risiko. Hochrisikopatienten gehören in die stationäre bzw. intensivierte Abklärung.
Therapie und Prognose
Myokarditistherapie supportiv und ätiologiegeleitet
Die Myokarditis hat sich in den letzten Jahren von einer häufig unspezifisch behandelten Erkrankung zu einem klar strukturierten klinischen Syndrom entwickelt. Bei ausbleibender klinischer Besserung, progredienter Symptomatik oder Hinweisen auf einen schweren Verlauf ist eine frühzeitige Überweisung an ein spezialisiertes Zentrum essenziell. Dort kann eine weiterführende Abklärung inklusive einer Endomyokardbiopsie erfolgen.
Therapeutisch ist die Behandlung der Myokarditis in den neuen Leitlinien stärker individualisiert. Die Basis bildet weiterhin die leitliniengerechte Therapie der Herzinsuffizienz bei eingeschränkter Ventrikelfunktion. Ergänzend spielt die konsequente körperliche Schonung in der akuten Phase eine zentrale Rolle. Ein weiterer wichtiger Aspekt ist die differenzierte Bewertung immunmodulatorischer Therapien. Diese sollten nicht routinemäßig eingesetzt werden, sondern gezielt bei nachgewiesenen immunvermittelten Formen der Myokarditis. Insbesondere bei autoimmunen oder entzündlich vermittelten Subtypen kann eine Kortikosteroidtherapie indiziert sein. Eine Hochdosis-Stoßtherapie mit intravenösem Methylprednisolon wird für schwere Formen der lymphozytären, der eosinophilen Myokarditis und der Riesenzellmyokarditis sowie bei kardialer Sarkoidose empfohlen. Gleichzeitig muss betont werden, dass die Evidenzlage, insbesondere für die lymphozytäre Myokarditis, weiterhin begrenzt ist und derzeit durch laufende Studien wie die MYTHs-Studie weiter untersucht wird.5 Eine weiterführende immunsuppressive Therapie wird insbesondere für die Riesenzellmyokarditis und als Zweitlinientherapie bei den anderen immunhistologischen Ätiologien empfohlen.
Hochrisikopatienten sollten engmaschig überwacht werden. In diesen Fällen ist häufig eine frühzeitige intensivmedizinische Betreuung erforderlich. Die rasche Identifikation dieser Patienten ist entscheidend, da sie von einer intensivierten Therapie und gegebenenfalls von mechanischer Kreislaufunterstützung profitieren können. Hierzu zählen insbesondere venoarterielle ECMO-Systeme oder mikroaxiale Pumpensysteme, die als „bridge to recovery“ eingesetzt werden können. Darüber hinaus sollte frühzeitig an einen Transfer in ein spezialisiertes Zentrum mit der Möglichkeit zur Herztransplantation und/oder dauerhaften mechanischen Unterstützung gedacht werden.4
Die Leitlinie erinnert daran, dass viele nicht komplizierte Myokarditiden einen günstigen Verlauf haben. Unkomplizierte Fälle heilen oft spontan aus. Gleichzeitig darf die Erkrankung nicht bagatellisiert werden: Ein Teil der Patienten entwickelt persistierende Funktionsstörungen, Narben oder im Verlauf eine inflammatorische Kardiomyopathie. Besonders problematisch sind fulminante Verläufe, schwere ventrikuläre Arrhythmien und eine protrahierte Entzündung.
Perikarditis: Colchicin wird weiter gestärkt, Anti-IL-1 rückt vor
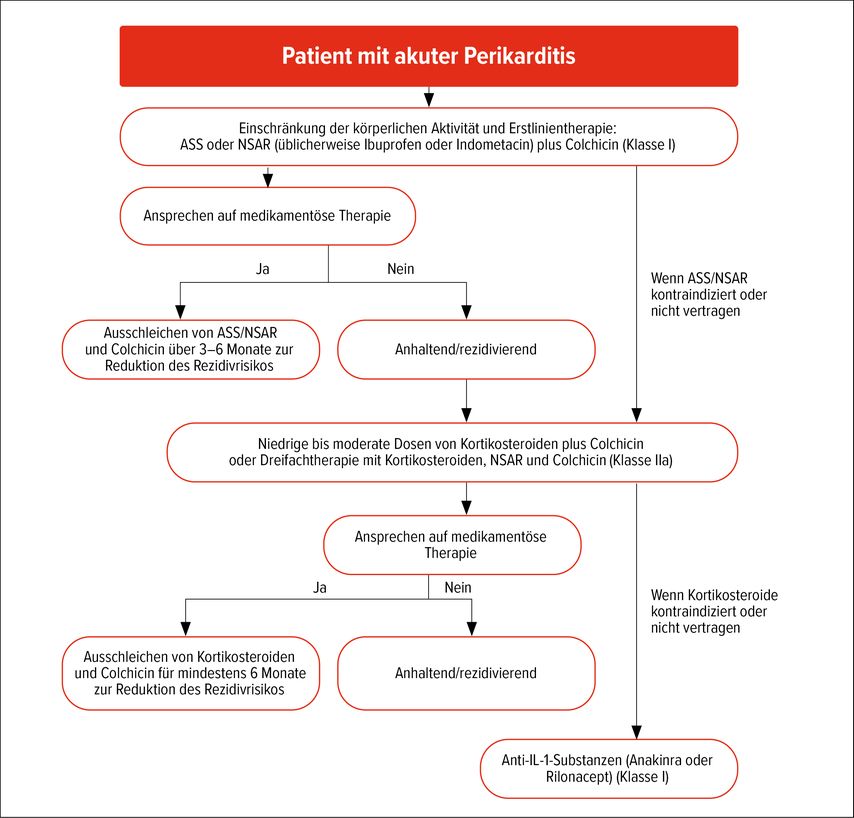
Bei der Perikarditis ist das therapeutische Konzept deutlich weniger komplex und in der Praxis gut umsetzbar (Abb.2).
Erstlinientherapie ist hoch dosiertes ASS oder ein NSAID in antiinflammatorischer Dosierung plus Colchicin, zusätzlich mit einem Protonenpumpenhemmer als Magenschutz. Colchicin wird dabei ausdrücklich als Bestandteil der Erstlinie empfohlen, um Rezidive zu verhindern.
Die Leitlinie präzisiert auch die Dauer: Beim ersten Schub soll Colchicin typischerweise mindestens 3 Monate, bei persistierenden oder rezidivierenden Verläufen mindestens 6 Monate gegeben werden. Wichtig: Colchicin sollte als letztes Medikament abgesetzt werden, wenn eine stabile Remission erreicht ist.
Kortikosteroide werden klar zurückhaltender eingeordnet. Sie sollen nicht als Erstlinientherapie eingesetzt werden, außer bei spezifischer Indikation oder wenn ASS/NSAID und Colchicin kontraindiziert sind bzw. versagen. Wenn Steroide nötig sind, sollen sie in niedriger bis mittlerer Dosierung und idealerweise zusammen mit Colchicin verwendet werden. Auch das langsame Ausschleichen wird betont.
Die größte therapeutische Aufwertung betrifft die Anti-IL-1-Therapie. Anakinra oder Rilonacept werden bei rezidivierender Perikarditis nach Versagen der Erstlinientherapie und Steroiden sowie bei erhöhtem CRP empfohlen. Darüber hinaus sollen sie auch bei persistierender oder rezidivierender Perikarditis mit CMR-Nachweis einer Perikardentzündung nach Versagen oder Unverträglichkeit anderer Therapien erwogen werden — sogar unabhängig vom CRP-Wert. Das ist klinisch hochrelevant, da hier die CMR nicht nur diagnostisch, sondern auch therapieentscheidend eingesetzt wird.
Bei der Perikarditis ist die Prognose der akuten idiopathischen/viralen Form meist gut, aber die Rezidivneigung bleibt eines der zentralen Probleme. Die Leitlinie versteht Rezidive nicht als Randproblem, sondern als eigenständige therapeutische Herausforderung.
Körperliche Aktivität und Nachsorge
Ein weiterer praxisrelevanter Punkt ist die stärkere Betonung von Schonung, strukturierter Nachsorge und kontrollierter Rückkehr zur Aktivität. Schon bei akuter Perikarditis gehört körperliche Schonung ausdrücklich zur Erstlinientherapie. Bei Myokarditis ist die Belastungssteuerung noch wichtiger, da Aktivität bei fortbestehender Entzündung oder arrhythmogenem Substrat potenziell riskant ist. Die Leitlinie verankert körperliche Aktivität deshalb als eigenen Themenblock. Außerdem wird die Verlaufskontrolle mit CRP und gegebenenfalls CMR für die Beurteilung der klinischen Remission und Steuerung der Therapiedauer empfohlen. In unkomplizierten Fällen genügt eine klinische Nachsorge mit oder ohne Echokardiografie. Das ist besonders für die Frage wichtig, wann Medikamente ausgeschlichen oder sportliche Belastungen wieder aufgenommen werden können. Die Entscheidung über die Wiederaufnahme sportlicher Aktivität sollte individuell und unter Berücksichtigung klinischer, bildgebender und laborchemischer Parameter erfolgen. Persistierendes LGE oder eine anhaltend eingeschränkte linksventrikuläre Funktion sind mit einer ungünstigeren Prognose assoziiert und sollten entsprechend in die Nachsorgeplanung einbezogen werden.
Zusammenfassung
Praxistipp
Bei jungen oder mittelalten Patienten mit Brustschmerzen ähnlich einem aktuen Koronarsyndrom, Troponinerhöhung und unauffälligen Koronarien muss immer an eine Myokarditis gedacht werden – besonders nach vorausgegangener Infektion. Bei vermeintlich milder Myokarditis ist nicht nur auf die EF zu achten, sondern auch auf LGE. Rhythmusstörungen und persistierende Biomarker können trotz erhaltener Pumpfunktion prognostisch relevant sein und Nachsorge sowie Belastungsfreigabe beeinflussen. Bei Perikarditis muss Colchicin früh und ausreichend lang eingesetzt werden, bis eine stabile Remission erzielt wurde. Zu frühes Absetzen ist ein klassischer Fehler und fördert Rezidive.Die ESC-Leitlinie 2025 stellt einen wichtigen Fortschritt dar, da sie mit dem IMPS-Konzept ein integriertes pathophysiologisches Verständnis myokardialer und perikardialer Entzündung etabliert. Besonders hervorzuheben ist die stärkere evidenzbasierte Integration der CMR als zentrale diagnostische Modalität, wodurch die nichtinvasive Diagnosesicherung deutlich verbessert wird. Die klare Risikostratifizierung und die algorithmische Struktur fördern eine standardisierte und reproduzierbare klinische Entscheidungsfindung. Zudem sind die therapeutischen Empfehlungen, insbesondere bei Perikarditis inklusive IL-1-Inhibition, konsistent mit aktueller Evidenz und translational gut begründet. Insgesamt trägt die Leitlinie zu einer höheren diagnostischen Präzision und einer optimierten Patientensteuerung bei.
Literatur:
1 Schulz-Menger J et al.: 2025 ESC Guidelines for the management of myocarditis and pericarditis. Eur Heart J 2025; 46(40): 3952-4041 2 Ferreira VM et al.: Cardiovascular magnetic resonance in nonischemic myocardial inflammation: expert recommendations. J Am Coll Cardiol 2018; 72(24): 3158-76 3 Schmidt M et al.: Temporary mechanical support in fulminant myocarditis: prognostic factors and clinical implications from the FULLMOON study. Int Care Med 2026; 52(2): 240-51 4 Lenz M et al.: Mechanical circulatory support systems in fulminant myocarditis: recent advances and outlook. J Clin Med 2024; 13(5): 1197 5 Ammirati E et al.: Rationale and study design of the international randomized control trial MYocarditis THerapy with steroids: the MYTHS trial. Eur Heart J 2024; 45(1): ehae666.1239
Das könnte Sie auch interessieren:
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
Inclisiran bei Patienten mit Statinintoleranz wirksam und sicher
Eine Analyse statinintoleranter Patienten aus dem Phase III Studienprogramm ORION zeigt, dass Inclisiran die LDL-Cholesterinspiegel kardiovaskulärer Hochrisikopatienten, die kein Statin ...