Medikamentenadhärenz in der Kardiologie – warum sie über Prognose entscheidet
Autor:
apl. Univ.-Prof. Priv.-Doz. Dr. Georg Goliasch, PhD
Herz Zentrum Währing, Wien
E-Mail: g.goliasch@herzzentrum18.at
Selbst wirksamste kardiovaskuläre Therapien versagen bei mangelnder Adhärenz. Fehlende Einnahme ist eine unterschätzte Hauptursache des Therapieversagens; entscheidend ist die konsequente Anwendung.
Keypoints
-
Medikamentenadhärenz ist ein eigenständiger Prognosefaktor.
-
Therapiekomplexität ist der stärkste Prädiktor für Non-Adhärenz.
-
Fixkombinationen verbessern Adhärenz und klinische Outcomes.
-
Adhärenz ist aktiv gestaltbar und Teil ärztlicher Kernkompetenz.
Die effektivste kardiovaskuläre Pharmakotherapie bleibt klinisch wirkungslos, wenn sie nicht oder nicht korrekt eingenommen wird. Trotz evidenzbasierter Leitlinien, hochwirksamer Substanzen und klar definierter Therapiezielwerte stellt unzureichende Medikamentenadhärenz eine der häufigsten und zugleich am stärksten unterschätzten Ursachen für Therapieversagen in der kardiovaskulären Medizin dar. Für die klinische Praxis bedeutet dies: Eine nachhaltige Prognoseverbesserung beginnt weniger mit der Einführung neuer Wirkstoffe als vielmehr mit der Sicherstellung einer konsequenten Einnahme bestehender Therapien.1
Definition und Begriffsabgrenzung
Die Weltgesundheitsorganisation definierte Adhärenz im Jahr 2003 als das Ausmaß, in dem das Verhalten einer Person – insbesondere Medikamenteneinnahme, Diät und Lebensstilmaßnahmen – mit den gemeinsam vereinbarten Empfehlungen von Gesundheitsfachkräften übereinstimmt.2 Der Begriff ersetzt bewusst den früher gebräuchlichen Terminus „Compliance“, der eine primär passive Rolle der Patient:innen implizierte.
In der klinischen Praxis ist die klare Unterscheidung zwischen Adhärenz und Persistenz essenziell. Adhärenz beschreibt die Qualität der Einnahme, also die korrekte Dosierung, den richtigen Einnahmezeitpunkt und die Regelmäßigkeit. Persistenz hingegen bezeichnet die Dauer der fortgesetzten Therapie und erfasst Therapieabbrüche oder -unterbrechungen. Beide Dimensionen sind voneinander unabhängig und haben jeweils einen eigenständigen Einfluss auf das klinische Outcome.3
Methoden zur Quantifizierung der Medikamentenadhärenz
Zur Messung der Medikamentenadhärenz werden überwiegend indirekte Verfahren eingesetzt. Am häufigsten kommen die Medication Possession Ratio (MPR) und die Proportion of Days Covered (PDC) zur Anwendung, wobei ein Schwellenwert von ≥80% häufig als Kriterium für „gute Adhärenz“ definiert wird. Diese Parameter basieren auf Verordnungs- und Abgabedaten und eignen sich insbesondere für populationsbasierte Analysen.4
Ergänzend werden elektronische Einnahme-Tracker eingesetzt, die Einnahmezeitpunkte dokumentieren oder Erinnerungsfunktionen bieten. In der klinischen Routine liefern zudem surrogate klinische Marker wertvolle Hinweise, etwa LDL-Cholesterin-Verläufe unter lipidsenkender Therapie oder Blutdruckentwicklungen bei antihypertensiver Behandlung. Allen Verfahren sind relevante Limitationen gemeinsam: Die Abholung eines Rezepts garantiert keine tatsächliche Einnahme, und Selbstberichte unterliegen systematischen Verzerrungen. Die vorhandenen Daten unterstreichen daher die Notwendigkeit einer methodischen Triangulation, um Adhärenz realistisch abzubilden.5
Studienrealität versus Versorgungsalltag
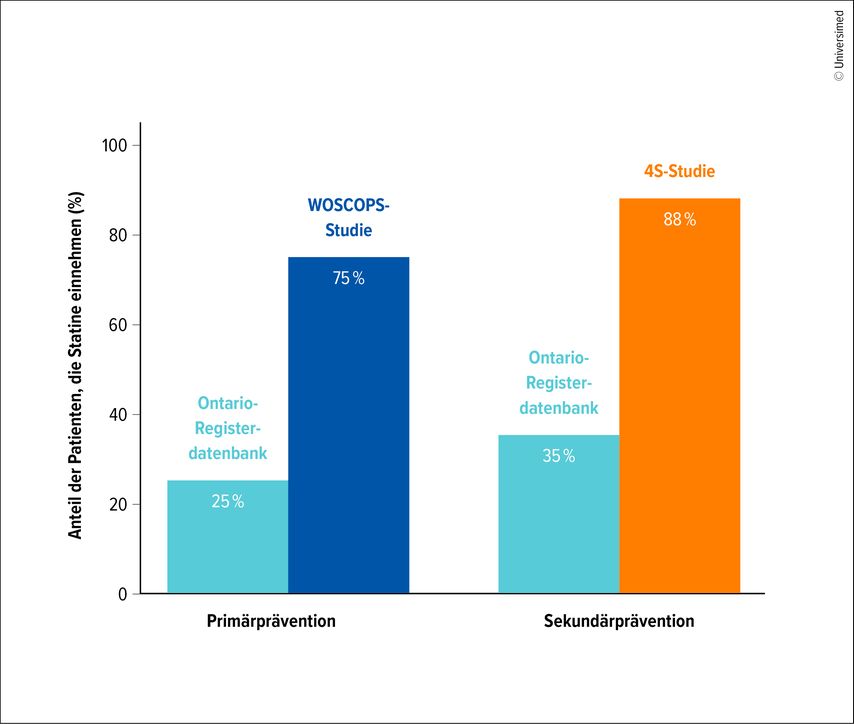
Ein zentrales Problem stellt die Diskrepanz zwischen randomisierten kontrollierten Studien und der Versorgungsrealität dar. Klinische Studien rekrutieren hochselektierte Patient:innen, bieten engmaschige Betreuung und erreichen dadurch Adhärenzraten, die im klinischen Alltag kaum reproduzierbar sind (Abb. 1).6
Abb. 1: Zwei-Jahres-Adhärenz zur Statintherapie in Primär- und Sekundärprävention. Registerdaten (Ontario) zeigen deutlich niedrigere Adhärenzraten im Versorgungsalltag im Vergleich zu randomisierten Studien (WOSCOPS, 4S) und verdeutlichen die ausgeprägte Diskrepanz zwischen Studienrealität und klinischer Praxis (modifiziert nach Kolandaivelu et al.: Eur Heart J 2014)¹
Register- und Versorgungsanalysen zeichnen hingegen ein konsistentes Bild ausgeprägter Non-Adhärenz. Bereits im ersten Jahr nach Initiierung einer antihypertensiven Therapie nehmen viele Patient:innen ihre Medikation unregelmäßig ein oder setzen sie vollständig ab. Adhärenzkurven zeigen einen steilen Abfall innerhalb der ersten Monate – ein Muster, das sich über verschiedene kardiovaskuläre Indikationen hinweg reproduzieren lässt.7
Klinische Konsequenzen der Non-Adhärenz
Die prognostische Relevanz mangelnder Adhärenz ist eindeutig belegt. Bei Patient:innen mit arterieller Hypertonie ist Non-Adhärenz mit einem signifikant erhöhten Risiko für Myokardinfarkt, Schlaganfall und Hospitalisierung assoziiert. In großen Kohortenanalysen mit mehr als 25000 Hypertoniker:innen zeigte sich eine klare Dosis-Wirkungs-Beziehung zwischen Adhärenzgrad und kardiovaskulären Ereignissen.8
Auch in der kardiovaskulären Sekundärprävention ist der Zusammenhang konsistent: Nach Myokardinfarkt oder bei manifester atherosklerotischer Erkrankung führt eine unzureichende Einnahme von Statinen und ACE-Hemmern zu einer signifikant schlechteren Prognose. Ereigniskurven trennen sich früh zugunsten adhärenter Patient:innen, wobei sich dieser Effekt im Langzeitverlauf weiter verstärkt.9
Bei Herzinsuffizienz ist Adhärenz ebenfalls ein entscheidender Outcome-Prädiktor. Aktuelle Übersichten zeigen, dass eine konsequente Einnahme der prognoseverbessernden Basistherapie mit signifikant niedrigeren Hospitalisierungs- und Mortalitätsraten einhergeht.10
Therapiekomplexität als zentraler Einflussfaktor
Ein konsistentes Kernergebnis der vorliegenden Evidenz ist der enge Zusammenhang zwischen Therapiekomplexität und Adhärenz. Mit steigender Tablettenanzahl und zunehmender Einnahmefrequenz sinkt die Therapietreue nahezu linear.11
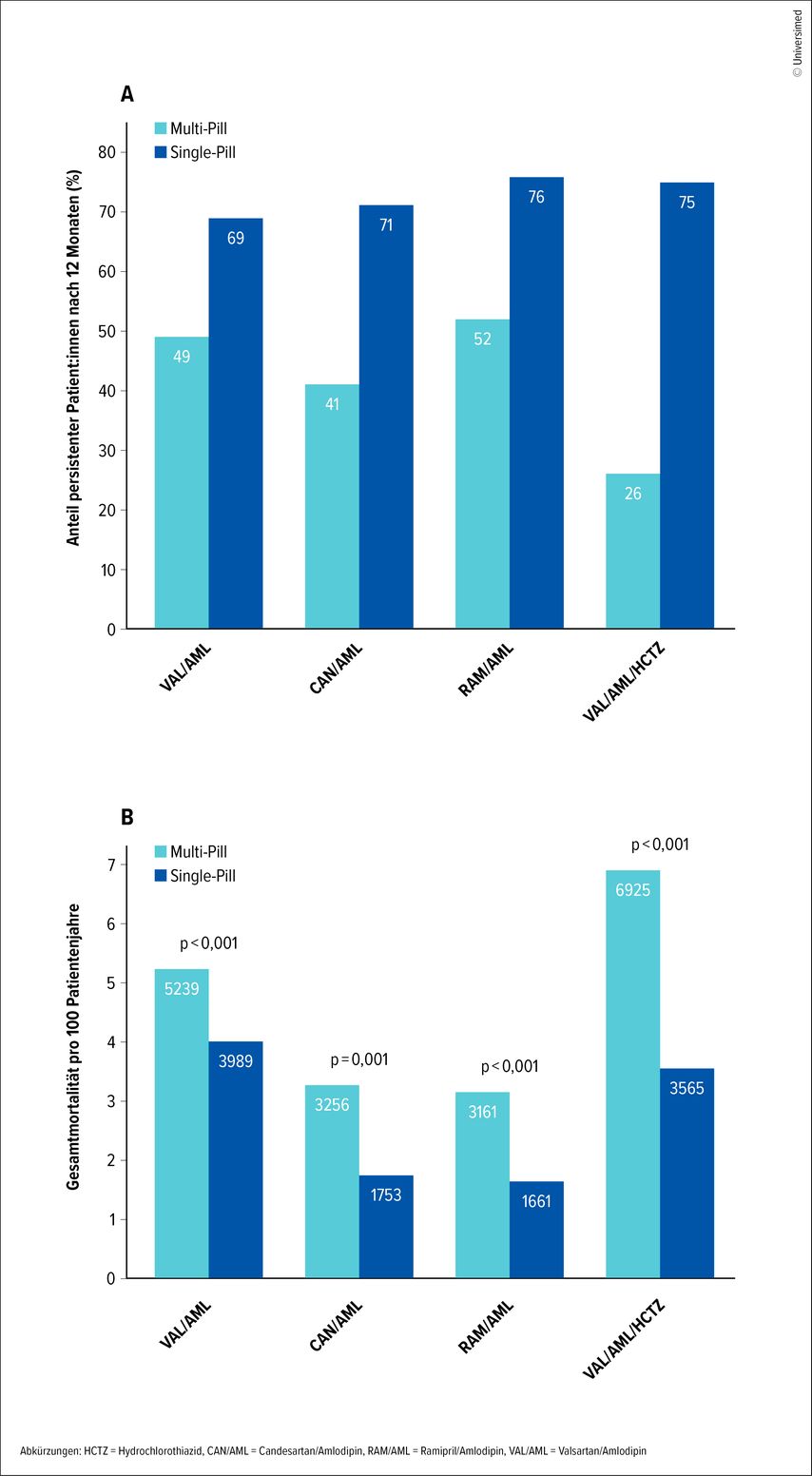
Besonders überzeugend sind die Daten zu Single-Pill-Kombinationen. Im Vergleich zu freien Kombinationen zeigen Fixkombinationen eine signifikant höhere Persistenz über Monate und Jahre. Diese verbesserte Persistenz geht nicht nur mit besseren Surrogatparametern wie Blutdruckkontrolle einher, sondern übersetzt sich auch in harte klinische Endpunkte, einschließlich Gesamtmortalität und kombinierter Endpunkte aus Hospitalisierung und Tod (Abb.2).12,13
Abb. 2: Persistenz und Gesamtmortalität unter Single-Pill- vs.freien Kombinationen. A) Anteil persistenter Patient:innen nach 12 Monaten unter Single-Pill-Kombinationen (SPC) im Vergleich zu Multi-Pill-Kombinationen (MPC), basierend auf verordneten und abgeholten definierten Tagesdosen. B) Gesamtmortalität pro 100 Patientenjahre in gematchten SPC- und MPC-Kohorten. Über alle Wirkstoffkombinationen hinweg sind SPCs mit höherer Persistenz und signifikant geringerer Mortalität assoziiert (modifiziert nach Schmieder et al.: Hypertension 2023)¹³
Ein prominentes Beispiel stellt das Polypill-Konzept dar, das mehrere therapeutische Targets der Atherosklerose in einer Tablette adressiert. Im SECURE-Trial führte dieser Ansatz zu einer signifikanten Verbesserung der Adhärenz und zu einer Reduktion kardiovaskulärer Ereignisse.14
Gesundheitsökonomische Implikationen
Eine verbesserte Medikamentenadhärenz ist nicht nur aus klinischer, sondern auch aus gesundheitsökonomischer Sicht von zentraler Bedeutung. Versorgungsanalysen zeigen konsistent, dass eine höhere Persistenz mit signifikant niedrigeren Gesamtkosten im Gesundheitssystem assoziiert ist.15 Dabei steigen zwar die direkten Arzneimittelausgaben infolge einer konsequenteren Einnahme, diese Mehrkosten werden jedoch durch eine deutliche Reduktion kostenintensiver Hospitalisierungen, Akutinterventionen und kardiovaskulärer Folgeereignisse mehr als kompensiert.
Insbesondere bei chronischen kardiovaskulären Erkrankungen mit hoher Ereignislast – wie arterieller Hypertonie, koronarer Herzkrankheit und Herzinsuffizienz – stellt Non-Adhärenz einen wesentlichen Kostentreiber dar. Wiederholte Krankenhausaufenthalte, eskalierende Therapiestrategien und invasive Maßnahmen sind häufig Ausdruck eines scheinbaren Therapieversagens, das in Wirklichkeit auf unzureichende Medikamenteneinnahme zurückzuführen ist. Gesundheitsökonomische Modellierungen legen nahe, dass Interventionen zur Verbesserung der Adhärenz – insbesondere strukturelle Maßnahmen wie Fixkombinationen – zu den kosteneffektivsten Strategien in der kardiovaskulären Prävention zählen. Damit ist Adhärenz nicht nur ein individueller Prognosefaktor, sondern ein zentraler Hebel für eine nachhaltige und ressourcenschonende Versorgung auf Systemebene.
Strategien zur Verbesserung der Adhärenz
Aus der vorliegenden Evidenz lassen sich klare und praxisrelevante Strategien ableiten. Der entscheidende Ansatzpunkt liegt weniger in patientenseitigen Verhaltensänderungen als in der ärztlichen Gestaltung der Therapie. Die wirksamste Intervention zur Verbesserung der Adhärenz ist die konsequente Reduktion der Therapiekomplexität.
Fixkombinationen spielen hierbei eine Schlüsselrolle. Zahlreiche Studien zeigen, dass Single-Pill-Kombinationen im Vergleich zu freien Kombinationen eine signifikant höhere Persistenz über Monate und Jahre erreichen.12,13 Dieser Effekt ist konsistent über unterschiedliche Wirkstoffklassen und Indikationen hinweg und erklärt sich durch die Reduktion der täglichen Tablettenanzahl sowie eine vereinfachte Einnahmestruktur. Entscheidend ist, dass sich die verbesserte Persistenz nicht nur in besseren Surrogatparametern widerspiegelt, sondern auch in einer Reduktion harter klinischer Endpunkte.
Ergänzend ist die Einnahmefrequenz ein zentraler Faktor. Einmal tägliche Einnahmeregime sind mit einer höheren Therapietreue assoziiert als mehrfach tägliche Dosierungen. Wo immer pharmakologisch möglich, sollte daher ein 1× tägliches Regime angestrebt werden. Auch organisatorische Aspekte sind relevant: Die Synchronisation aller Dauermedikamente auf gemeinsame Abholtermine reduziert logistische Hürden und unterstützt die langfristige Therapiekontinuität.
Das Polypill-Konzept stellt eine konsequente Weiterentwicklung dieser Prinzipien dar. Durch die Kombination mehrerer prognoserelevanter Wirkstoffklassen in einer Tablette adressiert es gleichzeitig verschiedene pathophysiologische Targets der Atherosklerose.
Praxistipp
Fragen Sie statt „Nehmen Sie Ihre Medikamente?“ besser: „Wie nehmen Sie Ihre Medikamente konkret ein?“ Das zeigt Non-Adhärenz und eröffnet die Möglichkeit, Therapiepläne gezielt zu vereinfachen.Patient:innen-Tools wie Wochenboxen oder digitale Erinnerungsanwendungen können die Adhärenz zusätzlich unterstützen, sollten jedoch als Ergänzung und nicht als Ersatz struktureller Therapievereinfachung verstanden werden. Ihr Nutzen ist besonders dann hoch, wenn sie gezielt ausgewählt und in ein ärztlich begleitetes Gesamtkonzept integriert werden.
Digitale Gesundheitsanwendungen können die Medikamentenadhärenz zusätzlich unterstützen, insbesondere bei jüngeren oder technikaffinen Patient:innen. Gesundheits-Apps ermöglichen Erinnerungsfunktionen, Einnahmedokumentation und teilweise auch die Visualisierung von Therapieplänen. Studien zeigen, dass solche digitalen Interventionen kurzfristig die Regelmäßigkeit der Einnahme verbessern können, insbesondere in der frühen Therapiephase.
Ihr Effekt bleibt jedoch meist moderat und stark abhängig von Nutzerakzeptanz, digitaler Kompetenz und kontinuierlicher Anwendung. Gesundheits-Apps entfalten ihren größten Nutzen daher nicht als isolierte Maßnahme, sondern als Bestandteil eines strukturierten Behandlungskonzepts mit ärztlicher Einbindung. Sie können helfen, Einnahmebarrieren frühzeitig zu identifizieren, ersetzen jedoch weder eine vereinfachte Pharmakotherapie noch die persönliche ärztliche Betreuung.
Unabhängig von der gewählten pharmakologischen Strategie bleibt die ärztliche Begleitung ein zentraler Erfolgsfaktor. Frühe Follow-up-Termine nach Therapiebeginn, strukturierte Nachsorge und das aktive Ansprechen potenzieller Nebenwirkungen sind entscheidend, um frühe Therapieabbrüche zu vermeiden.
Ein praxisnaher Ansatz ist dabei der Wechsel der Fragestellung von „Nehmen Sie Ihre Medikamente?“ hin zu „Wie nehmen Sie Ihre Medikamente ein?“. Lassen Sie sich Einnahmezeitpunkte, Tablettenanzahl und Einnahmeroutine beschreiben. Diese konkrete Exploration des Einnahmeverhaltens deckt Non-Adhärenz häufig frühzeitig auf und eröffnet die Möglichkeit, Therapiepläne gezielt zu vereinfachen – nicht selten mit größerem prognostischem Effekt als eine weitere Eskalation der Medikation.
Literatur:
1 Kolandaivelu K et al.: Non-adherence to cardiovascular medications. Eur Heart J 2014; 35(46): 326-33 2 World Health Organization: Adherence to long-term therapies. WHO, 2003 3 Vrijens B et al.: A new taxonomy for describing and defining adherence to medications. Br J Clin Pharmacol 2012; 73(5): 691-705 4 Tajeu GS et al.: Trends in antihypertensive medication discontinuation and low adherence among Medicare beneficiaries initiating treatment from 2007 to 2012. Hypertension 2016; 68: 565-75 5 Roebuck MC et al.: Medication adherence leads to lower health care use and costs despite increased drug spending. Health Aff (Millwood) 2011; 30(1): 91-9 6 American Heart Association: Heart Disease and Stroke Statistics 7Koenig W et al.: Retrospective real-world analysis of adherence and persistence to lipid-lowering therapy in Germany. Clin Res Cardiol 2024; 113(6): 812-21 8 Böhm M et al.: Effects of nonpersistence with medication on outcomes in high-risk patients with cardiovascular disease. Am Heart J 2013; 166: 306-14 9 Bansilal S et al.: Assessing the impact of medication adherence on long-term cardiovascular outcomes. J Am Coll Cardiol 2016; 68(8): 789-801 10 Savarese G et al.: Heart failure and obesity: translational approaches and therapeutic perspectives. A scientific statement of the Heart Failure Association of the ESC. Eur J Heart Fail 2025; 27(7): 112-21 11 Gupta AK et al.: Risk factors for nonadherence to antihypertensive treatment. Hypertension 2017; 69(6): 111-8 12 Parati G et al.: Adherence to single-pill versus free-equivalent combination therapy in hypertension: a systematic review and meta-analysis. Hypertension 2021; 77(2): 109-17 13Schmieder RE et al.: Improved persistence to medication, decreased cardiovascular events and reduced all-cause mortality in hypertensive patients with use of single-pill combinations: results from the START-Study. Hypertension 2023; 81: 456-65 14 Castellano JM et al.: Polypill strategy in secondary cardiovascular prevention. N Engl J Med 2022; 386: 2161-72 15 Pikkemaat M et al.: Treating hypertension with single pill combinations: a simple strategy to save costs for the patients and payers. J Hypertens 2025; 43(9): 1478-84
Das könnte Sie auch interessieren:
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
Inclisiran bei Patienten mit Statinintoleranz wirksam und sicher
Eine Analyse statinintoleranter Patienten aus dem Phase III Studienprogramm ORION zeigt, dass Inclisiran die LDL-Cholesterinspiegel kardiovaskulärer Hochrisikopatienten, die kein Statin ...